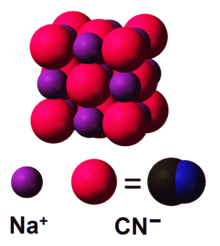
سيانيد الصوديوم
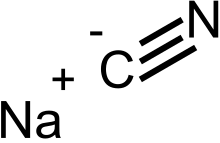
| |
| |
| المُعرِّفات | |
|---|---|
| رقم CAS | |
3D model (JSmol)
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.005.091 |
| رقم EC |
|
PubChem CID
|
|
| رقم RTECS |
|
| UNII | |
| UN number | 1689 |
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | NaCN |
| كتلة مولية | 49.0072 g/mol |
| المظهر | white solid |
| الرائحة | faint almond-like |
| الكثافة | 1.5955 g/cm3 |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | 48.15 g/100 mL (10 °C) 63.7 g/100 mL (25 °C) |
| قابلية الذوبان | soluble in ammonia, methanol, ethanol very slightly soluble in dimethylformamide, SO2 insoluble in dimethyl sulfoxide |
| معامل الانكسار (nD) | 1.452 |
| الكيمياء الحرارية | |
| Standard molar entropy S |
115.6 J·mol−1·K−1 |
| سعة الحرارة النوعية، C | 70.4 J·mol−1·K−1 |
| المخاطر | |
| صفحة بيانات السلامة | ICSC 1118 |
| ن.م.ع. مخطط تصويري |  
|
| NFPA 704 (معيـَّن النار) | |
| نقطة الوميض | Non-flammable |
| الجرعة أو التركيز القاتل (LD, LC): | |
LD50 (الجرعة الوسطى)
|
6.44 mg/kg (rat, oral) 4 mg/kg (sheep, oral) 15 mg/kg (mammal, oral) 8 mg/kg (rat, oral)[2] |
| حدود التعرض الصحية بالولايات المتحدة (NIOSH): | |
PEL (المسموح)
|
TWA 5 mg/m3[1] |
REL (الموصى به)
|
C 5 mg/m3 (4.7 ppm) [10-minute][1] |
IDLH (خطر عاجل)
|
25 mg/m3 (as CN)[1] |
| مركبات ذا علاقة | |
كاتيونات أخرى
|
Potassium cyanide |
مركـّبات ذات علاقة
|
Hydrogen cyanide |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
سيانيد الصوديوم هو مركب كيميائي له الصيغة NaCN، وهو سام مثل كل مركبات السيانيدات. It is a white, water-soluble solid. Cyanide has a high affinity for metals, which leads to the high toxicity of this salt. Its main application, in gold mining, also exploits its high reactivity toward metals. It is a moderately strong base.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التحضير
يحضر سيانيد الصوديوم من أميد الصوديوم وذلك بتسخينه مع الكربون عند 800°س، أي عملياً بإلقاء الفحم في مصهور أميد الصوديوم حيث يتشكل في البداية سيان أميد الصوديوم وذلك حسب التفاعلات التالية:
أ) عند درجة حرارة 600°س
ب) عند درجة حرارة 800°س
هناك طريقة أخرى تتمثل في صهر كلوريد الصوديوم وسيان أميد الكالسيوم معاً في فرن كهربائي.
أما الطريقة التجارية فهي بتعديل حمض سيانيد الهيدروجين بالصودا الكاوية
الاستخدامات
يستخدم في التعدين وذلك في معالجة فلز الذهب، كما يستخدم في تقسية الفولاذ. كما يستخدم أيضاً لتحضير حمض سيانيد الهيدروجين ومركب الأديبونتريل.
تعدين السيانيد
Gold cyanidation (also known as the cyanide process) is the dominant technique for extracting gold, much of which is obtained from low-grade ore. More than 70% of cyanide consumption globally is used for this purpose. The application exploits the high affinity of gold(I) for cyanide, which induces gold metal to oxidize and dissolve in the presence of air (oxygen) and water, producing the salt sodium dicyanoaurate:[3]
- 4 Au + 8 NaCN + O2 + 2 H2O → 4 Na[Au(CN)2] + 4 NaOH
A similar process uses potassium cyanide (KCN, a close relative of sodium cyanide) to produce potassium dicyanoaurate (KAu(CN)2).
Chemical feedstock
Several commercially significant chemical compounds are derived from cyanide, including cyanuric chloride, cyanogen chloride, and many nitriles. In organic synthesis, cyanide, which is classified as a strong nucleophile, is used to prepare nitriles, which occur widely in many chemicals, including pharmaceuticals. Illustrative is the synthesis of benzyl cyanide by the reaction of benzyl chloride and sodium cyanide.[4]
Niche uses
Being highly toxic, sodium cyanide is used to kill or stun rapidly such as in collecting jars used by entomologists and in widely illegal cyanide fishing.
السمية
Sodium cyanide, like other soluble cyanide salts, is among the most rapidly acting of all known poisons. NaCN is a potent inhibitor of respiration, acting on mitochondrial cytochrome oxidase and hence blocking electron transport. This results in decreased oxidative metabolism and oxygen utilization. Lactic acidosis then occurs as a consequence of anaerobic metabolism. An oral dosage as small as 200–300 mg can be fatal.
انظر أيضاً
المراجع
- ^ أ ب ت NIOSH Pocket Guide to Chemical Hazards 0562
- ^ "Cyanides (as CN)". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةUllmann - ^ Adams, Roger; Thal, A. F. (1922). "Benzyl cyanide". Organic Syntheses. 2: 9. doi:10.15227/orgsyn.002.0009.
المصادر
shreve´s chemical process industries, fifth edition, ISBN 0-07-057147-3
وصلات خارجية
- Institut national de recherche et de sécurité (1997). "Cyanure de sodium. Cyanure de potassium". Fiche toxicologique n° 111, Paris:INRS, 6pp. (PDF file, in French)
- International Chemical Safety Card 1118
- Hydrogen cyanide and cyanides (CICAD 61)
- National Pollutant Inventory - Cyanide compounds fact sheet
- NIOSH Pocket Guide to Chemical Hazards
- EINECS number 205-599-4
- CID 8929 from PubChem
- CSST (Canada)
- Sodium cyanide hazards to fish and other wildlife from gold

