التنكس البقعي
| التنكس البقعي | |
|---|---|
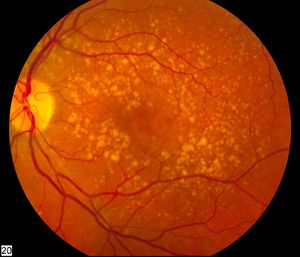 | |
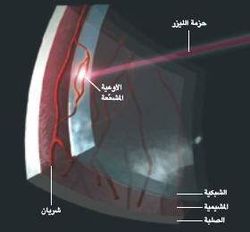
| Picture of the fundus showing intermediate age-related macular degeneration. | |
| التبويب والمصادر الخارجية | |
| التخصص | طب العيون |
| ICD-10 | H35.3 |
| ICD-9-CM | 362.50 |
| DiseasesDB | 11948 |
| MedlinePlus | 001000 |
| eMedicine | article/1223154 |
| Patient UK | فشل عرض الخاصية P1461: لم يتم العثور على الخاصية P1461. التنكس البقعي |
| MeSH | D008268 |
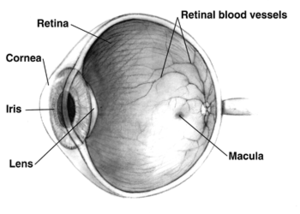

التنكس البقعي المرتبط بالسن Age-related macular degeneration
بدأ الباحثون بتعرّف أسباب هذا المرض البصري المفزع الذي يستهدف المسنين. لاحِظ بعناية عيني صديق لك وهو يقرأ كتابا، سترى أن العينين تدوران من جانب إلى آخر مع كل سطر من النص. إن عينيك تتحركان بالطريقة نفسها عندما تقرأ هذه المقالة. ولفهم مدى أهمية حركة العين هذه حاول قراءة هذه الجملة من بُعد معتاد، مركزًا نظرك على كلمة واحدة. ستكون قادرا على قراءة الكلمات الواقعة ضمن حدود تُقَدر بنحو سنتيمترين عن مركز نظرتك المحدِّقة، ولكنك لن تكون قادرا على قراءة الكلمات الأبعد من ذلك. فإذا كانت رؤيتك سوية ستدرك وجود النص الأبعد، لكنك لن تكون قادرا على رؤيته بالمَيْز المكاني (الحيزي) spatial resolution العالي المطلوب للقراءة. [1]
ثمة حقيقة جديرة بالملاحظة، وهي أننا نمضي حياتنا اليومية غير مدركين أن أقل من %1 من كل صورة يتم استقباله ومعالجته بميز عال. إننا غافلون إلى حد كبير عن هذا الجانب من التصميم، لأن حركات العين السريعة تتيح لنا تركيز بصرنا على ذلك الجزء من الصورة الذي يثير انتباهنا لحظيا. فعندما نركّز بصرنا فإننا ندير عينينا بحيث تقع صورة النقطة ذات الأهمية على المنطقة المركزية من الشبكية (وهي غشاء في رقة الورقة مؤلف من عصبونات (خلايا عصبية) neurons، يبطن الجدار الخلفي لمقلة العين). ويُطلق على هذه المنطقة المركزية التي هي الجزء الوحيد من الشبكية الذي ييسر رؤية عالية الميز، اسم النُّقْرَة (الحُفَيْرَة) fovea؛ وثمة منطقة أكبر قليلا تتمركز على النقرة، تدعى البُقْعَة macula.
إن الجهاز الإبصاري البشري يُحسِن استخدام عدد محدود من العصبونات على نحو فعّال، بتخصيصه أكثر من %99 من الشبكية لمهمة إبصار منخفض الميز. ومع ذلك ينطوي هذا التصميم على خطر ذي شأن؛ إذ إنه إذا تأذى الجزء المركزي من الشبكية بمرض ما فإن المصاب يعاني فقدانا ذا شأن في حدّة acuity البصر في الساحة المركزية للرؤية [انظر الشكل في الصفحة المقابلة]. وهذا ما يحدث في التنكس البقعي، وهو المرض الذي يؤثر في نحو مليوني أمريكي، معظمهم من المسنين. وثمة مواضع قليلة في الجسد البشري حيث يمكن أن يكون لفقدان أو اختلال وظيفي لمثل تلك القطعة البالغة الصغر من النسيج ـ التي يبلغ قطرها نحو ملّيمترين ـ نتائج مروعة كهذه.
إن أطباء العيون قادرون، منذ عهد بعيد، على تشخيص التنكّس البُقْعي على نحو دقيق، غير أن المهمة الصعبة في تحديد أسباب هذا المرض لم تبدأ إلا مؤخرا. ويأمل العلميون ـ بتحديدهم السّيْرورات التي تؤدي إلى تأذي الشبكية المركزية ـ تطويرَ معالجات جديدة بإمكانها إبطاء التنكس البقعي أو إيقافه. وربما يكتشف الباحثون، عاجلا أو آجلا، تقنيات فعّالة لإصلاح التأذي الشبكي.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
كيف تعمل الشبكية
لنبدأ بإلقاء نظرة إلى الشبكية السوية في العين البشرية. يدخل الضوء إلى العين عبر الحدقة، وتُبَئِّرُه العدسة لتشكيل صورة واضحة على الشبكية، حيث تلتقطه عصبونات مستقبلة للضوء تسمى العُصَيّات rods والمخاريط cones [انظر الشكل في الصفحة 23]. إن العصيات مسؤولة عن الرؤية في الضوء الخافت، في حين تعالج المخاريط الرؤية في الضوء الساطع، إضافة إلى رؤية اللون. ولكل خلية مستقبِلة للضوء لاحقة appendage طويلة تدعى الشدفة الخارجية outer segment، وهي مملوءة بپروتينات متخصصة تمتص الضوء، وتضخِّم المعلومات عن شدة المنبه ومدته، وتعمل على نقلها. ويضفي شكل الشدفة الخارجية على الخلايا المستقبلة للضوء المختلفة أسماءَ تُميِّزُها: فالشدفة الخارجية للمخروط تستدق تدريجيا حتى تغدو نقطة، غير أن الشدفة الخارجية للعمود تظل ـ على امتدادها ـ أسطوانية.
وكل شدفة خارجية لمستقبلة ضوئية تمتلئ بمئات الأكياس الغشائية المنبسطة (تدعى أقراصا discs) بعضها مرتب فوق بعض كأكداس الفطائر. تُكوَّن الأقراص والپروتينات المتخصصة في جسم الخلية المستقبلة للضوء، ثم تتجمع عند قاعدة الشدفة الخارجية. وتُصَنِّع كل خلية مستقبلةٍ للضوء نحو %10 من الشدفة الخارجية كل يوم. وما إن تضاف هذه المواد إلى قاعدة الشدفة الخارجية حتى يُقتطع طرف هذه الشدفة، ثم تقوّضه صَفْحةٌ من الخلايا المتخصصة تدعى الظهارة (الطلاء) الصباغية بالشبكية retinal pigment epitheliom (أو اختصارا RPE)، وهي تقع مباشرة وراء الشبكية. والأرجح أن هذه المنظومة أسلوب وجد لتعويض المكونات الپروتينية والليپيدية في الشدفة الخارجية التي عانت تأذيا كيميائيا من التعرض إلى الضوء والأكسجين، وهي سيرورة تعرف باسم الأكسدة الضوئية photo-oxidation.
كذلك تخدم الظهارة RPE الخلايا المستقبِلة للضوء بأساليب أخرى: إنها تصون التركيب الأيوني الصحيح للسائل المحيط بالمستقبلات الضوئية؛ وتعالج وتُعيد تدوير recycle مشتق الڤيتامين A الذي تستخدمه المستقبلات الضوئية من أجل كشف الضوء؛ كما أنها تنقل المغذيات nutrients وترشِّحها من أوعية الدم المشيمانية choroidal التي تقع وراء الظهارة RPE مباشرة. وأخيرا، كما يوحي بذلك اسمها، تكون الظهارة RPE مصطبغة بشدة. وتمتص حبيبات الميلامين في هذه الظهارة الضوء الذي يمر عبر المستقبلات الضوئية، خافضةً إلى الحد الأدنى الفقدان في جودة الصورة الذي يسببه الضوء الشارد داخل العين.
يأمل الباحثون تطويرَ معالجات جديدة تستطيع إبطاء تقدم التنكس البقعي أو إيقافه. إن المَعْلم المميز للتنكّس البُقْعي هو فقدان الرؤية المركزية، غير أن مظهر الشبكية يختلف على نحو كبير من مريض إلى آخر. وفي معظم الأحيان، يرتبط المرض البقعي عند المسنين ـ الذي يُدعى الاعتلال البقعي المتعلق بالعمر age-related maculopathy (أو اختصارا ARM) ـ بفقدان في خلايا الظهارة RPE. فعندما يُنظر إلى الشبكية عبر منظار العين ophthalmoscope يظهر فقدان تلك الخلايا على شكل باحات غير مصطبغة، أو مصطبغة ولكن على نحو غير منتظم. ويمكن تعرف فقدان خلايا الظهارة RPE على نحو أكثر دقة بالتصوير الفلوروسيني (اللاّصِف) للأوعية fluorescein angiography، وهو تقنية تمكِّن أطباء العيون من رؤية الأوعية الدموية للعين بحقن مركب فلوروسيني في تيار الدم. ففي العين السوية يُرى الصباغ الفلوروسيني بسهولة في أوعية الدم الدقيقة ضمن الشبكية، غير أنه لا يُرى ـ أو يُرى بصعوبة كبيرة ـ في الأوعية المشيمانية الأكثر انتشارا؛ لأن هذه الأوعية تقع خلف الاصطباغ الثقيل للظهارة RPE. أما في عين مصابة بالاعتلال ARM فيظهر الصبغ داخل الدورة المشيمانية في أي باحة فقدت خلايا من الظهارة RPE.
كذلك يستطيع التصوير الفلوروسيني أن يكشف عند نحو %10 من المصابين بالاعتلال ARM عن مشكلة أكثر إنذارا بالسوء: أوعية دموية جديدة نامية من داخل الشبكية أو من تحتها تماما، وهي سيرورة يُطلق عليها اسم تكوّن أوعية جديدة neovascularization. ففي الأحوال العادية تقوم صفحة رقيقة، تكونت خارج الخلايا من پروتينات وسلاسل من عديدات التسكّر، تعرف باسم غشاء بروك(1) Bruch's membrane، بفصل أوعية الدم المشيمانية عن الظهارة RPE. إن أي نمو في الأوعية المشيمانية عبر غشاء بروك هو مدعاة للقلق؛ لأن الأوعية الجديدة تكون عرضة للنزف، وهذا يؤدي في النهاية إلى ظهورٍ غير عكوس لندوب في الشبكية. زد على ذلك أن العيوب في غشاء بروك تتيح للسائل التراكم تحت الظهارة RPE أو بين الشبكية والظهارة RPE، وهذه حالة تُضعف التبادل الغازي والغذائي بين الشبكية ومورد الدم المشيماني.
المرض البقعي: نظرة إجمالية
- لرؤية شيء ما بِمَيْز عال، على المُشاهد أن يدير عينيه بحيث تقع صورة الشيء على المنطقة المركزية من الشبكية. إن بإمكان التنكس البقعي أن يؤذي هذه المنطقة بشدة مسببا فقدا ذا شأن في حدة الرؤية.
- يسمى المرض البقعي عند المسنين: الاعتلال البقعي المتعلق بالعمر age-related maculopathy (أو اختصارا ARM). ويؤدي هذا الاعتلال إلى فقد خلايا متخصصة في الشبكية تساعد العصبونات (الخلايا العصبية) المستقبِلة للضوء (الأعمدة والمخاريط).
- لما كان التاريخ الأسري للمرض عاملَ خطورة في الاعتلال ARM فإن الباحثين يحاولون تحديد هُوية الجينات المرتبطة بهذا الاعتلال. ويأمل العلميون ـ بتحليلهم هذه الجينات والپروتينات التي تنتجها ـ معرفةَ كيف يمكن إبطاء تفاقم المرض أو إيقافه.
في العين التامة التكوين، يبدو أن أي فجوات تتشكل ضمن طبقة الظهارة RPE ـ نتيجة لموت الخلايا ـ تُملأ على نحو غير متقن بخلايا جديدة من الظهارة RPE، وربما يكون ذلك بسبب القصور في انقسام الخلايا أو في تمايزها. والسؤال: لماذا تعجز خلايا الظهارة RPE عن العمل أو تموت عندما نتقدم في العمر؟ إن عَقِب أخيل (أو نقطة الضعف) للظهارة RPE ربما يتأتّى من دورها في إعادة تدوير الشدف الخارجية في المستقبلات الضوئية. إن خلايا الظهارة RPE كبيرة ومسطحة، وتقوم كل واحدة منها على إصلاح وصيانة نحو خمسين مستقبلة ضوئية. وهكذا فإن على كل خلية في الظهارة RPE أن تبتلع وتقوض %10 من الشدف الخارجية الخَمسين كل يوم طوال حياة الفرد. ويكافئ هذا القوت اليومي، من حيث الكتلة، خمس خلايا دم حُمْر، جاعلا من خلية الظهارة RPE الخليةَ البلعمية الأكثر فاعلية في الجسد إلى حد بعيد (البَلْعمة phagocytosis هي السيرورة التي تقوم فيها خلية ما بابتلاع المواد وهضمها).
وكلما تقدم الإنسان في العمر، يغدو بإمكان مادة تحت خلوية ـ تُدعى ليپوفوسين lipofuscin ـ التراكم داخل خلايا الظهارة RPE. ويمكن لترسبات صغيرة تدعى البُرَيْقات(2) (الدروزن) drusen أن تتراكم تحت الظهارة RPE مباشرة. ومع أن التركيب الكيميائي الصحيح لليپوفوسين والبريقات غير معروف تماما، فالمرجح أنهما يتألفان ـ جزئيا على الأقل ـ من حطام غير هضوم متخلف عن ابتلاع آلاف الشدف الخارجية. والبريقات هي من الكبر بحيث يمكن رؤيتها بمنظار العين، وترتبط وفرتها على نحو تقريبي بمخاطر فقدان البصر في الاعتلال ARM.
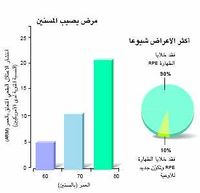
ووفقا للدراسات الوبائية، إن العوامل الوحيدة ذات الترابط الثابت بمخاطر الإصابة بالاعتلال ARM هي: العمر، وامتداد فترة تدخين الشخص للسگائر، ومدى انتشار المرض لدى أسرة هذا الشخص. لقد وجد الاعتلال ARM بين الأمريكيين في نحو 5 و 10 و %20 من الأفراد البالغة أعمارهم 60 و 70 و 80 سنة على الترتيب. ومع أن معظم هؤلاء الأفراد مصابون بالاعتلال ARM في مراحله المبكرة ويعانون فقدانا ضئيلا في الوظيفة الإبصارية، فهم معرضون لخطر تفاقم المرض إلى فقدان أشد خطورة للوظيفة الإبصارية.
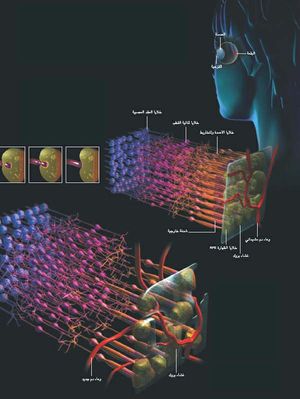
نظرة نافذة إلى داخل العين(****) تقع البقعة في مركز الشبكية، وهي الصفحة الرقيقة من العَصبونات (الخلايا العصبية) التي تبطن الجدار الخلفي للمقلة. ومع أن هذه البقعة لا يتجاوز عرضها مليمترين فإنها تحتوي على مئات آلاف المستقبلات الضوئية، وهي الأعمدة والمخاريط التي تمتص الضوء وترسل المعلومات البصرية إلى الدماغ.
البقعة السليمة

يمر الضوء قبل بلوغ الأعمدة والمخاريط (في اليمين) عبر طبقات من خلايا العقد العصبية وخلايا ثنائية القطب (وهي خلايا شفافة تقريبا). وتتاخم الشدف الخارجية للمستقبلات الضوئية صفحة من الخلايا تسمى الظهارة (الطلاء) الصباغية بالشبكية (RPE). تقوم هذه الخلايا بإعادة تدوير محتويات الشدف الخارجية؛ فكلما نمت شدفة اقتُطع طرفها فتهضمه خلية من الظهارة RPE (في الأسفل).
تأثيرات التنكس البقعي

قد يتدخل التنكس البقعي في إعادة تدوير الشُّدف الخارجية للمستقبلات الضوئية. تتراكم مواد غير هضومة في خلايا الظهارة RPE عاملة على قتلها ببطء. ثم تموت المستقبِلات الضوئية المجاورة. وفي بعض الحالات تخترق أوعية الدم المشيمانية غشاء بروك وتدخل في الشبكية، حيث تستطيع أن تسبب ندوبا غير عكوسة.
الارتباط الوراثي
إن اكتشاف كون التاريخ الأسري للاعتلال ARM عامل خطورة يوحي باحتمال أن يكون للمرض مكوِّن وراثي. وبطبيعة الحال، قد يعكس التعنقد الأسري familial clustering عاملا بيئيا مشتركا أكثر من كونه جينات مشتركة، غير أن دراسات أجريت على توائم متطابقة وتوائم أخوية fraternal twins بينت أن التوائم المتطابقة تُبدي ما يقارب %100 من التوافق في الاعتلال ARM ـ أي إذا كان لدى أحد التوأمين المتطابقين الاعتلال ARM فمن شبه المؤكد أن يوجد أيضا لدى التوأم الآخر. أما بين التوائم الأخوية أو عند الإخوة غير التوائم فسوف يكون التوافق أقل من %50. إن أبسط تفسير لهذه البيانات هو أن لدى التوائم المتطابقة درجة أكبر من التوافق لأنهم متطابقون وراثيا (تتشارك التوائم الأخوية، في المتوسط، في نصف الجينات).
وتقدم البيانات الخاصة بالتوائم أدلة ملزمة على وجود مكوِّن وراثي للاعتلال ARM، غير أنها لا تشير إلى أن هذا يعكس فعل جينة واحدة أو عشر جينات أو مئة جينة، كما أنها لا تقدم لنا أي طريقة بسيطة لتحديد هوية الجينات الوثيقة الصلة بالموضوع. أضف إلى ذلك، أن الاعتلال ARM يبدي تحديا خاصا للطريقة النمطية في تحديد هوية جينات المرض، التي تتضمن دراسة أُسَر تضم عددا كبيرا من الأفراد المتأثرين بالمرض. فضلا عن أن مرضا يحدث متأخرا في الحياة سيصاب به عادة قلة فقط من أفراد الأسرة، لأن كثيرا منهم سيكونون أصغر سنا من أن تظهر لديهم دلائل المرض، في حين أن آخرين سيكونون قد ماتوا قبل ظهور أي أعراض لديهم.
وللتغلب على هذه الصعوبات، ركَّز الباحثون على مجموعة من أمراض بقعية أقل شيوعا ولكنها تحدث باكرا في الحياة وتُوَرَّث وفق أنماط واضحة. ومن بين هذه الأمراض، تعد الاعتلالات الآتية هي المدروسة على نحو أوسع: البُرَيْقات الأسرية السائدة dominant familial drusen، والحَثَل البقعي المُحّي الشكل vitelliform macular dystrophy، وحثل سورسبي القاعي(3) Sorsby's fundus dystrophy، ومرض استارگارت(4) Stargardt. ويؤثر كل من هذه الاعتلالات عادة في الشبكية المركزية، كما أنه يتواكب مع تراكم بعض المواد ضمن الظهارة RPE أو تحتها. ومرض استارگارت هو الأكثر شيوعا بين الأمراض الأربعة، فهو يحدث عند فرد واحد من كل 000 10 شخص. ومع أن هذه الأمراض المبكرة الاستهلال جديرة بالدراسة في حد ذاتها، فإن مشابهتَها الاعتلال ARM تقدم إمكانية إضافية، وهي احتمال أن تمدنا بمفاتيح حاسمة لفهم أسباب الاعتلالات المتعلقة بتقدم العمر.
وكانت هوية الجينات المسؤولة عن هذه الأمراض المبكرة الاستهلال قد حُدِّدت، خلال السنوات العديدة الماضية، عن طريق دراسات بالغة الدقة لأسر مصابة بها. وقد حدد الباحثون في كل حالة موقع الجينة المسببة للمرض في الصبغي (الكروموسوم) بمقارنة الأنماط الوراثية، ثم حددوا هوية الجينة نفسها باكتشاف تغيرات في تسلسلات الدنا DNA (أي طفرات الجينة) تميز المصابين من غيرهم. فلاحظوا في ثلاثة من هذه الأمراض أن أي ضرب من مجموعة متنوعة من الطفرات تَحدث في الجينات الوثيقة الصلة بالموضوع قد يسبب الاعتلال. ولكن مرض البريقات الأسرية السائدة لا يتبع هذه القاعدة، إذ يبدو أن كل من يصاب به يحمل الطفرة نفسها تماما. وتشير البيانات إلى أن المصابين المنتشرين على امتداد أوروبا والولايات المتحدة يتشاركون في سليف مشترك حَمَل هذه الطفرة.
بعد ذلك وجَّه الباحثون انتباههم إلى الپروتينات التي تُنتجها جينات المرض. وآلية مرض استارگارت هي الآن أكثرها اتضاحا لنا. ومع أن هذا الاعتلال يتميز بتراكم شديد للّيپوفوسين في الظهارة RPE، فنحن نعرف الآن أن العيب الأساسي يقع في الشُّدف الخارجية للمستقبلات الاعتلال. تكوّد جينة مرض استارگارت لپروتين ناقل transport protein يستقر في أغشية الأقراص بالشّدف الخارجية ويدعى ABCR. وتشير التجارب إلى أن الپروتين ABCR يستخدم الجزيء ثلاثي فُسْفات الأدينوسين (ATP)، وهو مصدر الطاقة الكيميائية للخلية، لنقل أحد مشتقات الڤيتامين A إلى داخل الخلية المستقبِلة للضوء.
وتفاعُل النقل هذا هو جزء من دورة أكبر تجدد تزويد الشدفة الخارجية للخلية المستقبلة للضوء بالصيغة الحاسمة الحساسة للضوء من الڤيتامين A المسماة الشبكي المقرون 11 11-cisretinal. إن سيرورة امتصاص الضوء تحوِّل الشبكي المقرون 11 إلى مشتق ذي صلة به يسمى الشبكي المفروق الكلي all-trans retinal، يُطلَق في غشاء القرص، ومن ثم يُحوَّر كيميائيا ويُنقل إلى خلية في الظهارة RPE. ولكن عيوبا في الپروتين ABCR تبطئ التحوير الكيميائي «للشبكي المفروق الكلي» مسببة تراكم هذا المركب. ولسوء الحظ يتفاعل هذا الشبكي، تلقائيا وبمعدل منخفض، مع ليپيدات غشاء القرص ليشكِّل مادة تعرف باسم A2E ـ وهي مشتق ثابت يقاوم التقويض. وبِتواصل ابتلاع خلايا الظهارة RPE للشدف الخارجية تتراكم المادة A2E في الخلايا على شكل ليپوفوسين. ويشير دليل حديث إلى أن المادة A2E تضعف عيوشية viability الظهارة RPE، بجعل الخلايا حساسة للتأذي بالضوء.
هل تتعلق آلية مرض استارگارت بآلية الاعتلال ARM؟ ثمة صلة محتملة تعود إلى اكتشاف أن المادة A2E تتراكم أيضا في الظهارة RPE للعين البشرية السوية مع التقدم في العمر، وإن يكن ذلك بمستويات أدنى مما هي عليه في عيون مصابة بمرض استارگارت. وفي الواقع كانت هوية المادة A2E محدَّدة أولا كأحد المكونات الجوهرية للّيپوفوسين في عيون المسنين. ويوحي هذا الاكتشاف بأن تأثيرات المادة A2E في العيون السّوية قد تشابه تأثيراتها في العيون المصابة بمرض استارگارت. وأشارت دراسات وراثية حديثة إلى ارتباط ثان؛ فقد تبين أن الأفراد ذوي الاعتلال ARM يتعرضون لتغيريْن في تعاقب الدنا في جينة الپروتين ABCR بتواتر أكبر مما يحدث عند عموم الجمهور. وتوحي هذه النتيجة بأن بعض حالات الاعتلال ARM على الأقل قد تتأثر بتغيرات في تسلسلات جينة الپروتين ABCR.
ولكن دراسات مماثلة للجينات المسؤولة عن الأمراض الأخرى المبكرة الاستهلال لم تُظهر أي طفرات لتلك الجينات عند المصابين بالاعتلال ARM. ومع ذلك من المهم دراسة تلك الاعتلالات على نحو شامل؛ إذ يمكن لعيوب وظيفية مماثلة تتعلق بالكيمياء الحيوية وبيولوجيا الخلية أن تقوم أيضا بدور ما في الاعتلال ARM. فمثلا، يشير أحد الأبحاث إلى أن الطفرات الوراثية التي تسبب حَثَل سورسبي القاعي يمكن أن تضعف مقدرة العين على تقويض المواد الموجودة خارج الخلايا، مثل غشاء بروك. فعند المصابين بهذا الاعتلال يزداد غشاء بروك ثخانةً ازديادا كبيرا، وهذا يُنقص انتشار المغذيات الأساسية إلى الظهارة RPE والشبكية. أما آليات البُرَيْقات الأسرية السائدة والحَثَل البقعي المحي الشكل فغير مفهومة على هذا النحو الجيد، غير أن الدليل الأولي يوحي بأن هذه الأمراض يمكن أن تتدخل أيضا في العمل الوظيفي السوي لغشاء بروك والظهارة RPE.
وركز خط آخر من البحث على تنكس الشبكية الناتج من سيرورة الرؤية نفسها. فامتصاص الڤيتامين A ومشتقاته الموجودة في الشبكية للضوء يُنتج جذورا حرة فعالة كيميائيا، هي مركبات تحتوي على الأكسجين وبها إلكترونات غير متزاوجة unpaired. لقد أظهرت أبحاث أجريت على كائنات حية تتنوع تنوعا واسعا، يتراوح بين البشر والبكتيرات، أن الجذور الحرة هي مصدر رئيسي لتأذي معظم أشكال الحياة، إن لم يكن جميعها. وإضافة إلى ذلك، توحي دراسات على تنكس الشبكية في حيوانات المختبر أن هذا النمط من التأذي يحدث في المستقبِلات الضوئية والظهارة RPE كليهما. ومن مفارقات الطبيعة أن خاصيات امتصاص الضوء التي تجعل الڤيتامين A ومشتقاته مفيدة جدا كمواد إحساس بصري، هي بعينها التي تجعلها منتجات فاعلة للجذور الحرة.
واستهدف عدد من الدراسات الوبائية epidemiological اختبار التعرض للضوء طوال الحياة كعامل خطورة محتمل للإصابة بالاعتلال ARM. وتُظهر أدلة من بعض هذه الدراسات أن مستويات عالية من التعرض للضوء ربما يمكنها فعلا أن تزيد من مخاطر حدوث الاعتلال. أضف إلى ذلك أن التأذِّي بالأكسدة الضوئية photo-oxidative damage يمكن أن يغدو أشد سوءا بكيماويات من أمثال المادة A2E، التي يفترض أنها تزيد في إنتاج جذور حرة في الظهارة RPE.
كيف تُنقص الشبكية والظهارة RPE التأذي بالأكسدة الضوئية؟ تحتوي الشبكية على تراكيز عالية من بضعة كيماويات مضادة للأكسدة «تتشرّب» الجذور الحرة على نحو فعال. وثمة مركبان من مضادات الأكسدة، هما الزيازانثين(5) zeaxanthin واللوتين(6) lutein، يوجدان بتراكيز عالية في البقعة macula؛ أما مضاد الأكسدة الثالث، وهو الڤيتامين E، فيوجد بتراكيز عالية في الشدف الخارجية للمستقبلات الضوئية، وكذلك في الظهارة RPE. وتأتي جميع مضادات الأكسدة الثلاثة هذه من النباتات؛ فالخضراوات الورقية ذات اللون الأخضر الداكن (مثل السبانخ وبعض ضروب الكرنب) غنية على نحو خاص بالزيازانثين واللوتين.
علينا ألا ننسى أنه في حالة مرض يتفاقم طوال عقود، سيكون لأي علاج يبطئ تقدم المرض بمعدل 10 أو %20 أثر هائل. وثمة دفاعات أخرى تستخدمها خلايا الجسم تتضمن الإنزيم المحتوي على الزنك وهو «فوق أكسيد الديسميوتاز»(7) superoxide dismutase، وإنزيما آخر هو الكاتالاز catalase، وكل منهما يثبط عدة جذور حرة. لقد قادت هذه الملاحظات بعض الباحثين إلى افتراض أن زيادة مقادير الزِّيازانثين واللوتين والزنك في طعام المرء يمكن أن تخفض من احتمال حدوث الاعتلال ARM أو تؤخر استهلاله. ولكن لسوء الحظ أدَّت دراسات وبائية صممت لتقييم العلاقة إلى نتائج متضاربة. وليس هناك إجماع واضح حتى الآن على فعالية أي من الإضافات الغذائية في إنقاص احتمال الإصابة بالمرض البقعي.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
فرص نجاح المعالجات
إن المعالجات الوحيدة المقبولة في الوقت الحاضر للتنكّس البقعي هي تلك التي تهدف إلى تخريب الأوعية الدموية الجديدة التي نمت عبر غشاء بروك. فالتخثير الضوئي photocoagulation، الذي هو عماد العلاج الحالي، يتم بكيّ أوعية الدم بحزمة ليزر شديدة التركيز، توجه إلى هدف تحت الشبكية عبر القرنية والعدسة. ولكن التسخين الموضعي ـ لسوء الحظ ـ يتلف الشبكية في موضع التشعيع على نحو لاعكوس. وثمة معالجة ليزرية جديدة واعدة، تُدعى المعالجة الدينامية الضوئية photodynamic therapy، يمكنها أن تجنِّب غالبا هذه المشكلة، وذلك باستهداف الأوعية الدموية الجديدة على نحو أدق بغية تخريبها. ففي هذه المعالجة يحقن (يُزرق) في وريد المريض صبغ ممتص للضوء يدعى المُحَسِّس الضوئي photosensitizer، ثم توجَّه بعد ذلك حزمة ليزر منخفض الطاقة إلى أوعية الدم الجديدة. وعندما يمتص المحسِّس الضوئي ضوء الليزر ينتج تركيزا عاليا من جذور حرة تخرب أوعية الدم، ولكنها تستثني ـ إلى حد بعيد ـ الشبكية المجاورة. وتُجرى الآن محاولات سريرية متقدمة على المعالجة الدينامية الضوئية، وستكون مُتاحة على نطاق واسع خلال سنة أو سنتين على الأرجح.
ومع أن تكوّن الأوعية الجديدة هو التهديد الأهم للرؤية الذي يطرحه الاعتلال ARM، فإن %90 من هؤلاء المصابين ليس لديهم هذا العَرَض، ومن ثم فهم غير مرشحين لهذه المعالجة. أضف إلى ذلك أن التخثير الضوئي والمعالجة الدينامية لا تصححان سيرورة المرض الأساسية أو تبطئانها، ومن ثَمَّ فإن الأفراد الذين حصلوا على هذه المعالجات سيظلون يعانون نمو أوعية دموية جديدة.
ما الشكل الذي قد تأخذه المعالجات المقبلة؟ يقوم الباحثون بالعمل على اكتشاف عدة طرائق بديلة لإزالة أوعية الدم الجديدة أو إبطاء نموها. وتتضمن هذه الطرائق إزالةً جراحية ميكروية (صِغْرِية) للأوعية الدموية عبر شق صغير في الشبكية، وتشعيعًا عالي الطاقة لمؤخر العين باستخدام تقنيات استعيرت من المعالجة الإشعاعية للسرطان. وهناك مقاربة مهمة أخرى هي تقنية جراحية تجريبية تُدعى تدوير الشبكية retinal rotation. وفي هذه الطريقة تُرفع الشبكية بلطف عن الظهارة RPE التي تحتها، وتُدار بضع درجات حول العصب البصري، ثم تترك لتستقر على الظهارة RPE في موضعها الجديد. وإذا ما حُدِّد قبل الجراحة موضع الفقد الخلوي أو تكوين أوعية جديدة في المنطقة الواقعة تحت النقرة، فسيصير بالإمكان تدوير النقرة بحيث تستقر على منطقة من الظهارة RPE أكثر معافاة. وكما هو متوقع فإن تدوير إحدى الشبكيتين يجعل الدماغ يستقبل إشارات متضاربة من العينين. ولحسن الحظ يمكن حل هذه المشكلة جراحيا بتطويل أو تقصير عضلات شتى حول كرة العين، لإحداث تدوير تعويضي لكامل العين في الاتجاه المعاكس.
ويعد اغتراس خلايا الظهارة RPE إمكانية أخرى مثيرة للاهتمام. ففي دراسات على حيوانات المختبر، غدا العلميون قادرين على تنمية خلايا الظهارة RPE خارج الجسد، ومن ثم اغتراسها تحت الشبكية بمعدلات نجاح عالية. ومن بين الأسئلة المطروحة: هل بمقدور هذه التقنية تأخير فقد وظيفة الإبصار في البشر أو إيقافه. وهل بمقدور التقنيات الجراحية الميكروية أن تبلغ من التطور ما يُمكِّن من وضع الخلايا تحت النقرة على نحو موثوق من دون أن تسبب تأذيا إضافيا. وكما في جميع طرائق الاغتراس، يمكن أن يحد الرفض المناعي البُقيا الطويلة الأمد للخلايا المغترسة إن كانت مستمدة من فرد آخر. ويمكن تجنب هذه المشكلة باستخدام خلايا ممنوحة من الشبكية المحيطية للمريض نفسه.
بل إن بعض الباحثين تخيلوا إصلاح الشبكية نفسها أو إعادة إنمائها. وكان هذا الهدف قد عُدَّ منذ زمن بعيد غير ممكن عمليا، لأن شبكية الثدييات البالغة لا تُبدي دليلا على تمكنها من إجراء مزيد من الانقسامات الخلوية. ولكن نمو الشبكية يحدث طوال حياة الأفراد البالغة في أنواع مختلفة من الأسماك ذات الشبكيات المعقدة تعقيد شبكياتنا نحن. ففي هذه الحيوانات تقطن الخلايا الجذعية (التي يمكنها الانقسام والتميز مكونةً جميع أنماط خلايا الشبكية) عند الحافات الخارجية للشبكية وتوجِّه نموها المستمر. وتشير أبحاث حديثة إلى أن خلايا جذعية مماثلة قد توجد في حالة هاجعة على حافات شبكية الثدييات. وقد يكون بالإمكان تنشيط هذه الخلايا أو اغتراسها لإصلاح التأذي في الشبكية أو في الظهارة RPE.
ولا شك أن تكلفة هذه المعالجات ومخاطرها سيحدان من أن يستخدمها مرضى يواجهون فقدانا إبصاريا شديدا ووشيكا. ومع ذلك، من المرغوب فيه جدا تطوير معالجة أقل بَضْعا less invasive بإمكانها إبطاء الاعتلال عند مرحلة مبكرة أو إيقافه. إن الأبحاث الأساسية في العلل الكيميائية الحيوية والخلوية المسؤولة عن التنكّس البُقْعي سوف تضع الأسس لإنجاز هذا الهدف. ولا يُستبعد افتراض تمكُّن العلميين من إيجاد مركب طبيعي أو صنعي يحسّن أداء خلايا الظهارة RPE أو يَمُد في عَيوشِيّتها. إن مركبا كهذا بإمكانه، مثلا، حماية الظهارة RPE من التأذِّي بالأكسدة الضوئية، أو يحسن فعاليتها في تقويض الشدف الخارجية للمستقبلة الضوئية. ومع أن تحديد هذه التدخلات لعلاج التنكس البقعي قد يبدو طموحا بعيد المنال، علينا ألا ننسى أن أي علاج يبطئ، ولو بنسبة 10 أو %20، من استفحال مرض يتفاقم خلال عقود، سيكون علاجا ذا تأثير هائل.
المؤلفان
Hui Sun - Jeremy Nathans ، عملا معا على الشبكية ثماني سنوات في كلية الطب بجامعة جونز هوپكنز. حصل صَنْ على الدكتوراه في البيولوجيا الجزيئية وعلم الوراثة من جامعة جونز هوپكنز عام 1998، ويعمل الآن زميلا باحثا بعد الدكتوراه. أما ناتانس فهو أستاذ، وكان قد حصل على الدكتوراه في الكيمياء الحيوية والدكتوراه في الطب من كلية طب جامعة استانفورد عام 1987. والمؤلفان عضوان في معهد هوارد هيوز الطبي. ومع أنهما ترعرعا في طرفين متباعدين من الكرة الأرضية (تيانجين في الصين، وبالتيمور في الولايات المتحدة على الترتيب) فإن اهتماماتهما المهنية متماثلة تماما.
الانتشار
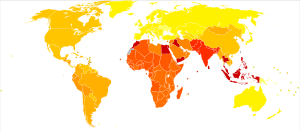
انظر أيضاً
- Cherry-red spot
- Fuchs spot
- Micropsia
- مقالات في المعرفة تتضمن نصوصا من مجلة العلوم.
- بوابة مجلة العلوم
المراجع
- Age-Related Macular Degeneration. Edited by Jeffrey W. Berger, Stuart L. Fine and Maureen G.
- Maguire. Mosby,1999.
- The National Eye Institute's Web site on macular degeneration:
- www.nei.nih.gov/publications/armd.htm
- The Web site of the Foundation Fighting Blindness: www.blindness.org
- The Web site of RetNet, which has information on genetic eye diseases:
- www.sph.uth.tmc.edu/Retnet
- Scientific American, October 2001
المصادر
- ^ مجلة العلوم
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. Retrieved Nov. 11, 2009.
{{cite web}}: Check date values in:|accessdate=(help)