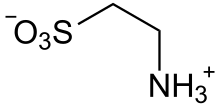
حمض التورين
| |
| |
| الأسماء | |
|---|---|
| اسم أيوپاك المفضل
2-Aminoethanesulfonic acid | |
| أسماء أخرى
حمض التوريك
| |
| المُعرِّفات | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.168 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | C2H7NO3S |
| كتلة مولية | 125.13 g mol-1 |
| المظهر | مادة صلبة بيضاء أو عديمة اللون |
| الكثافة | 1.734 ج/سم3 (عند −173.15 °س) |
| نقطة الانصهار | |
| الحموضة (pKa) | <0, 9.06 |
| مركبات ذا علاقة | |
مركـّبات ذات علاقة
|
Sulfamic acid Aminomethanesulfonic acid Homotaurine |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
التورين (إنگليزية: Taurine؛ /ˈtɔːriːn/)، أو 2-حمض إيثان سولفنيك الأميني، هو حمض سلوفنيك أميني غير مركب للپروتينات ينتشر على نطاق واسع في الأنسجة الحيوانية.[1] وهو مكون رئيسي في العصارة المرارية وقد يتواجد في الأمعاء الغليظة، مشكلاً أكثر من 0.1% من وزن الجسم البشرؤي. اسمه مشتق من الكلمة اللاتينية taurus (اللفظ المقارب لليونانية القديمة ταῦρος، taûros) وتعني الثور، حيث عُزل لأول مرة من عصارة الثيران المرارية عام 1826 بواسطة العالم الألماني فريدريش تيدمان وليوبولد جملين.[2] اكتشف في العصارة المرارية البشرية عام 1846 بواسطة إدموند رونالدز.[3]
يلعب حمض التورين العديد من الأدوار الحيوية، مثل اقتران أحماض الصفراء، كمضاد للأكسدة، تنظيم التناضح، الاستقرار الغشائي، وتعديل إشارات الكالسيوم. وهو ضروري للوظائف القلبية الوعائية، وتطور وعمل العضلات الهيكلية والشبكية والجهاز العصبي المركزي.
تركيزات التورين في النباتات البرية منخفضة للغاية أو لا يمكن اكتشافها، لكن عُثر على وزن رطب يصل إلى 1000 نانومول/جرام في الطحالب.[4][5]
وهو مثال غير اعتيادي للتواجد الطبيعي لحمض السلفونيك.
الخصائص الكيميائية والكيميائية-الحيوية
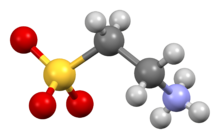
يتواجد التورين كايون مزدوج]] H
3N+
CH
2CH
2SO−
3، كما تم التحقق منه بواسطة دراسة البلورات بالأشعة السينية.[6] لحمض السلفونيك pKa[7] منخفض، مما يؤكد أنه يتأين بالكامل إلى سلفونات عند درجة حموضة الأمعاء.
التخليق
يُحصل على التورين المخلق عن طريق تحلل النشادر من حمض الأيزثيونيك (2-حمض هيدروكسي إيثان سلفونيك)، والذي يحصل عليه بدوره من تفاعل أكسيد الإيثيلين مع ثنائي كبريتيت الصوديوم المائي. يتضمن النهج المباشر تفاعل الأزيريدين مع حمض الكبريتوز.[8]
عام 1993، أُنتج حوالي 5.000-6.000 طن من التورين للأغراض التجارية: 50% لأغذية الحيوانات الأليفة و50% للتطبيقات الدوائية.[9] اعتباراً من 2010، كان لدى الصين وحدها أكثر من 40 مصنع للتورين. تستخدم معظم هذه المصانع طريقة الإيثانولامين لإنتاج معظم الإنتاج السنوي الذي يقارب 3.000 طن.[10]
معملياً، يمكن إنتاج التورين عن طريق ألكلة الأمونيا بدون أملاح بروموإيثان سلفونات.[11]
التخليق الحيوي
يُشتق التورين طبيعياً من السيستين. يحدث تخليق التوراين في الثدييات داخل البنكرياس عبر مسار حمض سلفينيك السيستين. في هذا المسار، يتأكسد السيستين أولاً إلى حمض الكبريتيك، الذي يحفزه إنزيم ديوكسجيناز السيستين. بدوره، يُنزع الكربوكسيل من حمض السلفينيكلسيستين، بواسطة سلفينو ألانين ديكاربوكسيلاز لتشكيل الهيبوتورين. يتأكسد الهيبوتورين إنزيميًا لإنتاج التورين بواسطة [[نازعة هيدروجين الهيبوتورين].[12]
كما يُنتج التورين بواسطة مسار تحويل الكبرتة، الذي يحول الهوموسيستين إلى سيستاثيونين. بعدها يتحول السيستاثيونين إلى هيبوتورين عن طريق العمل المتسلسل لثلاثة إنزيمات: cystathionine gamma-lyase وcysteine dioxygenase و cysteine sulfinic acid decarboxylase. ثم يتأكسد الهيبوتورين إلى تورين كما هو موصوف أعلاه.[13]
أبلغ عن مسار التخليق الحيوي للتورين من السرين والكبريتات في الطحالب الدقيقة،[14] تطوير أجنة الدجاج،[15] وكبد الدجاج.[16] يقوم سيرين الديهيدراتاز بتحويل السيرين إلى [[2-أمينوكريلات] ، والذي يتم تحويله إلى حمض السيستيك بواسطة 3′-فوسفوادينيل سلفات: 2-أمينوكريلات سي-سلفوترانسفيراز. يتم تحويل حمض السيستيك إلى تورين بواسطة ديكاربوكسيلاز حمض السلفينيك سيستين.
الأهمية الغذائية
يتواجد التورين بشكل طبيعي في الأسماك واللحوم.[17][18][19]
يبلغ متوسط المدخول اليومي للتورين في الأنظمة الغذائية لآكلي اللحوم (غير النباتيين) حوالي 58 ملجم (تتراوح من 9 إلى 372 ملجم) ويكون منخفضًا أو مهملاً في النظام الغذائي النباتي الصارم. في دراسة أخرى، قُدر كمية التورين المتناولة بشكل عام بأقل من 200 ملجم/يوماً، حتى في الأفراد الذين يتناولون نظامًا غذائيًا يحتوي على كميات كبيرة من اللحوم. وفقًا لدراسة ثالثة، قدر استهلاك التورين بين 40 و400 ملجم/يومياً.[20]
يتأثر توافر التورين اعتمادًا على كيفية تحضير الطعام، تحتف الوجبات الغذائية النيئة بأكبر قدر من التورين، أما الخبز أو السلق فيؤديان خسارة كمية كبيرة من التورين.[21]
عُثرر على مستويات من التواين أقل بكثير لدى النباتيين مقارنة بمجموعة التحكم في النظام الغذائي الأمريكي القياسي. كان توراين البلازما 78% من قيم التحكم، وكان التورين البولي 29%.[22]
يُعتقد أنه في حالات الولادة المبكرة، يفتقد الأطفال إلى الإنزيمات اللازمة لتحويل السيستاثيونين إلى لالسيستين، وبالتالي قد يصابون بنقص التورين. يوجد التورين في حليب الثدي، ومنذ أوائل الثمانينيات، أُضيف إلى العديد من تركيبات الرضع، تجنباً لنقص التورين. ومع ذلك، لم تخضع هذه الممارسة للدراسة بشكل دقيق، وعلى هذا النحو لم يثبت أنها ضرورية، أو حتى مفيدة.[23]
مشروبات الطاقة والمكملات الغذائية
يدخل التورين في مكونات بعض مشروبات الطاقة. تحتوي الكثير من مشروبات الطاقة على 1000 ملج من التورين[24] حتى 2000 ملج.[25]
كما يتواجد التورين في مختلف المكملات الغذائية التي يستخدمها الرياضيين.
الوظائف الفسيولوجية
الفسيولوجيا البشرية والتغذية
التورين ضروري لوظيفة القلب والأوعية الدموية وتطور ووظيفة العضلات الهيكلية وشبكية العين والجهاز العصبي المركزي.[26] وهو مركب طليعي تخليقي لأملاح الصوديوم الصفراوية taurochenodeoxycholate وsodium taurocholate. التورين ضروري لأداء عضلات الهيكل العظمي عملها بشكل طبيعي.[27]
على المستوى الخلوي، يعمل التورين كعنصر أسموليتي ينظم حجم الخلية. كما أنه يساعد على تعديل تركيزات الكالسيوم الحرة من الخلايا.[28]
يعمل التوراين كمضاد للأكسدة، ويقمع سمية الهيبوكلوريت والهيبوبروميت المنتج فسيولوجياً. يتفاعل التورين مع هذه العوامل المهلجنة لتشكيل ن-كلورو- و ن-بروموتورين، وهي أقل سمية من سلائفها من الهيبوهاليدات.[29]
للتورين تأثيرات متعددة على ابتناء الدهون وتقويضها، بما في ذلك تثبيط التعبير عن اختزال HMG-CoA، وقمع إفراز صميم البروتين B100، وتنظيم التعبير عن CYP7A1، وتنظيم التعبير عن مستقبلات البروتينات الدهنية منخفضة الكثافة.[30][31]
يعتبر التورين الحاجز الدموي الدماغي[32][33] وهو يساهم في مجموعة واسعة من الظواهر الفسيولوجية بما في ذلك النقل العصبي التثبيطي،[34] استقرار الغشاء[35] التثبيط الارتجاعي الانفجار التنفسي للخلايا العدلة/خلايا الدم البيضاء، تنظيم النسيج الدهني واستتباب الكالسيوم،[36] الشفاء من الصدمة التناضحية،[37] الحماية ضد حفيز الجلوتامات الزائد،[38] والوقاية من نوبات الصرع.[39]
يعمل التورين كمثبط للجلكنة. كان لدى الجرذان المصابة بالسكري المعالجة بالتورين انخفاض في تكوين المنتج النهائي للجلكنة المتقدم (AGEs) ومحتوى AGEs.[40][41] وجدت وزارة الزراعة الأمريكية ارتباطًا بين تطور إعتام عدسة العين وانخفاض مستويات فيتامين ب6 وحمض الفوليك والتورين في الأنظمة الغذائية لكبار السن.[42]
وجدت مراجعة منهجية عام 2022 أنه من خلال 5 دراسات ذات صلة، خفضت مكملات التورين مستويات HbA1c، ومستوى سكر الدم الصائم، وHOMA-IR. أوصت هذه المراجعة بتجارب إضافية لتوجيه الممارسة السريرية.[43]
هناك دليل على أن التورين قد يكون له تأثير مفيد في الوقاية من اعتلال الأوعية الدقيقة المرتبط بالسكري والإصابة الأنبوبية الخلالية في اعتلال الكلى السكري.[44][45]
مكافحة الشيخوخة وإطالة العمر
في 8 يونيو 2023، اقترحت دراسة جديدة أن نقص التورين قد يلعب دوراً هاماً في حدوث الشيخوخة. حققت الدراسة في تأثير هذا الحمض الأميني على الصحة وطول العمر عبر تجارب معملية على حيوانات مختلفة، وأشارت النتائج إلى أن استعادة فقدان التورين المرتبط بالعمر من خلال المكملات قد حسن العمر الصحي للديدان والقوارض والرئيسيات غير البشرية.[46]
سُمي حمض التورين بهذا الاسم لأنه تم التعرف عليه لأول مرة في بول الثيران- هو أحد أكثر الأحماض الأمينية وفرة الموجودة في البشر والحيوانات المعقدة الأخرى. كما هو الحال مع العديد من الأشياء، تنخفض تركيزات التورين في الدم مع تقدم العمر في الفئران والقرود والبشر، وفي البشر ترتبط المستويات المنخفضة من التورين بمخاطر أعلىلمرض السكري من النوع 2 وارتفاع ضغط الدم والبدانة والالتهابات وأمراض الكبد.[47]
لكن لم يتضح ما إذا كان التورين يؤثر على حدوث الشيخوخة. شرعت هذه الدراسة في التأكد مما إذا كانت وفرة التورين التي تنخفض مع تقدم العمر هي عامل نشط في العملية - أو عامل عابر خلال حدوث الشيخوخة على المدى الطويل.
أظهرت الأبحاث السابقة التي أجريت على أنواع مختلفة من الحيوانات أن نقص التورين في السنوات المبكرة من العمر يؤدي إلى ضعف وظيفي في العضلات والهيكل العظمي والعينين والجهاز العصبي، وجميعها مرتبطة بالاضطرابات المرتبطة بالشيخوخة. في حين أظهرت التجارب السريرية الصغيرة التي تبحث في مكملات التورين نتائج واعدة في الأمراض الأيضية والالتهابية، ظل تأثير تركيزات التورين على صحة الحيوان وطول العمر غير مفهوم بشكل جيد.
لفهم ما إذا كانت وفرة التورين تؤثر على الحياة الصحية بشكل أفضل، قام بارميندر سينج، زميل في مختبر كاباهي في معهد باك، وزملاؤه بقياس تركيزات التورين في الدم في الفئران والقرود والبشر بأعمار مختلفة.
اكتشف الباحثون أنه في القرود البالغة من العمر 15 عامًا، كانت تركيزات التورين في الدم أقل بنسبة 85% من تلك الموجودة في القرود البالغة من العمر 5 سنوات. وبالمثل، انخفضت مستويات التورين بأكثر من 80% على مدى عمر الإنسان. أظهرت الفئران المتقدمة في السن أيضًا انخفاض مستويات التورين، ولاحظ الباحثون أن الفئران التي تفتقر إلى الناقل الرئيسي للتورين كان لها عمر أقصر عند البالغين.
ومع ذلك، كان الانخفاض في مستويات التورين قابلاً للانعكاس من خلال مكملات التورين. في الواقع، زادت المكملات من متوسط عمر الديدان والفئران بنسبة 10-23% و10-12% على التوالي. والجدير بالذكر أن إعطاء الفئران التورين عن طريق الفم بجرعات 500 و1000 ملليجرام لكل كيلوجرام من وزن الجسم يوميًا كان مرتبطًا بتحسين في القوة والتنسيق والوظائف الإدراكية. علاوة على ذلك، فقد أبطأ العديد من السمات المميزة للشيخوخة: فقد قلل من الشيخوخة الخلوية، وحمايته من نقص التيلوميراز، والتغلب على الخلل الوظيفي في الميتوكوندريا، وقلل من تلف الحمض النووي والالتهاب.
أظهرت الفئران في منتصف العمر التي تم تغذيتها بالتورين تحسنًا في أداء العظام والعضلات والبنكرياس والمخ والدهون والأمعاء والجهاز المناعي، ولوحظ أيضًا تأثيرات على طول العمر في القرود وقرود المكاك الريسوسي في منتصف العمر، حيث أثرت مكملات التورين أيضًا بشكل إيجابي على العظام، الصحة الأيضية والمناعية.
تسلط هذه النتائج المقنعة الضوء على إمكانات مكملات التورين كإستراتيجية مضادة للشيخوخة، وهناك ما يبرر إجراء مزيد من البحث. من أجل تحديد ما إذا كانت مكملات التورين تزيد من العمر الافتراضي للأشخاص، ستكون هناك حاجة لإجراء تجارب سريرية على البشر؛ تحتاج أيضًا إلى تحديد المخاطر المحتملة المرتبطة بمكملات التورين، خاصة وأن الجرعات المستخدمة في دراسة سينج وآخرون كانت مرتفعة نسبيًا، مما يؤكد الحاجة إلى توخي الحذر عند اعتبار التورين مكملًا لطولالعمر.
أثناء دعوتهم لإجراء تجارب إكلينيكية على التورين، حذر المؤلفون الرئيسيون للدراسة العامة من عدم تناول المكملات دون إشراف طبي- بما في ذلك عدم المبالغة في تناول مشروبات الطاقة - مشيرين إلى أن هناك طرقًا أخرى لتعزيز المستقلب الطبيعي. وأظهرت الدراسة أن ممارسة التمارين الرياضية لفترة زمنية أدت إلى زيادة تركيز مستقلبات التورين في الدم والتي قد تفسر جزئياً التأثيرات المضادة للشيخوخة الناتجة عن التمارين الرياضية. يمكن أيضًا الحصول على التورين من خلال النظام الغذائي؛ يمكن الحصول على أعلى كميات من التورين من المحا ، وخاصة الأسقلوب وبلح البحر والمحار، كما يمكن العثور على كميات كبيرة من التورين في لحم الديك الرومي والدجاج.
أجريت الكثير من التجارب على الديدان الخيطية في معهد باك. يصف الأستاذ جوردون ليثجو، وهو من بين 56 باحثًا ساهموا في الدراسة، النتائج بأنها مذهلة: "كيف يمكننا أن نرى تأثيرات التورين المضادة للشيخوخة في الديدان، ثم في الفئران ثم الرئيسيات من الجنسين. هذه رسالة قوية حول تأثيرات المستقلبات التي تحدث بشكل طبيعي وما يمكن أن يحدث عندما يتم استعادتها إلى مستويات الشباب. هذه النتائج تمنحني الأمل في أن التدخلات البسيطة والآمنة يمكن أن يكون لها تأثير كبير على الشيخوخة".
بحسب جولي أندرسن، الأستاذة في معهد باك، وهي مؤلفة مشاركة أخرى تعتبر هذه الورقة البحثية انتصارًا كبيرًا لمجال علم الشيخوخة متعدد التخصصات. "على سبيل المثال، تم تضمين صحة العظام في هذه البحث. بالنسبة للجزء الأكبر، لا يتحدث الأشخاص المهتمون بصحة العظام إلى الأشخاص الذين يدرسون جوانب أخرى من الشيخوخة. هذه الدراسة تكسر الجدران بين الخميرة والديدان والفئران والرئيسيات، كما تقول أندرسن: "إنه مثال رائع لكيفية تحقيق اختراقات من خلال كونك متعدد التخصصات".
قاد عالم الأبحاث د. مانيش شامولي، الكثير من أعمال على الديدان والخلايا العصبية المذكورة في الورقة البحثية، وأصبح المؤلف الثاني للدراسة. يقول شامولي: "يبدو أن التورين قد يعمل، جزئيًا، من خلال زيادة نشاط مركب الميتوكوندريا 1، وليس مفاجأة عند النظر في العديد من السمات المميزة للشيخوخة التي تنطوي على خلل في الميتوكوندريا".
سيجري شامولي مزيدًا من الأبحاث حول الديدان لتحديد آليات عمل التورين المحددة. ويضيف شامولي: "هذه الورقة قوية جدًا لأنه قد أعيد إنتاج النتائج ذاتها في العديد من المعامل؛ كان هناك 34 منظمة بحثية مسجلة في الورقة، وأضاف: "مدرجًا فريقًا يضم علماء من جامعة كولومبيا بمدينة نيويورك، وجامعة واشنطن في سياتل وجامعة هارفارد في بوسطن ومعهد ماساتشوستس للتكنولوجيا في الولايات المتحدة، إلى جانب منظمات في نيودلهي، الهند وأستراليا وألمانيا وإيطاليا وفرنسا والمملكة المتحدة وسنغافورة وتركيا.
الفسيولوجيا الحيوانية والتغذية
بحسب الدراسات التي أُجريت على الجرذان، ينتج التورين تأثيرًا مضاداً للقلق وقد يعمل كمُعدِّل أو عامل مضاد للقلق في الجهاز العصبي المركزي عن طريق تنشيط مستقبلات الجلايسين.[48][49][50]
في الجرذان المصابة بالسكري، قللت مكملات التورين بشكل طفيف من دهون الجسم في البطن مع تحسن تحمل الجلوكوز.[51] يعتبر التورين فعالاً في إزالة رواسب الكبد الدهنية في الجرذان والوقاية من أمراض الكبد وتقليل تليف الكبد في الحيوانات المختبرة.[52][53] وبالمثل، فإن إعطاء التورين للأرانب المصابة بالسكري أدى إلى انخفاض بنسبة 30% بمستويات الجلوكوز في الدم.[54]
الجرذان المصابة بنقص التورين الوراثي لديها استنفاد شبه كامل لمستويات تورين الهيكل العظمي والعضلات القلبية وانخفاض بنسبة تزيد عن 80% من القدرة على ممارسة الرياضة مقارنة بالفئران الطبيعية. يمكن أن يؤثر التورين على تدفق الدم في الأعصاب، وسرعة التوصيل العصبي الحركي، والعتبات الحسية للأعصاب في الجرذان المصابة باعتلال الأعصاب السكري.[55][56]
تفتقد القطط إلى الآلية الإنزيمية (sulfinoalanine decarboxylase) لإنتاج التورين وبالتالي يجب أن تحصل عليه من نظامها الغذائي.[57]
يمكن أن يؤدي نقص التورين في القطط إلى تنكس الشبكية وفي النهاية العمى - حالة تعرف باسم تنكس الشبكية المركزي (CRD)،[58][59] وكذلك تساقط الشعر وتسوس الأسنان. الآثار الأخرى لنظام غذائي يفتقر إلى هذا الحمض الأميني الأساسي هي تمدد عضلة القلب والفشل الإنجابي عند الإناث.[60] ثبت أن انخفاض تركيز التوراين في البلازما مرتبط باعتلال عضلة القلب التوسعي لدى القطط.[61] على عكس تنكس الشبكية المركزي، يمكن عكس الحالة بالمكملات. يعتبر التورين الآن أحد متطلبات رابطة مسؤولي مراقبة الأعلاف الأمريكية (AAFCO) وأي منتج غذائي جاف أو رطب مُصدق عليه من قبل الرابطة يجب أن يحتوي على 0.1٪ تورن كحد أدنى في الأغذية الجافة و0.2% في الأغذية الرطبة.[62]
تشير الدراسات إلى ضرورة توفير الأحماض الأمينية بمعدل 10 ملجم/كجم من وزن الجسم/يوماً للقطط المنزلية.[63]
يبدو أن التورين ضروري لنمو العصفوريات. يبحث العديد من تلك الطيور عن العناكب الغنية بالتورين لإطعام صغارها، خاصة بعد الفقس مباشرة. قارن الباحثون سلوكيات وتطور الطيور التي تتغذى على نظام غذائي مكمل بالتورين مع نظام غذائي مقيد ووجدوا أن الصغار الذين يتغذون على نظام غذائي غني بالتورين حيث كان الولدان أكثر عرضة للمخاطر وأكثر مهارة في مهام التعلم المكاني.[64]
استخدم التورين في خلطات الحفظ بالتبريد للتلقيح الصناعي الحيواني.[65]
في دراسة لتحليل مستخلصات أنسجة العين لدى الجرذان، وجد أن التورين كان أكثر الأحماض الأمينية وفرة في شبكية العين، والجسم الزجاجي، والعدسة، والقرنية، والقزحية، والجسم الهدبي. داخل شبكية العين، يعتبر التورين ضروريًا لتطوير المستقبلات الضوئية.[28]
تشير دراسة نُشرت عام 2023 إلى أن تركيز التورين في الدم ينخفض أثناء الشيخوخة، كما تم قياسه في الجرذان والقرود والبشر. الجرذان والديدان التي تم تغذيتها عن طريق الفم بنظام ثابت من مكملات التورين عاشت لفترة أطول من الكائنات الضابطة، مع زيادة متوسط العمر بنسبة 10 إلى 12%.[66][67][68]
السلامة والسمية
أثبلغ عن زيادة كبيرة في تركيز هرمون النمو البلازما لدى بعض مرضى الصرع أثناء اختبار تحمل التورين (الجرعة الفموية 50 مليجرام لكل كيلوجرام من كتلة الجسم يوميًا)، مما يشير إلى إمكانية تحفيز الوطاء وتعديل وظيفة الغدد الصماء العصبية.[69]
وجدت دراسة أجريت عام 1966 أن مؤشر لأن التورين (2 جرام/يومياً) يتمتع ببعض الوظائف في استمرار الصدفية واحتمالية تحفيزها.[20] فشلت ثلاث دراسات لاحقة في تدعيم هذه النتيجة.[70][71][72]قد يكون من الضروري أيضًا مراعاة أن امتصاص التورين من المشروبات قد يكون أسرع من امتصاصه من الأطعمة.[20]
يتمتع التورين بمستوى آمن ملحوظ من المدخول التكميلي لدى البالغين الأصحاء العاديين بمعدل يصل إلى 3 ملاعق كبيرة/يومياً.[73]
ومع ذلك ، وجدت دراسة أجرتها هيئة سلامة الأغذية الأوروبية عدم وجود آثار ضارة لما يصل إلى 1000 ملجم من التورين لكل كيلوجرام من وزن الجسم يوميًا.[74]
وجدت مراجعة نُشرت عام 2008 عدم وجود تقارير موثقة عن آثار صحية سلبية أو إيجابية مرتبطة بكمية التورين المستخدمة في مشروبات الطاقة، وخلصت إلى أن "كميات الجوارانا والتورين والجنسنج الموجودة في مشروبات الطاقة الشعبية أقل بكثير من الكميات التي يُتوقع أن تقدم فوائد علاجية أو آثار سلبية".[75]
استخدامات أخرى
في مستحضرات التجميل ومحاليل العدسات اللاصقة
منذ عام 2000، طُرحت مستحضرات التجميل التي تحتوي على التورين، ربما بسبب خصائصه المضادة التليف. لقد ثبت أنه يمنع آثار TGFB1 الضارة لبصيلات الشعر.[76] كما أنه يساعد في الحفاظ على ترطيب البشرة.[77]
يستخدم التورين ايضاً في بعض محاليل العدسات اللاصقة.[78]
المشتقات
يستخدم التورين لتحضير أدوية النتوبيمين الطاردة للديدان (التوتابين).
- التوروليدين
- حمض التوروكوليك وحمض التوروسلكوليك
- 5-التوروموستين تورين مثيل أوريدين و5-تورين مثيل-2-ثيوريدين كيوريدينات معدلة في tRNA المتقدرة (البشرية).[79]
- التوريل هي المجموعة الوظيفية المرتبطة بالكبريت، 2-أمينو إثيل سلفونيل.[80]
- التورينو هي المجموعة الوظيفية المرتبطة بالنيتروجين، 2-سلفو إثيل أمينو.
انظر أيضاً
- هوموتورين (التراميبروسات)، مركب طليعي للأكامبروسيت.
- التوريتات، مجموعة مواد كيميائية.
مرئيات
| نقص حمض التورين قد يكون سبباً في الشيخوخة وقصر العمر، يونيو 2023. |
المصادر
- ^ Schuller-Levis GB, Park E (September 2003). "Taurine: new implications for an old amino acid". FEMS Microbiology Letters. 226 (2): 195–202. doi:10.1016/S0378-1097(03)00611-6. PMID 14553911.
- ^ Tiedemann F, Gmelin L (1827). "Einige neue Bestandtheile der Galle des Ochsen". Annalen der Physik. 85 (2): 326–337. Bibcode:1827AnP....85..326T. doi:10.1002/andp.18270850214.
- ^ Ronalds BF (2019). "Bringing Together Academic and Industrial Chemistry: Edmund Ronalds' Contribution". Substantia. 3 (1): 139–152.
- ^ Kataoka, Hiroyuki; Ohnishi, Naomi (1986). "Occurrence of Taurine in Plants". Agricultural and Biological Chemistry. 50 (7): 1887–1888. doi:10.1271/bbb1961.50.1887.
- ^ McCusker, Sarah; Buff, Preston R.; Yu, Zengshou; Fascetti, Andrea J. (2014). "Amino acid content of selected plant, algae and insect species: a search for alternative protein sources for use in pet foods". Journal of Nutritional Science (in الإنجليزية). 3: e39. doi:10.1017/jns.2014.33. ISSN 2048-6790. PMC 4473169. PMID 26101608.
- ^ Görbitz CH, Prydz K, Ugland S (2000). "Taurine". Acta Crystallographica Section C. 56: e23–e24. doi:10.1107/S0108270199016029.
- ^ Irving CS, Hammer BE, Danyluk SS, Klein PD (October 1980). "13C nuclear magnetic resonance study of the complexation of calcium by taurine". Journal of Inorganic Biochemistry. 13 (2): 137–150. doi:10.1016/S0162-0134(00)80117-8. PMID 7431022.
- ^ Kosswig K (2000). "Sulfonic Acids, Aliphatic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a25_503.
{{cite encyclopedia}}: Cite has empty unknown parameter:|authors=(help) - ^ Tully PS, ed. (2000). "Sulfonic Acids". Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. doi:10.1002/0471238961.1921120620211212.a01. ISBN 978-0471238966.
- ^ Amanda Xia (2010-01-03). "China Taurine Market Is Expected To Recover". Press release and article directory: technology. Archived from the original on 2018-09-20. Retrieved 2010-05-24.
- ^ Marvel CS, Bailey CF, Cortese F (1938). "Taurine". Org. Synth. 18: 77. doi:10.15227/orgsyn.018.0077.
- ^ Sumizu K (September 1962). "Oxidation of hypotaurine in rat liver". Biochimica et Biophysica Acta. 63: 210–212. doi:10.1016/0006-3002(62)90357-8. PMID 13979247.
- ^ Ripps H, Shen W (2012). "Review: taurine: a "very essential" amino acid". Molecular Vision. 18: 2673–2686. PMC 3501277. PMID 23170060.
- ^ McCusker, Sarah; Buff, Preston R.; Yu, Zengshou; Fascetti, Andrea J. (2014). "Amino acid content of selected plant, algae and insect species: a search for alternative protein sources for use in pet foods". Journal of Nutritional Science (in الإنجليزية). 3: e39. doi:10.1017/jns.2014.33. ISSN 2048-6790. PMC 4473169. PMID 26101608.
- ^ Machlin, L.J.; Pearson, P.B.; Denton, C.A. (1955). "The Utilization of Sulfate Sulfur for the Synthesis of Taurine in the Developing Chick Embryo". Journal of Biological Chemistry. 212 (1): 469–475. doi:10.1016/s0021-9258(18)71134-4. ISSN 0021-9258. PMID 13233249.
- ^ Sass, N. L.; Martin, W. G. (1972-03-01). "The Synthesis of Taurine from Sulfate III. Further Evidence for the Enzymatic Pathway in Chick Liver". Experimental Biology and Medicine (in الإنجليزية). 139 (3): 755–761. doi:10.3181/00379727-139-36232. ISSN 1535-3702. PMID 5023763. S2CID 77903.
- ^ Bouckenooghe T, Remacle C, Reusens B (November 2006). "Is taurine a functional nutrient?". Current Opinion in Clinical Nutrition and Metabolic Care. 9 (6): 728–733. doi:10.1097/01.mco.0000247469.26414.55. PMID 17053427. S2CID 24064647.
- ^ Brosnan JT, Brosnan ME (June 2006). "The sulfur-containing amino acids: an overview". The Journal of Nutrition. 136 (6 Suppl): 1636S–1640S. doi:10.1093/jn/136.6.1636S. PMID 16702333.
- ^ Huxtable RJ (January 1992). "Physiological actions of taurine". Physiological Reviews. 72 (1): 101–163. doi:10.1152/physrev.1992.72.1.101. PMID 1731369. S2CID 27844955.
- ^ أ ب ت "Opinion on Caffeine, Taurine and D-Glucurono – g -Lactone as constituents of so-called 'energy' drinks". Directorate-General Health and Consumers, European Commission, European Union. 1999-01-21. Archived from the original on 2006-06-23.
- ^ Jacobson SG, Kemp CM, Borruat FX, Chaitin MH, Faulkner DJ (October 1987). "Rhodopsin topography and rod-mediated function in cats with the retinal degeneration of taurine deficiency". Experimental Eye Research. 45 (4): 481–490. doi:10.1016/S0014-4835(87)80059-3. PMID 3428381.
- ^ Laidlaw SA, Shultz TD, Cecchino JT, Kopple JD (April 1988). "Plasma and urine taurine levels in vegans". The American Journal of Clinical Nutrition. 47 (4): 660–663. doi:10.1093/ajcn/47.4.660. PMID 3354491.
- ^ Heird WC (November 2004). "Taurine in neonatal nutrition – revisited". Archives of Disease in Childhood. Fetal and Neonatal Edition. 89 (6): F473–474. doi:10.1136/adc.2004.055095. PMC 1721777. PMID 15499132.
- ^ rockstar69.com Original Rockstar Ingredients
- ^ Chang, PL (2008-05-03). "Nos Energy Drink – Review". energyfanatics.com. Archived from the original on 2008-06-17. Retrieved 2010-05-21.
- ^ Huxtable RJ (January 1992). "Physiological actions of taurine". Physiological Reviews. 72 (1): 101–163. doi:10.1152/physrev.1992.72.1.101. PMID 1731369. S2CID 27844955.
- ^ Warskulat U, Flögel U, Jacoby C, Hartwig HG, Thewissen M, Merx MW, et al. (March 2004). "Taurine transporter knockout depletes muscle taurine levels and results in severe skeletal muscle impairment but leaves cardiac function uncompromised" (PDF). FASEB Journal. 18 (3): 577–579. doi:10.1096/fj.03-0496fje. PMID 14734644. S2CID 19037998. Archived from the original (PDF) on 2019-02-21.
- ^ أ ب Ripps, H; Shen, W (2012). "Review: taurine: a "very essential" amino acid". Molecular Vision. 18: 2673–86. PMC 3501277. PMID 23170060.
- ^ Marcinkiewicz J, Kontny E (January 2014). "Taurine and inflammatory diseases". Amino Acids. 46 (1): 7–20. doi:10.1007/s00726-012-1361-4. PMC 3894431. PMID 22810731.
- ^ Dong, Yuanyuan; Li, Xiaoling; Liu, Yaling; Gao, Jie; Tao, Jinhui (August 2021). "The molecular targets of taurine confer anti-hyperlipidemic effects". Life Sciences. 278: 119579. doi:10.1016/j.lfs.2021.119579. PMID 33961852. S2CID 233998543.
- ^ Yanagita T, Han SY, Hu Y, Nagao K, Kitajima H, Murakami S (October 2008). "Taurine reduces the secretion of apolipoprotein B100 and lipids in HepG2 cells". Lipids in Health and Disease. 7: 38. doi:10.1186/1476-511x-7-38. PMC 2579289. PMID 18925970.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Urquhart N, Perry TL, Hansen S, Kennedy J (May 1974). "Passage of taurine into adult mammalian brain". Journal of Neurochemistry. 22 (5): 871–872. doi:10.1111/j.1471-4159.1974.tb04309.x. PMID 4407108. S2CID 32864924.
- ^ Tsuji A, Tamai I (1996). "Sodium- and chloride-dependent transport of taurine at the blood-brain barrier". Taurine 2. Advances in Experimental Medicine and Biology. Vol. 403. pp. 385–391. doi:10.1007/978-1-4899-0182-8_41. ISBN 978-1-4899-0184-2. PMID 8915375.
- ^ Olive MF (2002). "Interactions between taurine and ethanol in the central nervous system". Amino Acids. 23 (4): 345–357. doi:10.1007/s00726-002-0203-1. PMID 12436202. S2CID 5406826.
- ^ Schaffer SW, Jong CJ, Ramila KC, Azuma J (August 2010). "Physiological roles of taurine in heart and muscle". Journal of Biomedical Science. 17 Suppl 1 (Suppl 1): S2. doi:10.1186/1423-0127-17-S1-S2. PMC 2994395. PMID 20804594.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Foos TM, Wu JY (February 2002). "The role of taurine in the central nervous system and the modulation of intracellular calcium homeostasis". Neurochemical Research. 27 (1–2): 21–26. doi:10.1023/A:1014890219513. PMID 11926272. S2CID 29948337.
- ^ Stummer W, Betz AL, Shakui P, Keep RF (September 1995). "Blood-brain barrier taurine transport during osmotic stress and in focal cerebral ischemia". Journal of Cerebral Blood Flow and Metabolism. 15 (5): 852–859. doi:10.1038/jcbfm.1995.106. PMID 7673378.
- ^ Leon R, Wu H, Jin Y, Wei J, Buddhala C, Prentice H, Wu JY (April 2009). "Protective function of taurine in glutamate-induced apoptosis in cultured neurons". Journal of Neuroscience Research. 87 (5): 1185–1194. doi:10.1002/jnr.21926. PMID 18951478. S2CID 24725862.
- ^ El Idrissi A, Messing J, Scalia J, Trenkner E (2003). "Prevention of epileptic seizures by taurine". Taurine 5. Advances in Experimental Medicine and Biology. Vol. 526. pp. 515–525. doi:10.1007/978-1-4615-0077-3_62. ISBN 978-1-4613-4913-6. PMID 12908638.
- ^ Effects of taurine on advanced glycosylation end products and expression of TGF-β in renal cortex of, TsingHua, 2005, http://www.shvoong.com/medicine-and-health/1599878-effects-taurine-advanced-glycosylation-end/ Archived 2016-08-13 at the Wayback Machine
- ^ Huang JS, Chuang LY, Guh JY, Yang YL, Hsu MS (December 2008). "Effect of taurine on advanced glycation end products-induced hypertrophy in renal tubular epithelial cells". Toxicology and Applied Pharmacology. 233 (2): 220–226. doi:10.1016/j.taap.2008.09.002. PMID 18834896.
- ^ "ARS: 50 Years of Research for the Growing World". Ars.usda.gov. Retrieved 2012-10-27.
- ^ Tao, Xiaomei; Zhang, Zhanzhi; Yang, Zhenpeng; Rao, Benqiang (July 2022). "The effects of taurine supplementation on diabetes mellitus in humans: A systematic review and meta-analysis". Food Chemistry: Molecular Sciences. 4: 100106. doi:10.1016/j.fochms.2022.100106. PMC 9235038. PMID 35769396.
- ^ Wu QD, Wang JH, Fennessy F, Redmond HP, Bouchier-Hayes D (December 1999). "Taurine prevents high-glucose-induced human vascular endothelial cell apoptosis". The American Journal of Physiology. 277 (6): C1229–1238. doi:10.1152/ajpcell.1999.277.6.C1229. PMID 10600775.
- ^ Verzola D, Bertolotto MB, Villaggio B, Ottonello L, Dallegri F, Frumento G, et al. (November 2002). "Taurine prevents apoptosis induced by high ambient glucose in human tubule renal cells". Journal of Investigative Medicine. 50 (6): 443–451. doi:10.1136/jim-50-06-04. PMID 12425431. S2CID 22191154.
- ^ "Taurine deficiency as a driver of aging". science.org. 2023-06-08. Retrieved 2023-06-17.
- ^ "Taurine deficiency: New research identifies possible driver for aging". longevity.technology. 2023-06-08. Retrieved 2023-06-17.
- ^ Kong WX, Chen SW, Li YL, Zhang YJ, Wang R, Min L, Mi X (February 2006). "Effects of taurine on rat behaviors in three anxiety models". Pharmacology, Biochemistry, and Behavior. 83 (2): 271–276. doi:10.1016/j.pbb.2006.02.007. PMID 16540157. S2CID 30644212.
- ^ Zhang CG, Kim SJ (2007). "Taurine induces anti-anxiety by activating strychnine-sensitive glycine receptor in vivo". Annals of Nutrition & Metabolism. 51 (4): 379–386. doi:10.1159/000107687. PMID 17728537. S2CID 10017887.
- ^ Chen SW, Kong WX, Zhang YJ, Li YL, Mi XJ, Mu XS (August 2004). "Possible anxiolytic effects of taurine in the mouse elevated plus-maze". Life Sciences. 75 (12): 1503–1511. doi:10.1016/j.lfs.2004.03.010. PMID 15240184.
- ^ Nakaya Y, Minami A, Harada N, Sakamoto S, Niwa Y, Ohnaka M (January 2000). "Taurine improves insulin sensitivity in the Otsuka Long-Evans Tokushima Fatty rat, a model of spontaneous type 2 diabetes". The American Journal of Clinical Nutrition. 71 (1): 54–58. doi:10.1093/ajcn/71.1.54. PMID 10617946.
- ^ Kerai MD, Waterfield CJ, Kenyon SH, Asker DS, Timbrell JA (1998). "Taurine: protective properties against ethanol-induced hepatic steatosis and lipid peroxidation during chronic ethanol consumption in rats". Amino Acids. 15 (1–2): 53–76. doi:10.1007/BF01345280. PMID 9871487. S2CID 20334658.
- ^ McCall B (2005-12-28). "The ultimate hangover cure?". bbc.co.uk. Retrieved 2008-09-01.
- ^ Winiarska K, Szymanski K, Gorniak P, Dudziak M, Bryla J (February 2009). "Hypoglycaemic, antioxidative and nephroprotective effects of taurine in alloxan diabetic rabbits". Biochimie. 91 (2): 261–270. doi:10.1016/j.biochi.2008.09.006. PMID 18957317.
- ^ Li F, Abatan OI, Kim H, Burnett D, Larkin D, Obrosova IG, Stevens MJ (June 2006). "Taurine reverses neurological and neurovascular deficits in Zucker diabetic fatty rats". Neurobiology of Disease. 22 (3): 669–676. doi:10.1016/j.nbd.2006.01.012. PMID 16624563. S2CID 22502432.
- ^ Pop-Busui R, Sullivan KA, Van Huysen C, Bayer L, Cao X, Towns R, Stevens MJ (April 2001). "Depletion of taurine in experimental diabetic neuropathy: implications for nerve metabolic, vascular, and functional deficits". Experimental Neurology. 168 (2): 259–272. doi:10.1006/exnr.2000.7591. PMID 11259114. S2CID 28261875.
- ^ Knopf K, Sturman JA, Armstrong M, Hayes KC (May 1978). "Taurine: an essential nutrient for the cat". The Journal of Nutrition. 108 (5): 773–778. doi:10.1093/jn/108.5.773. PMID 641594.
- ^ "Taurine And Its Importance In Cat Foods". Iams Cat Nutrition Library. 2004. Archived from the original on 2006-10-19. Retrieved 2006-08-22.
- ^ "Nutrient Requirements of Cats". Nutrient Requirements of Cats, Revised Edition, 1986. 1986. Archived from the original on 2006-09-01. Retrieved 2006-09-10.
- ^ Hayes KC, Carey RE, Schmidt SY (May 1975). "Retinal degeneration associated with taurine deficiency in the cat". Science. 188 (4191): 949–951. Bibcode:1975Sci...188..949H. doi:10.1126/science.1138364. PMID 1138364.
- ^ Pion PD, Kittleson MD, Rogers QR, Morris JG (August 1987). "Myocardial failure in cats associated with low plasma taurine: a reversible cardiomyopathy". Science. 237 (4816): 764–768. Bibcode:1987Sci...237..764P. doi:10.1126/science.3616607. PMID 3616607.
- ^ "AAFCO Cat Food Nutrient Profiles". Archived from the original on 2015-05-29. Retrieved 30 May 2015.
- ^ Burger IH, Barnett KC (1982). "The taurine requirement of the adult cat". Journal of Small Animal Practice. 23 (9): 533–537. doi:10.1111/j.1748-5827.1982.tb02514.x.
- ^ Arnold KE, Ramsay SL, Donaldson C, Adam A (October 2007). "Parental prey selection affects risk-taking behaviour and spatial learning in avian offspring". Proceedings. Biological Sciences. 274 (1625): 2563–2569. doi:10.1098/rspb.2007.0687. PMC 2275882. PMID 17698490.
- ^ Shiva Shankar Reddy N, Jagan Mohanarao G, Atreja SK (June 2010). "Effects of adding taurine and trehalose to a tris-based egg yolk extender on buffalo (Bubalus bubalis) sperm quality following cryopreservation". Animal Reproduction Science. 119 (3–4): 183–190. doi:10.1016/j.anireprosci.2010.01.012. PMID 20197223.
- ^ Singh, Parminder; et al. (June 9, 2023). "Taurine deficiency as a driver of aging". Science. 380 (6649). doi:10.1126/science.abn92.
- ^ "Taurine May Be a Key to Longer and Healthier Life". Columbia University Irving Medical Center. June 8, 2023. Retrieved 2023-06-09.
- ^ McGaunn, Joseph; Baur, Joseph A. (June 8, 2023). "Taurine linked with healthy aging". Science. 380 (6649): 1010–1011. doi:10.1126/science.adi302.
- ^ Mantovani J, DeVivo DC (November 1979). "Effects of taurine on seizures and growth hormone release in epileptic patients". Archives of Neurology. 36 (11): 672–674. doi:10.1001/archneur.1979.00500470042006. PMID 508122.
- ^ Zackheim HS, Farber EM (March 1968). "Taurine and psoriasis". The Journal of Investigative Dermatology. 50 (3): 227–230. doi:10.1038/jid.1968.32. PMID 5644896. Retrieved 2013-11-23.
- ^ Zackheim HS (1982). "Taurine and Diet in Psoriasis". Archives of Dermatology. 118 (12): 961. doi:10.1001/archderm.1982.01650240005005. PMID 7149750.
- ^ Zackheim HS, Farber EM (May 1969). "Low-protein diet and psoriasis. A hospital study". Archives of Dermatology. 99 (5): 580–586. doi:10.1001/archderm.1969.01610230072012. PMID 5780964.
- ^ Shao A, Hathcock JN (April 2008). "Risk assessment for the amino acids taurine, L-glutamine and L-arginine". Regulatory Toxicology and Pharmacology. 50 (3): 376–399. doi:10.1016/j.yrtph.2008.01.004. PMID 18325648.
the newer method described as the Observed Safe Level (OSL) or Highest Observed Intake (HOI) was utilized. The OSL risk assessments indicate that based on the available published human clinical trial data, the evidence for the absence of adverse effects is strong for Tau at supplemental intakes up to 3 g/d, Gln at intakes up to 14 g/d and Arg at intakes up to 20 g/d, and these levels are identified as the respective OSLs for normal healthy adults.
- ^ "EFSA adopts opinion on two ingredients commonly used in some energy drinks". 12 February 2009. efsa.europa.eu.
- ^ Clauson KA, Shields KM, McQueen CE, Persad N (2008). "Safety issues associated with commercially available energy drinks". Journal of the American Pharmacists Association. 48 (3): e55–63, quiz e64–67. doi:10.1331/JAPhA.2008.07055. PMID 18595815. S2CID 207262028.
- ^ Collin C, Gautier B, Gaillard O, Hallegot P, Chabane S, Bastien P, et al. (August 2006). "Protective effects of taurine on human hair follicle grown in vitro". International Journal of Cosmetic Science. 28 (4): 289–298. doi:10.1111/j.1467-2494.2006.00334.x. PMID 18489269. S2CID 32840479.
We showed that taurine [...] prevented TGF-β1-induced deleterious effects on hair follicle.
- ^ Janeke G, Siefken W, Carstensen S, Springmann G, Bleck O, Steinhart H, et al. (August 2003). "Role of taurine accumulation in keratinocyte hydration". The Journal of Investigative Dermatology. 121 (2): 354–361. doi:10.1046/j.1523-1747.2003.12366.x. PMID 12880428.
- ^ James TJ, Hansen D, Nolfi J (2004-04-01). "Ocular Health and Next Generation Solutions". Optometric Management. Archived from the original on 2005-04-19. Retrieved 2008-01-10.
- ^ Suzuki T, Suzuki T, Wada T, Saigo K, Watanabe K (December 2002). "Taurine as a constituent of mitochondrial tRNAs: new insights into the functions of taurine and human mitochondrial diseases". The EMBO Journal. 21 (23): 6581–6589. doi:10.1093/emboj/cdf656. PMC 136959. PMID 12456664.
- ^ Bünzli-Trepp U (2007). Systematic nomenclature of organic, organometallic and coordination chemistry. EPFL Press. p. 226. ISBN 9781420046151.
وصلات خارجية
- CS1 maint: unflagged free DOI
- Articles with changed EBI identifier
- Articles with changed DrugBank identifier
- ECHA InfoCard ID from Wikidata
- Articles containing unverified chemical infoboxes
- Short description is different from Wikidata
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- Articles containing لاتينية-language text
- Articles with hatnote templates targeting a nonexistent page
- Amines
- Sulfonic acids
- Glycine receptor agonists
- Inhibitory amino acids
