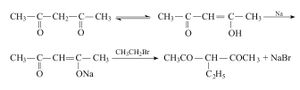
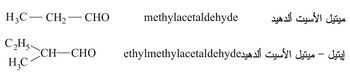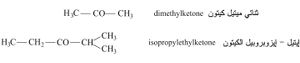مجموعة كربونيل
الكربونيل carbonyl، في الكيمياء العضوية عبارة عن مجموعة وظيفية (زمرة فعالة) تتألف من ذرة كربون مرتبط برابطة مضاعفة بذرة أكسجين : C=O.
يمكن أن يشير الكربونيل أيضاً إلى أحادي أكسيد الكربون كربيطة في المعقدات العضوية واللاعضوية، مثل كربونيل النيكل، ولكن يكون الكربون مرتبطاً برابطة ثلاثية مع الأكسجين في هذه الحالة : C≡O .
تدخل الزمرة الكربونيلية في بنية عدد كبير من الزمر الوظيفية، ولكثير من هذه الزمر أهمية كبيرة في المركبات الموجودة في الطبيعة، ومن المركبات التي تدخل فيها زمرةُ الكربونيل الألدهيدات والكيتونات. وينتسب إلى المشتقات الكربونيلية carbonyl derivatives الحموض الكربوكسيلية[ر] ومشتقاتها مثل كلوريدات الحموض الكربوكسيلية.
الألدهيدات والكيتونات (أو الخلونات أو السيتونات) مركبات عضوية تحوي مجموعة الكربونيل. فإذا أشبعَت زمرة الكربونيل أحدَ تكافؤيها الحرين بذرة هدروجين أعطت جذر الفورميل وهو الجذر الوظيفي المميز للألدهيدات. وإذا أشبَعَت بعد ذلك تكافؤها الثاني بجذر ألكيل أعطت الألدهيدات ذات الصيغة العامة ويشذ عن ذلك الفورم ألدهيد، أو ألدهيد النمل formaldehyde، الذي تحمل فيه مجموعة الكربونيل ذرتي هدروجين. أما إذا أشبعت مجموعة الكربونيل تكافؤيها الحرين بجذرين ألكيليين فإنها تعطي الكيتونات ذات الصيغة العامة ومن الملاحظ أن الزمرة الوظيفية -CHO في الألدهيدات تشغل دائماً نهاية السلسلة لاتصافها بتكافؤ حر وحيد. أما الزمرة الوظيفية فتشغل أماكن داخلية لاتصافها بتكافؤين حرين.
التسمية
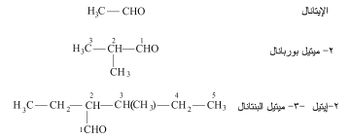
1 - تشتق تسمية الألدهيدات وفق IUPAC الاتحاد الدولي للكيمياء البحتة والتطبيقية International Union of Pure and Applied Chemistry بإضافة اللاحقة النوعية (آل al) إلى اسم الفحم الهدروجيني الرئيسي المشتقة منه. ويختار كفحم هدروجيني رئيسي الفحم الهدروجيني الموافق لأطول سلسلة تحوي الزمرة الوظيفية الألدهيدية. ويشار بأعداد إلى مواضع الفروع الجانبية أو المتبادلات حيث يوافق الـرقم1 الزمرة الوظيفية الألدهيدية. ويمكن حذف هذا الرقم إذا كانت هذه الزمرة هي الزمرة الوظيفية الوحيدة في المركب

2 - نمط التسمية الشائعة: يشار إلى الألدهيدات - والحدود الأولى منها خاصة - في هذا النمط من التسمية بالاسم الشائع للحمض الذي تعطيه عند أكسدتها بعد وَسْم هذا الاسم بكلمة ألدهيد:
ويشار على مواضع الفروع الجانبية أو المتبادلات بحروف يونانية على اعتبار الكربون −α هو الكربون المجاور للزمرة الألدهيدية
−β هدروكسي البوتير ألدهيد
![]()
3ـ تسمية الألدهيدات كمشتقة من أسيت ألدهيد: يمكن تسميتها بعدها مشتقة من الأسيت ألدهيد
أما الكيتونات فتشتق تسميتها حسب IUPAC إما بإضافة السابقة (أوكسو oxo) وإما بإضافة اللاحقة (ون -one) إلى اسم الفحم الهدروجيني. ويحدد موقع الزمرة C=O فيها بأصغر الأرقام الممكنة. وتختار كسلسلة رئيسية - كما هي الحال في الألدهيدات - أطول سلسلة تحوي الزمرة الكيتونية. وتسمى الكيتونات البسيطة أيضاً بذكر الجذور المرتبطة بالزمرة الكربونيلية متبوعة بكلمة كيتون وهي التسميات الموضوعة ضمن الأقواس.
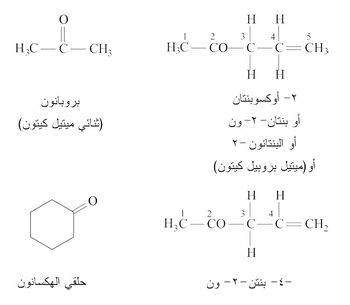
2ـ نمط التسمية الشائعة: تدعى الحدود الدنيا في هذا النمط من التسمية بإضافة كلمة كيتون بعد ذكر اسمي الجذرين الألكيليين المتحدين مع الزمرة الكيتونية
ويدعى الكيتون بسيطاً أو متناظراً إذا كانت زمرتا الألكيل متماثلتين في الكيتون. ويدعى مختلطاً أو غير متناظر إذا كانتا مختلفتين. وتدعى بعض الكيتونات بأسماء خاصة. فالكيتون CH3 −CO−CH3 يدعى بالاسم أسيتون acetone.
3 - تسمية الكيتونات كمشتقات من الأسيتون: تسمى السيتونات كذلك بوصفها مشتقة من الأسيتون
α, αَ- ثنائي ميتيل أسيتون H2C − CH2 − CO − CH2 − CH3
مركبات الكربونيل
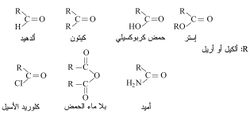
تميز مجموعة الكربونيل الفئة التالية من المركبات:
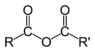
| المركب | ألدهيد | كيتون | حمض كربوكسيلي | إستر | أميد | إينون | هاليد الأسيل | بلا ماء الحمض |
| البنية | 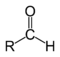 |
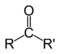 |
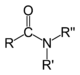 |
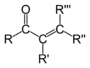 |
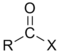 |
| ||
| الصيغة العامة | RCHO | RCOR' | RCOOH | RCOOR' | RCONR'R'' | RC(O)C(R')CR''R''' | RCOX | (RCO)2O |
مشتقات ثنائي الكربونيل
مشتقات ثنائي الكربونيل dicarbonyl derivatives كما يدل عليها اسمها هي مركبات عضوية تحوي زمرتي كربونيل C=O، وتشمل ثنائيات الألدهيد وثنائيات الكيتون والألدهيدات الكيتونية والحموض الكيتونية والحموض الألدهيدية، وتتعين الخواص الكيمياوية لهذه المركبات، مثلها في ذلك مثل المشتقات ثنائيات الزمر الوظيفية بالمواضع النسبية لهذه الزمر بعضها بالنسبة إلى بعضها الآخر.[1]
وقد صنفت بناء على ذلك إلى :
O - 2,1OO (أو -α) ثنائيات الكربونيل RCOCOR
O - 3,1OO (أو -β) ثنائيات الكربونيل RCOCH2COR
O - 4,1OO (أو -γ) ثنائيات الكربونيل RCOCH2CH2COR
c2,1C- (أو -α) ثنائيات الكربونيل N1,2-dicarbonyl (α-)
اصطناعها
- بالحلمهة ( التحلل بالماء) الحمضية لـ -α أوكسي ايمينو الكيتونات (أحادي أوكسيم O-2,1O ثنائي الكيتون ) الناتج من تفاعل حمض الآزوتيت HNO2 مع الكيتون الحاوي زمرة متيل أو متيلين في الموضع α- بالنسبة إلى الزمرة الكربونيلية.
- بأكسدة الأسيلوئينات والبنزوئينات إلى ثنائيات الكربونيل.
خواصها الكيمياوية
تقوم هذه المركبات بالتفاعلات العادية المميزة للألدهيدات والكيتونات. وهي تكوِّن ضروب أحادي أوكسيم وضروب ثنائي أوكسيم.
ولثنائيات الكيتون O-2,1 Oبعض التفاعلات المميزة:
1- تفاعل كانيزارو Cannizzaro reaction ضمن الجزيء الذي يتم بوجود قلوي قوي إذ تتأكسد إحدى زمرتي الألدهيد على حساب الأخرى.
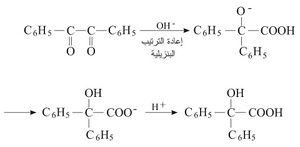
2- إعادة الترتيب البنزيلية Benzilic acid rearrangement
تتفاعل ثنائيات الكيتون عند معالجتها بضروب هدروكسيد المعادن القلوية معطية ملح الحمض الهدروكسيلي. فعلى سبيل المثال عند معالجة البنزيل بهدروكسيد الصوديوم يخضع لإعادة الترتيب البنزيلية وينتج ملح بنزيلات الصوديوم التي تعطي عند تعديلها بحمض لاعضوي حمض البنزيليك:
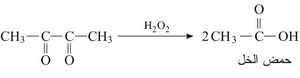
3- الأكسدة التفكيكية: تتحطم الرابطة C-C بين زمرتين كربونيليتين بسهولة بفعل المؤكسدات، فعند فعل الماء الأكسجيني في ثنائي الأسيتيل يتكون جزيئان من حمض الخل.
4- تفاعلات مميزة للبوتان ديون O-3,2 O واسمه الشائع: (ثنائي الاسيتيل)
أ- يشكل مع أيونات النيكل (Ni) معقداً أحمر ينحل بصعوبة في الماء ويستعمل في التحليل الكيفي والكمي للنيكل إذ يتكون معقد صيغتة:
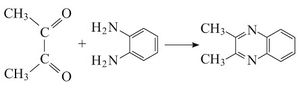
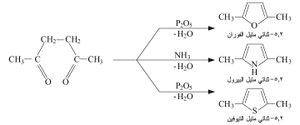
ب- هذه المركبات (ثنائي الأسيتيل واحد منها) مع المركبات الحاوية زمرتي NH2 معطية حلقات غير متجانسة heterocyclic compounds. وهذا التفاعل يفيد في تمييز كل من −α ثنائيات الكيتون والمركبات ثنائية الأمين: مثال ذلك تفاعل ثنائي الأسيتيل مع أورتو- ثنائي أمينوالبنزن:
وكذلك تفاعل ثنائي الأسيتيل مع البولة (اليوريا) الذي يعطي: 5.4 - ثنائي متيل الإميدازوليدون -2.
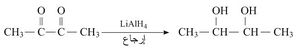
ج - يعطي إرجاع (اختزال) البوتان ديون O-3,2O بهدريد الليثيوم والألمنيوم الديول الموافق:
O-3,1O (أو -β) ثنائيات الكربونيل 3,1 - dicarbonyl (-β)
أهمها مالون ثنائي الألدهيد (بروبان دي آل) وفورميل أسيتون (3- اوكسو بوتانال) وأسيتيل أسيتون (بنتان ديون-4.2 ).
اصطناعها=
- تكاثف كلايزن Claisen condensation بين خلات الإتيل والأسيتون بوجود أسس قوية:
- تفاعل بلا ماء حمض الخل مع الأسيتون بوجود ثلاثي فلوريد البور BF3 حفّازاً (وسيطاً):
الخواص الكيمياوية
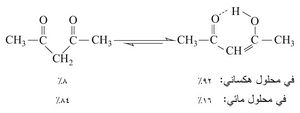
1- يحتوي أسيتيل الأسيتون على هدروجين زلوق - CH2- ولذلك فهو يتفاعل كالمركبات الحامضية، وهو موجود في شكلين أينولي وكيتوني.
ويتوقف التوازن على درجة الحرارة والمحل.
تعزى النسبة العالية من الشكل الإينولي إلى قدرة أسيتيل الأسيتون على تكوين رابطة هدروجينية ضمن جزيئّية يساعد على تشكلها إمكانية تكون حلقة سداسية.
2- تشكل O-3,1O ثنائيات الكربونيل معقدات مخلبية chelation مستقرة حلولـــة في المحلات العضويــة مثل ثنائي إتيل الإيتر والبنزن والكلوروفورم، مثال ذلك أسيتيل أسيتونات النحاس (II) الزرقاء اللون والقليلة الانحلال في الماء.
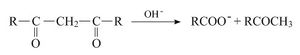
3- تتفكك عند تسخينها مع القلويات القوية معطية الكيتون والحمض.
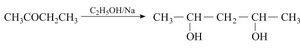
4- ترجَع بالهدروجين المنطلق من تفاعل الإيتانول مع الصوديوم المعدني:
5- تتفاعل مباشرة مع الصوديوم المعدني مشكلة إينولات تتفاعل بدورها مع هاليدات الألكيل معطية مشتقاتها الألكيلية:
6 - يتفاعل أسيتيل الأسيتون بصيغتة الإينولية فقط مع الأغوال في وسط حمضي معطياً إيترات الإينول.
7 - يسمح فعل البروم في الشكل الإينولي enol form فقط بمعايرة الإينول في ثنائي الكيتون (تفاعل ماير).
8 - يتفاعل N-3,1 ثنائي الكربونيل مع الهدرازين N2H4 معطياً مركباً حلقياً غير متجانس هو O-5,3O متيل بيرازول.
-4,1 (أو -γ) ثنائيات الكربونيل 1,4-dicarbonyls (-γ)
يُعد أسيتونيل الأسيتون CH3COCH2CH2COCH3 الفرد الأول في هذه المجموعة. وهو يحضر بمعالجة أسيتو أسيتات الإتيل بأحادي بروم الأسيتون في وسط قلوي متبوعاً بحلمهة ثم نزع كربوكسيل:
الخواص الكيميائية
لا تنحل ثنائيات الكربونيل O-4,1O في القلويات، إلا أنها تشكل بسهولة مركبات حلقية غير متجانسة مع خماسي أكسيد الفسفور أو النشادر أو خماسي كبريتيد الفسفور.
تجدر الإشارة إلى أنه لم يتيسر تحضير O-5,1O و O-7,1O ثنائيات الكربونيل، إذ أدت المحاولات جميعها إلى تشكيل مركبات مغلقة. أما O-6,1O و O-8,1O ثنائيات الكربونيل فهي مركبات معروفة.
طرق التحضير
يتم الحصول على الألدهيدات والكيتونات بأحد التفاعلات الآتية: الأكسدة، الإرجاع، الحلمهة، التفكك الحراري النازع لغاز الكربون، الإماهة، تفاعل أوكسو أو الكربلة (إدخال جذر الكربونيل).
1ـ تؤدي أكسدة الكحولات alcohols باستخدام ثنائي كرومات البوتاسيوم في وسط حمضي إذ تتأكسد الكحولات الأولية إلى ألدهيدات، والأغوال الثانوية إلى كيتونات لها العدد نفسه من ذرات الكربون.
2 - نزع الهدروجين من الكحولات، وذلك بإمرار أبخرة الكحولات الأولية أو الثانوية على مسحوق النحاس المسخن حتى الدرجة 250 ْ - 400 ْ س، إذ ينفصل منها الهدروجين وتتكون الألدهيدات أو الكيتونات. ومن محاذير الطريقة السابقة أن الأكسدة تستمر في جزء من المركب الكربونيلي الناتج.
3 - حلمهة hydrolysis المشتقات ثنائية الهالوجين التوءمية gem أو geminal وذلك باستعمال محاليل القلويات المائية. تحتوي هذه المركبات على ذرتي هالوجين مرتبطتين إما بذرة كربون أولية وإما ثانوية. تعطي الحلمهة في الحالة الأولى الألدهيدات وفي الثانية الكيتونات.
وليس لهذا التفاعل أهمية في التحضير؛ لأن المشتقات ثنائية الهالوجين التوءمية تحضر بدءاً من هذه المركبات الكربونيلية.
كما تستحصل الألدهيدات والكيتونات بمعالجة الألكنات alkenes بالأوزون O3، وتختلف النواتج حسب تركيب الألكِن المستخدم، فإذا احتوى الألكِن على سلسلة مستقيمة مثل الإيتيلين تكوّن الألدهيد، أما إذا كانت السلسلة متفرعة مثل إيزو البوتيلين كان الناتج كيتوناً. أو بإماهة الأستيلينات alkynes بوجود حفّاز، فالأستيلين يتفاعل مع الماء بوجود حفّاز من حمض الكبريت الحاوي كبريتات الزئبق مكوناً الأسيت ألدهيد. أما أقران الأستيلين فتعطي جميعها كيتونات عند معالجتها بالطريقة نفسها.
وهناك طرائق خاصة عديدة لاستحضار الألدهيدات وطرائق خاصة لاستحضار الكيتونات مثال ذلك إرجاع كلوريدات الحموض بهدرجة كلوريد الحمض بوجود هدروكسيد البلاديوم Pd(OH)2 المرسب على كبريتات الباريوم ويتوقف الإرجاع عند مرحلة الألدهيد. وتقوم الكبريتات هنا بمنع الإرجاع اللاحق للألدهيد.
ويحضَّر الأسيتون نفسه بالتقطير الجاف لأستيات الكلسيوم:
الخواص الفيزيائية
توجد بعض الألدهيدات والكيتونات في الطبيعة، في بعض العطور، مثل النونانال C8H17 − CHO الموجود في زيت نبات العرنوقي (الجيرانيوم).
يسهم في زمرة الكربونيل في الألدهيدات والكيتونات شكلان أساسيان للطنين (التجاوب) هما:
وقد تبين من الدراسات التي أجريت على عزوم ثنائي القطب أن الشكل الأيوني أقل أهمية بقليل من الشكل المشترك.
ولما كانت الرابطة المضاعفة تتألف من رابطة σ وأخرى π ولما كانت ذرة الأكسجين أكثر كهرسلبية من ذرة الكربون، فإنها تشوه السحابة الإلكترونية π لتجعل الكثافة الإلكترونية حول ذرة الأكسجين أشد وأكبر.
إن قطبية زمرة الكربونيل تجعل الألدهيدات والكيتونات مركبات قطبية ولكنها غير قادرة على تشكيل روابط هدروجينية بين جزيئاتها بعكس الكحولات والحموض الكربوكسيلية الموافقة. وهكذا فإن للألدهيدات درجات غليان (الجدول-1) أخفض من درجات غليان الكحولات الموافقة، فأسيت ألدهيد على سبيل المثال يغلي عند الدرجة 20.6 ْس في حين يغلي الكحول الإتيلي عند الدرجة 78.5 ْ س.
أبسط أفراد الألدهيدات الفورم ألدهيد هو غاز في الدرجة العادية من الحرارة يدعى محلوله المائي الحاوي 40% منه الفورمالين.
تذوب الألدهيدات الدنيا في الماء بجميع النسب ويقل ذوبانها بازدياد أوزانها الجزيئية، ولكن تذوب جميعها في الكحولات والإيتر. وتمتاز الألدهيدات الدنيا بروائح نفاذة، أما العليا الحاوية تسع أو عشر ذرات كربونية فروائحها تشبه روائح الزهور.
أبسط أفراد الكيتونات الأسيتون وهو سائل يغلي عند الدرجة 56.4 ْ س، والأفراد التالية (الجدول-1) عبارة عن سوائل، أما العليا فهي مواد صلبة. الكيتونات الدنيا ذوابة في الماء وجميعها ذوابة في الكحولات والإيتر. تمتاز الكيتونات البسيطة بروائح مميزة أما الوسطى فروائحها مقبولة وتشبه رائحة النعنع.
الخواص الكيمياوية للألدهيدات والكيتونات
تعود خواص الألدهيدات والكيتونات في الدرجة الأولى إلى خواص الزمرة الكربونيلية وينشأ الفرق بين الألدهيدات والكيتونات إلى وجود ذرة الهدروجين المرتبطة مباشرة بزمرة الكربونيل في الأولى وعدم وجودها في الثانية.
وتتوقف فعالية الجذر الكربونيلي في مركباته على طبيعة الجذرين المتحدين به وتتناسب عكساً مع حجميهما. فالمتبادلات الضخمة الحجم تقي جذر الكربونيل من الجزيء المهاجم. وتزداد هذه الوقاية بازدياد ضخامة الجذر. ومن التفاعلات التي تخضع لها المركبات الكربونيلية:
1 - تفاعلات الإضافة: تعطي الألدهيدات والكيتونات مع النوكليوفيلات -أي الكواشف الشغوفة بالشحنات الموجبة - منتجات إضافة addition تكون الصيغة الجزيئية لها محصلة لمجموع المواد المتفاعلة؛ 2ـ تفاعلات تكاثف condensation تتحد فيها المواد المتفاعلة ثم تفقد جزيئات بسيطة مثل الماء والكحولات.
أما تفاعلات التكاثف فتحدث بين الألدهيدات والكيتونات وكثير من المركبات الحاوية زمرة -NH2 مشكلة مركبات غير مشبعة
Y قد تكون H أو زمرة ألكيل alkyl أو زمرة أريل aryl
ولوجود زوج إلكتروني وحيد على ذرة آزوت (نتروجين) الأمونيا، يمكنه أن يضاف إلى الألدهيد أو الكيتون. فالتفاعل مع الإيتانال، على سبيل المثال.
يوضح ذلك نمط التفاعل الذي يقوم به الهدرازين N2H4 مع الإيتانال، حيث يشبه في خطوته الأولى التفاعل مع الأمونيا.
يتصف هذا الجزيء بوجوده العابر، فهو ينقصم معطياً جزيئاً يدعى الهدرازون:
يمكن إيجاز التفاعل على النحو:
يصنف التفاعل، بسبب تحرر الماء، على أنه تكاثف (يستعمل هذا الحد أيضاً لوصف التفاعلات العضوية التي تتحرر فيها جزيئات صغيرة نسبياً غير الماء). وتجدر الملاحظة أن هذا التفاعل ليس سوى نمط خاص من الهجوم النكليوفيلي. ولولا وجود الزوج الإلكتروني الوحيد على ذرتي الآزوت في الهدرازين لما أمكن حدوث التفاعل. يبيِّن الجدول تفاعلات عدة من هذا النمط، وقد استخدم الإيتانال في المثال السابق، لكن جميع الألدهيدات والكيتونات الأخرى تعطي تفاعلات مشابهة. ويعزى السبب في أهمية هذه التفاعلات إلى أنها تستخدم في تعرّف الألدهيدات والكيتونات.
التوتوميري (التماكب النزوحي) الكيتو - إنولية keto- enol tautomerism:
تشير بعض خواص الألدهيدات والكيتونات إلى أنه باستطاعة هذه المركبات أن تتفاعل مثل الكحولات غير مشبعة، وبصورة عامة يوجد توازن بين البنيتين الجزيئيتين. البنية الألدهيدية أو الكيتونية وبنية الكحول غير المشبع. ويختل هذا التوازن بإضافة بعض الكواشف فيتحول أي منها بسرعة إلى الأخرى. فهذان الشكلان هما إيزوميران وسمي كل من الشكلين الإيزوميريين توتومير (من اليونانية: tauto نفس، meros أجزاء). وتعرف الصيغة التي تحوي الزمرة الكربونيلية بالشكل الألدهيدي أو الكيتوني؛ وتعرف الصيغة التي تحوي الكحول غير المشبع بالشكل الإينولي أو الإينول.
ويتطلب تشكل البنية الإينولية في كل ألدهيد أو كيتون هجرةَ هدروجين من ذرة الكربون α- على الأكسجين، ونشوء رابطة مضاعفة بين ذرتي الكربون للحفاظ على التكافؤ الرباعي لكل منهما.
وبصورة عامة يمكن أن تحصل حادثة التوتوميري في أي مركب يحوي زمرة -CH2- أو -CH- مجاورة لمجموعة الكربونيل:
وقد ترجمت حادثة التوتوميري إلى العربية بعبارة التماكب النزوحي نسبة إلى الهجرة المذكورة، فالهدروجين α يتصف بخواص الحموضة (النزوحية) والحموضة هنا نسبية وتفسر حموضة الهدروجينات − α هذه باستقرار الأنيون الناتج من نزع بروتون من الموضع − α طنينياً (بالتجاوب).
يمكن للأنيون المتكون من الشكل الإينولي بهذه الطريقة أن يتبرتن (يضم بروتوناً H+) بطريقتين ليعطي مركبات متماكبة تعرف بالمتماكبات الكيتونية والإنولية التي يمكنها أن تتحول إلى أنيون الإنولات enolate بفقدان بروتون.
يحصل هذا التماكب الكيتوني - الإنولي بوجود حفاز قلوي، فحتى الأسس الضعيفة كالسطوح القلوية للأوعية الزجاجية قادرة على تحقيق هذا التماكب. يحتوي أي ألدهيد أو كيتون عادي على تركيز ضئيل من الإنول يصل إلى 1% وقد يرتفع في حالات خاصة إلى 50%.
والكيتون أكثر ثباتاً في الأوساط المعتدلة من الإنول ويحصل هذا التماكب في وسط حمضي.
تعد أنيونات الإنولات المتكونة من الألدهيدات والكيتونات مراحل وسطية في العديد من التفاعلات. وفيما يأتي أهم تفاعلين منها وهما الهلجنة والتكاثف الألدولي .
أ - الهلجنة
تتهلجن الألدهيدات والكيتونات بسرعة بوساطة الهالوجينات عند ذرة الكربون المجاورة للزمرة الكربونيلية وتزداد سرعة الهلجنة بوجود حفاز قلوي أو حمضي. تجري الهلجنة مع أيون الإنولات بفعل القلوي. لذلك تتفاعل الهالوجينات حتى اليود مع الألدهيدات والكيتونات والذي يحدث هو أن ذرة الهالوجين تحل محل ذرة الهدروجين على ذرة الكربون المجاورة لزمرة الكربونيل، في تفاعل نموذجه على النحو الآتي:
وقد وجد بدراسة حركية التفاعل أن اليود لا يتفاعل مباشرة مع البروبانون، بل يتفاعل مع الشكل الإنولي للكيتون، الذي يوجد متوازناً مع الشكل الكيتوني. وتفكك القلويات النواتج ثلاثية الهالوجين معطية الهالوفورم الموافق.
ب - التكاثف الألدولي
إذا أجريت الألدلة بحضور كلوريد التوتياء، أو حمض كلور الماء، أو أي عامل مجرِّد للماء فلن يكون الراسب ألدولاً بل ألدهيداً ذا وظيفة إتيلينية لأن الألدول المتشكل يتجرد من جزيء الماء.
تتفاعل المركبات الكربونيلية في وسط قلوي مع نفسها أو مع المركبات الكربونيلية الأخرى إذا كانت هذه المركبات حاوية زمرة ميتيل أو ميتيلين فعالة (تقع في الموقع -α بالنسبة للكربونيل). يتفاعل الأسيت ألدهيد مع نفسه في وسط قلوي ليعطي الألدول.
يدعى هذا التفاعل التكاثف الألدولي aldol condensation.
تفقد الألدولات الماء عند تسخينها وحدها أو مع قليل من حمض معدني معطية الكروتون ألدهيد crotonaldehyde (التكاثف الكروتوني) وهو ألدهيد غير مشبع
تفاعلات الأكسدة
تحتوي الألدهيدات على ذرة هدروجين متصلة بذرة كربون الكربونيل وهي تتأكسد بسهولة بالمؤكسدات اللطيفة، ولا يحدث ذلك في الكيتونات وهذا هو الاختلاف الواضح الوحيد بين الألدهيدات والكيتونات؛ إذ تقاوم الكيتونات بشدة فعل الأكسدة ولا تتأكسد إلا بصعوبة فاصمة الرابطة كربون-كربون التي تصل زمرة الكربونيل بأحد الجذرين المرتبطين في جزيء الكيتون، معطية حمضين عددُ ذرات الكربون في كل منهما أقل منه في الكيتون الأصلي.
أ - الأكسدة بمحلول فهلنغ Fehling وهو مزيج من محلول كبريتات النحاس ومحلول قلوي من طرطرات الصوديوم والبوتاسيوم حيث يتأكسد الألدهيد إلى حمض في حين يرجع أيون النحاس (II) إلى أكسيد النحاس (I) الأحمر.
ب - الأكسدة بكاشف تولين Tollen وهو محلول نترات الفضة النشادرية، حيث يتأكسد الألدهيد إلى الحمض في حين يرجَع أيون الفضة إلى معدن الفضة الحر على هيئة مرآة.
أما الكيتونات فلا تدخل في مثل هذين التفاعلين إلا أن أكسدتها بمؤكسد قوي تؤدي إلى تحطيمها وفصم الرابطة C-CO وينتج مزيج من الحموض الكربوكسيلية.
تفاعلات الإرجاع
ترجَع الألدهيدات إلى الأغوال الأولية، أما الكيتونات فترجع إلى الأغوال الثانوية. ويمكن أن يؤدي الإرجاع إلى الفحم الهدروجيني الأم حسب المرجعات المستخدمة، يؤدي الإرجاع بـ LiAlH4 أو NaBH4 أو HCl / Zn أو الهدرجة الحفزية بـ (H2/Ni) إلى تكون الكحولات الموافقة:
يتم إرجاع الألدهيدات والكيتونات إلى الفحم الهدروجيني الأم بإحدى طريقتين إما باستخدام ملغمة الزنك وHCl، وإما بمعالجة الألدهيدات أو الكيتونات بالهدرازين وذلك بتسخين الهدرازونات الناتجة حتى 200 ْس بوجود ألكوسيد الصوديوم RONa فيتفكك الهدرازون الناتج إلى الفحم الهيدروجيني:
وتقوم الألدهيدات والكيتونات بتفاعلات كثيرة أخرى منها تكوين الأسيتالات والكيتالات وتفاعلها مع كواشف غرينيار Grignard reagents (هاليدات ألكيل المغنزيوم RMgX).
تتفاعل مركبات غرينيار بالانضمام مع المركبات الكربونيلية مكونة مركبات بينية تعطي عند حلمهتها نواتج تتوقف على بنية المركب الكربونيلي المستخدم، فتعطي مع الفورم ألدهيد كحولات أولية ومع غيره من الألدهيدات كحولات ثانوية، أما مع الكيتونات فإنها تعطي كحولات ثالثية. كما تقوم الألدهيدات بتفاعلات البلمرة (التماثر) فهي تتبلمر بوجود كميات قليلة من حموض قوية إلى تريميرات وتتراميرات حلقية. فالأسيت ألدهيد يتبلمر مثلاً إلى بارا ألدهيد وميتا ألدهيد حسب الوسط الحمضي المستعمل ودرجة حرارة التفاعل.
اختبار شيف
تعطي الألدهيدات مع كاشف شيف Schiff لوناً قرمزياً، في حين لا تستجيب الكيتونات لهذا التفاعل وكاشف شيف محلول لصبغة روزانيلين (الفوكسين) أزيل لونها بـ SO2 .[2]
الحالة الطبيعية والاستعمالات
الكيتونات والألدهيدات المعقدة واسعة الانتشار في الطبيعة: فالسكاكر، على سبيل المثال هي ألدهيدات أو كيتونات متعددة الهدروكسيل.
وهي مركبات وسطية رئيسة في اصطناع عدد كبير من المنتجات مثل المواد اللدنة، والمتفجرات، والمنتجات الصيدلانية، والعطور.
انظر أيضا
المصادر
- ^ فاروق قنديل. "مشتقات ثنائيات الكربونيل". الموسوعة العربية. Retrieved 2012-09-01.
- ^ فاروق قنديل. "الكربونيلية (المشتقات -)". الموسوعة العربية. Retrieved 2012-02-26.
قراءات اضافية
- L.G. Wade, Jr. Organic Chemistry, 5th ed. Prentice Hall, 2002. ISBN 0-13-033832-X
- The Frostburg State University Chemistry Department. Organic Chemistry Help (2000).
- Advanced Chemistry Development, Inc. IUPAC Nomenclature of Organic Chemistry (1997).
- William Reusch. tara VirtualText of Organic Chemistry (2004).
- Purdue Chemistry Department [1] (retrieved Sep 2006). Includes water solubility data.
- William Reusch. (2004) Aldehydes and Ketones Retrieved 23 May 2005.
- ILPI. (2005) The MSDS Hyperglossary- Anhydride.
- روبرت ت.موريسون، وروبرت ن. بويد، الكيمياء العضوية، ترجمة فاروق قنديل وصالح القادري وآخرين (المركز العربي للتعريب والترجمة والتأليف والنشر، دمشق 2000).
- PAULA YURKANIS BRUICE , Organic Chemistry (Prentice Hall ,Pearson Education Inc. 2004).