إپوكسيد
ساهم بشكل رئيسي في تحرير هذا المقال
|
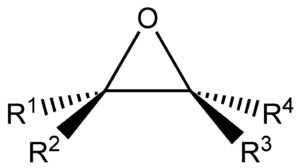
الإپوكسيد Epoxide هو عبارة عن إيثر ثلاثي حلقي (ذرة أكسجين مرتبطة بذرتي كربون). تكون الحلقة تقريباً مثلث متساوي الأضلاع، مما يجعله عالي الانفعال، فالحلقة المنفعلة (ذات الطاقة العالية) يمكن أن تنفتح بكواشف عدة مما يجعل الإبوكسيدات أكثر تفاعلاً من الإيثرات الأخرى.
تحتل ذرة الأكسجين أحد رؤوس المثلث، أي أنه مركب حلقي غير متجانس.
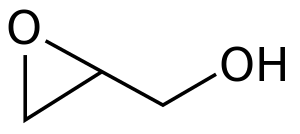
وأبسط هذه المركبات تأخذ اسمها من المركب الأب أكسيد الإثيلين أو الأوكسيران Oxirane، مثل كلورومثيلأوكسيران chloromethyloxirane. وكمجموعة وظيفية، فإن الإپوكسيدات يسبق اسم كل منها بالسابقة "إپوكسي" كما في المركب 1,2-epoxycycloheptane الذي يمكن أن يـُسمى أيضاً cycloheptene epoxide، أو ببساطة cycloheptene oxide.
الپوليمر الحاوي على وحدات من الإبوكسيد غير المتفاعل يسمى پوليإپوكسيد Polyepoxide أو إپوكسي epoxy. راتنجات الإپوكسي تستعمل كمواد لاصقة ومواد بناء. پلمرة إپوكسيد تنتج پوليإيثر، فعلى سبيل المثال أكسيد الإثيلين يتبلمر ليعطي پوليإثيلين گليكول، المعروف أيضاً بإسم أكسيد الپوليإثيلين.
التخليق
هناك عدة طرق لتحضير الإپوكسيدات، هي:
فوق أكسدة الاولفين
معاملة الألكن مع فوق الحموض Olefin peroxidation
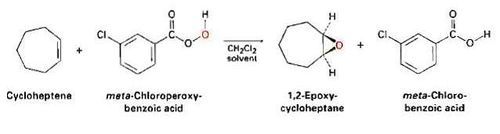
عاملنا ألكين هو حلقي الهبتان مع فوق حمض (RCO3H) هو فوق حمض ميتاـ كلورو بنزوئيك، فتشكل الإيبوكسيد وهو عبارة عن 1-2 إيبوكسي حلقي الهبتان.
وهذه الطريقة الأكثر استخداماً لتحضير الإيبوكسيدات في المخابر.
معظم الإپوكسيدات يتم توليدها بمعالجة ألكينات alkene بكواشف تحتوي على فوق الأكسيد peroxide.
يتواصل التفاعل عبر ما يشيع تسميته "آلية الفراشة."[1] ويـُنظـَر إلى فوق الأكسيد على أنه محب للإلكترون، وللألكين على أنه محب للنواة. ويعتبر التفاعل منسـَقاً (الأرقام في الآلية المعروضة أدناه هي للتبسيط).
إحلال SN2 داخل الجزيء
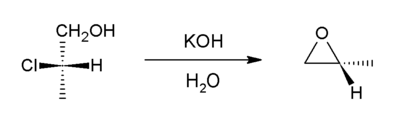
أو التحضير من هالو الهيدرينات. هذه الطريقة هي تنويعة من تخليق إيثر وليامسون. في هذه الحالة، يحل أيون ألكوكسيد محل ذرة كلوريد داخل نفس الجزيء. المركبات السابقة تسمى هالوهيدرينات.
الهالوهيدرين الذي يحوي هالوجين (بروم، كلور ....) ومجموعة OH، نحضره بداية من الألكِن بمفاعلته مع الهالوجين والماء، ثم نعامله في وسط قلوي (NaOH) فيعطي الإيبوكسيد.[2]
تقريباً نصف انتاج العالم من أكسيد الپروپيلين يأتي من هذا الطريق،[3] فتفاعل تشكيل الإپوكسيد داخل الجزيء هو أحد الخطوات الرئيسية في تفاعل دارزنس.
ففي تفاعل جونسون-كوري-تشايكوڤسكي تتولد الإبوكسيدات من مجموعات الكربونيل و إليدات السلفونيوم. وفي هذا التفاعل، يكون السلفونيوم هو المجموعة المغادرة بدلاً من الكلوريد.
الإپوكسدة المحبة للنواة
الإپوكسدة غير المتماثلة
تفاعل فتح الحلقة Ring opening
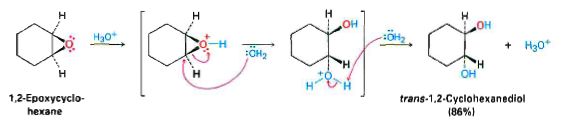
بوسط حمضي ثم ماءAcid catalyzed epoxide opening
يتم شطر الإيبوكسيدات عند معالجتها بحمض تماما كباقي الإيثرات، لكن يمكن أن يتم ذلك تحت شروط أخف وذلك بسبب التوتر في الحلقة ring strain . وكما سنلاحظ، فإن وجود حمض مميه (حمض وماء) وممدد بدرجة حرارة الغرفة كافٍ ليقوم بحلمهة الإيبوكسيدات إلى "مفروق 1،2ديولات" Trans1,2diols
في التفاعل السابق تم وضع الإيبوكسيد في وسط حمضي فأخذ الأكسجين بروتوناً فتشكلت شارة أوكسونيوم ، ويذهب المزدوج الالكتروني ويتشكل كاربوكاتيون C+ ، ثم تأتي جزيئة ماء لترتبط على الـ C+ أوبعدها يُطرد بروتون من الماء فيبقى OH ويتشكل ديول ترانس.
وبنفس الآلية يعطينا أكسيد الإثيلين في وسط حمضي ديول هو الإثيلين غليكول