أكسجة غشائية خارج الجسم
| Extracorporeal membrane oxygenation | |
|---|---|
 | |
| أسماء أخرى | Extracorporeal life support (ECLS) |
| ICD-10-PCS | 5A15223 |
| ICD-9-CM | 39.65 |
| MeSH | 29295 |
| MedlinePlus | 007234 |
| HCPCS-L2 | 36822 |
الأكسجة الغشائية خارج الجسم ( ECMO ) ، والمعروفة أيضًا باسم دعم الحياة خارج الجسم ( ECLS ) ، هي تقنية خارج الجسم لتوفير دعم طويل الأمد للقلب والجهاز التنفسي للأشخاص الذين لا يستطيع القلب والرئتين توفير كمية كافية من تبادل الغازات أو التروية للحفاظ على الحياة. إن تقنية ECMO مستمدة إلى حد كبير من المجازة القلبية الرئوية ، والتي توفر دعمًا على المدى القصير مع الدورة الدموية الاصلية الموقوفة.
يعمل ECMO عن طريق سحب الدم مؤقتًا من الجسم للسماح بالأكسجة الاصطناعية لخلايا الدم الحمراء وإزالة ثاني أكسيد الكربون. بشكل عام ، يتم استخدامه إما في مجازة ما بعد القلب أو في مرحلة متأخرة من العلاج لشخص يعاني من قصور شديد في القلب و / أو فشل الرئة ، على الرغم من أنه يرى الآن استخدامًا لعلاج السكتة القلبية في بعض المراكز ، مما يسمح بعلاج السبب الأساسي من التوقف بينما يتم دعم الدورة الدموية والأكسجين. يستخدم ECMO أيضًا لدعم المرضى المصابين بالالتهاب الرئوي الفيروسي الحاد المرتبط بـ COVID-19 في الحالات التي لا تكون فيها التنفس الصناعي كافي للحفاظ على مستويات الأكسجين في الدم.
الاستخدامات الطبية
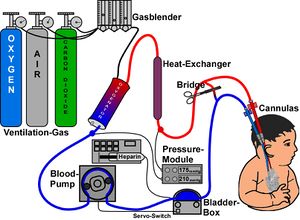

يتم نشر المبادئ التوجيهية التي تصف مؤشرات وممارسات ECMO من قبل منظمة دعم الحياة خارج الجسم (ELSO). تختلف معايير بدء ECMO حسب المؤسسة ، ولكنها تشمل بشكل عام الفشل القلبي أو الرئوي الحاد الذي يمكن عكسه ولا يستجيب للسيطرة التقليدية. تتضمن الأمثلة على الحالات السريرية التي قد تحفز بدء ECMO ما يلي:[1]
- فشل تنفسي نتيجة نقص الأكسجين مع نسبة شدة الأكسجين الشرياني إلى جزء من الأكسجين المستنشق (PaO2 / FiO2) <100 ملم زئبقي على الرغم من تحسين إعدادات التهوية ، بما في ذلك جزء الأكسجين المستنشق (FiO2) ، ضغط الزفير النهائي الإيجابي (PEEP) ، ونسبة الشهيق إلى الزفير (I: E)
- فشل الجهاز التنفسي نتيجة لفرط ثاني اكسد الكربون مع درجة الحموضة الشريانية <7.20
- صدمة قلبية مستعصية
- توقف القلب
- الفشل في الفصل من المجازة القلبية الرئوية بعد جراحة القلب
- كجسر إما لزرع القلب أو وضع جهاز مساعدة البطين
- كجسر لزرع الرئة
- الصدمة الإنتانية هي مثيرة للجدل اكثر ولكن تم دراستها بشكل متزايد من ECMO
- انخفاض حرارة الجسم ، مع درجة حرارة أساسية تتراوح بين 28 و 24 ° C وعدم استقرار القلب ، أو مع درجة حرارة قلب أقل من 24 درجة مئوية.[2]
في أولئك الذين يعانون من السكتة القلبية أو الصدمة القلبية ، يبدو أنه يحسن البقاء والنتائج الجيدة .[3]
استخدلم في مرضى COVID-19
بدءًا من أوائل فبراير 2020 ، يستخدم الأطباء في الصين بشكل متزايد ECMO كدعم مساعد للمرضى الذين يعانون من الالتهاب الرئوي الفيروسي الحاد المرتبط بعدوى SARS-CoV-2 ( COVID-19 ) عندما تظل مستويات أكسجة الدم حتى بعد التهوية منخفضة للحفاظ على المريض.[4] تشير التقارير الأولية إلى أنها تساعد في استعادة تشبع الأكسجين في الدم لدى المرضى وتقليل الوفيات بين ما يقرب من 3 ٪ من الحالات الشديدة حيث تم استخدامه .[5] بالنسبة للمرضى المصابين بأمراض خطيرة ، ينخفض معدل الوفيات من حوالي 59-71٪ مع العلاج التقليدي إلى حوالي 46٪ مع أكسجة الأغشية خارج الجسم .[6]
النتائج
وقد أظهرت الدراسات المبكرة فائدة البقاء على قيد الحياة مع استخدام ECMO للأشخاص الذين يعانون من فشل تنفسي حاد خاصة في وضع متلازمة الضائقة التنفسية الحادة .[7][8] استمر تسجيل من قبل ELSO لما يقرب من 51000 شخص تلقوا ECMO أبلغ عن نتائج مع بقاء 75 ٪ لفشل الجهاز التنفسي عند الوليد ، و 56 ٪ لفشل الجهاز التنفسي لدى الأطفال ، و 55 ٪ للبقاء على قيد الحياة لفشل الجهاز التنفسي لدى البالغين .[9] سجلت التجارب السريرية الأخرى غير المراقبة والمراقبة معدلات بقاء من 50 إلى 70 في المائة .[10][11] هذه معدلات البقاء على قيد الحياة أفضل من معدلات البقاء التاريخية .[12][13][14] على الرغم من أن ECMO يستخدم لمجموعة من الحالات بمعدلات وفيات متفاوتة ، فإن الكشف المبكر هو المفتاح لمنع تطور التدهور وزيادة نتائج البقاء على قيد الحياة .[15]
في المملكة المتحدة ، يتركز تعيين ECMO الوريدي في مراكز ECMO المخصصة لتحسين الرعاية المحتملة وتعزيز نتائج أفضل.
موانع الاستخدام
معظم موانع الاستعمال نسبية ، وتوازن بين مخاطر الإجراء مقابل الفوائد المحتملة. موانع النسبية هي:
- ظروف لا تتوافق مع الحياة الطبيعية إذا تعافى الشخص
- الظروف الموجودة مسبقًا التي تؤثر على نوعية الحياة (حالة الجهاز العصبي المركزي ، ورم خبيث في المرحلة النهائية ، وخطر حدوث نزيف جهازي مع منع تخثر الدم)
- العمر والحجم
- الفشل: أولئك الذين يعانون من مرض شديد ، أو الذين خضعوا للعلاج التقليدي لفترة طويلة جدًا ، أو لديهم تشخيص قاتل.
الاثار الجانبية
عصبي
إحدى النتائج الشائعة لدى البالغين الذين يعالجون ECMO هي الإصابة العصبية ، والتي قد تشمل نزيف داخل الدماغ ، ونزيف تحت العنكبوتية واحتشاءات إقفارية في المناطق الحساسة من الدماغ ، واعتلال الدماغ الإقفاري نقص الأكسجة ، وغيبوبة غير مفسرة ، وموت المخ .[16] يحدث النزيف في 30 إلى 40 في المائة من أولئك الذين يتلقون ECMO ويمكن أن يهدد الحياة. ويرجع ذلك إلى كل من ضخ الهيبارين المستمر والخلل الوظيفي في الصفائح الدموية. تقنية جراحية دقيقة ، والحفاظ على عدد الصفائح الدموية أكبر من 100000 / مم 3 ، والحفاظ على الهدف من التخثر المنشط يقلل من احتمال النزيف[citation needed]
الدم
قلة الصفيحات التي يسببها الهيبارين (HIT) شائعة بشكل متزايد بين الأشخاص الذين يتلقون ECMO. عندما يُشتبه في حدوث HIT ، يتم استبدال تسريب الهيبارين عادة بمضاد تخثر غير الهيبارين. .[17]
هناك تدفق الدم إلى الوراء في الأبهر الهابط كلما تم استخدام الشريان والوريد الفخذي في حالة ECMO. يمكن أن يحدث ركود الدم إذا لم يتم الحفاظ على مُخْرَجٌ البطين الأيسر ، مما قد يؤدي إلى تجلط الدم. .[citation needed]
جسر لمساعدة الجهاز
في ECMO الشرياني الوريدي ، أولئك الذين لا تتعافى وظائفهم القلبية بشكل كاف ليتم فصلهم من ECMO يمكن ربطهم بجهاز مساعدة البطين (VAD) أو زرع. يمكن أن تحدث مجموعة متنوعة من المضاعفات أثناء عملية الإقناء ، بما في ذلك ثقب الأوعية الدموية مع النزيف ، وتسلخ الشرايين ، والإقفار البعيد ، والموقع غير الصحيح (على سبيل المثال ، قنية الوريد الموضوعة داخل الشريان) ، ولكن هذه الأحداث تحدث بشكل غير متكرر .[citation needed]
اطفال
إن الخدج معرضون لخطر مرتفع بشكل غير مقبول للنزيف داخل البطيني (IVH) إذا تم إعطاؤه ECMO في عمر الحمل أقل من 32 أسبوعًا. .[18]
الانواع


هناك عدة أشكال من ECMO. النوعان الأكثر شيوعًا هما ECMO الوريدي الشرياني (VA) و ECMO الوريدي الوريدي (VV). في كلتا الحالتين ، الدم الذي يتم سحبه من الجهاز الوريدي يتم اكسجته خارج الجسم. في ECMO الشرياني الوريدي ، يتم إرجاع هذا الدم إلى الجهاز الشرياني وفي ECMO وريدي-الوريدي يتم إرجاع الدم إلى الجهاز الوريدي . فيECMO وريدي-الوريدي ، لا يتم توفير دعم القلب.
وريدي -شرياني
في ECMO الوريدي الشرياني (VA) ، عادة ما يتم وضع قنية وريدية في الوريد الفخذي الأيمن أو الأيسر لاستخراجها ، وعادة ما يتم وضع قنية الشرايين في الشريان الفخذي الأيمن أو الأيسر للتسريب.[20] يجب الحفاظ على رأس قنية الفخذ الوريدي بالقرب من تقاطع الوريد الأجوف السفلي والأذين الأيمن ، بينما يتم الحفاظ على رأس قنية الشريان الفخذي في الشريان الحرقفي .[20] Iفي البالغين ، يُفضل الوصول إلى الشريان الفخذي لأن الإدخال أسهل .[20] يمكن استخدام ECMO الوريدي الشرياني المركزي إذا تم بالفعل إجراء المجازة القلبية الرئوية أو تم إجراء بضع القفص الطارئ (مع قنية في الأذين الأيمن (أو الوريد الأجوف العلوي / الوريد الأجوف سفلي لإصلاح الصمام ثلاثي الشرف) والأبهر الصاعد) .
يُحفظ ECMO الوريدي الشرياني عادةً عندما تكون وظيفة القلب الأصلية في الحد الأدنى للتخفيف من زيادة السكتة القلبية المرتبطة بالضخ ضد التدفق التراجعي الناتج عن قنية الأبهر.
وريدي-وريدي
في ECMO الوريدي الوريدي (VV) ، عادة ما توضع الكانيولات في الوريد الفخذي الأيمن لتصريف الوريد الوداجي الداخلي الأيمن للتسريب .[21] بدلاً من ذلك ، يتم إدخال قسطرة مزدوجة التجويف في الوريد الوداجي الداخلي الصحيح ، وتصريف الدم من الوريد الأجوف العلوي والسفلي وإعادته إلى الأذين الأيمن.
البدء
يجب أن يتم تنفيذ ECMO فقط من قبل الأطباء الذين لديهم تدريب وخبرة في بدايته وصيانته وإيقافه. يتم إجراء إدخال ECMO عادةً في غرفة العمليات من قبل جراح القلب والصدر . يتم إجراء التحكم في ECMO بشكل شائع من قبل ممرضة مسجلة أو معالج في الجهاز التنفسي أو متخصص في التروية. بمجرد أن تقرر بدء ECMO ، يتم منع المريض من تخثر الدم بالهيبارين الوريدي لمنع تكوين الجلطة من تجلط المكساج. قبل البدء ، يتم إعطاء بلعة في الوريد من الهيبارين وقياسها للتأكد من أن تتنشيط زمن التخثر يتراوح بين 300-350 ثانية. بمجرد أن يكون تنشيط زمن التخثر بين هذا النطاق ، يمكن بدء ECMO وسيبدأ تنقيط الهيبارين بعد ذلك كجرعة مداومة.[22]
إقناء
قنية يمكن وضعها عن طريق الجلد بواسطة طريقة سيلدينغر ، وهي طريقة بسيطة نسبيا والمشترك للحصول على الوصول إلى الأوعية الدموية، أو عن طريق فغر جراحي. يتم استخدام أكبر القنيات التي يمكن وضعها في الأوعية لزيادة التدفق وتقليل إجهاد القص.
يمكن وضع ECMO المطلوب لمضاعفات جراحة ما بعد القلب مباشرة في غرف القلب أو الأوعية الكبيرة المناسبة. تسمح القنية المركزية من خلال بضع الصدر الجانبي للمرضى الذين ينتظرون زراعة الرئة بالبقاء غير مسكنين ومتنقلين .[23]
معايرة
بعد الإقناء والاتصال بدائرة ECMO ، يتم تحديد الكمية المناسبة من تدفق الدم عبر دائرة ECMO باستخدام المعلمات الديناميكية الدموية والفحص البدني. تتم موازنة أهداف الحفاظ على تروية العضو النهائي عبر دائرة ECMO مع تدفق الدم الفسيولوجي الكافي عبر القلب لمنع الركود والتكوين اللاحق لجلطة الدم.
الحفاظ

بمجرد تحقيق الأهداف التنفسية والديناميكية الدموية الأولية ، يتم الحفاظ على تدفق الدم عند هذا المعدل. يتم تسهيل التقييم والتعديلات المتكررة من خلال قياس التأكسج الوريدي المستمر ، الذي يقيس تشبع الأوكسي هيموغلوبين الدم مباشرة في الطرف الوريدي لدائرة ECMO.
اعتبارات خاصة
يستخدم وريدي-وريدي ECMO عادة لفشل الجهاز التنفسي ، بينما يستخدم ECMO الشرياني -الوريدي لفشل القلب. هناك اعتبارات فريدة لكل نوع من أنواع ECMO التي تؤثر على المعالجة.
تدفق الدم
عادة ما تكون معدلات التدفق القصوى تقريبًا مطلوبة خلال ECMO الوريدي- الوريدي لتحسين توصيل الأكسجين. في المقابل ، يجب أن يكون معدل التدفق المستخدم أثناء ECMO الشرياني الوريدي مرتفعًا بما يكفي لتوفير ضغط تروية مناسب وتشبع الأوكسي هيموغلوبين الوريدي (يقاس على دم مصرف) ولكنه منخفض بما يكفي لتوفير التحميل المسبق الكافي للحفاظ على مخرج البطين الأيسر.
إدرار البول
نظرًا لأن معظم الناس يعانون من زيادة السوائل عند بدء ECMO ، فإن إدرار البول العدواني مضمون حدوثه بمجرد استقرار المريض في ECMO. يمكن إضافة الترشيح الفائق بسهولة إلى دائرة ECMO إذا كان المريض يعاني من عدم كفاية إخراج البول. "ثرثرة" ECMO ، أو عدم استقرار الأشكال الموجية ECMO ، يمثل نقصًا في الإنعاش ويدعم وقف إدرار البول العدواني أو الترشيح الفائق.
مراقبة البطين الايسؤ
تتم مراقبة خرج البطين الأيسر بصرامة أثناء ECMO الشرياني-الوريدي لأن وظيفة البطين الأيسر يمكن أن تضعف من زيادة حمولة تلوية ، مما قد يؤدي بدوره إلى تكوين الجلطة داخل القلب. .[24][25]
الانقطاع والتوقف
بالنسبة لأولئك الذين يعانون من فشل في الجهاز التنفسي ، تشير التحسينات في المظهر الشعاعي ، والمطاوعة الرئوية ، وتشبع الأوكسي هيموغلوبين الشرياني إلى أن الشخص قد يكون جاهزًا للتخلص من دعم ECMO. بالنسبة لأولئك الذين يعانون من قصور في القلب ، يرتبط نبض الأبهر المعزز بتحسين إخراج البطين الأيسر ويشير إلى أنهم قد يكونون مستعدين للإقلاع عن دعم ECMO. إذا كانت جميع العلامات في حالة جيدة ، فإن تدفقات الدم على ECMO ستنخفض ببطء وسيتم ملاحظة معالم المرضى خلال هذا الوقت لضمان قدرة المريض على تحمل التغييرات. عندما تكون التدفقات أقل من 2 لتر في الدقيقة ، تتم محاولة الإزالة الدائمة ويستمر مراقبة المريض خلال هذا الوقت حتى يمكن إزالة الكانيولات (قنيات)) .[26]
تجربة تحرير ECMO الوريدي الوريدي
يتم إجراء تجارب ECMO وريدي-الوريدي من خلال التخلص من جميع غازات التيار المعاكس من خلال مكساج. يبقى تدفق الدم خارج الجسم ثابتًا ، ولكن لا يحدث نقل الغاز. ثم تتم ملاحظتها لعدة ساعات ، يتم خلالها تحديد إعدادات جهاز التهوية اللازمة للحفاظ على الأكسجين والتهوية الكافيين خارج ECMO كما هو مبين في نتائج غازات الدم الشرياني والوريدي.
تجربة تحرير ECMO الشرياني الوريدي
تتطلب تجارب ECMO الشرياني الوريدي ربطاً مؤقتًا لكل من خطوط التصريف والتسريب ، بينما تسمح لدائرة ECMO بالتدوير من خلال جسر بين الأطراف الشريانية والوريدية. هذا يمنع تجلط الدم الراكد داخل دائرة ECMO. بالإضافة إلى ذلك ، يجب تدفق الخطوط الشريانية والوريدية باستمرار باستخدام محلول ملحي من الهيبارين أو بشكل متقطع مع دم من الهيبارين من الدائرة. بشكل عام ، تعد تجارب ECMO الشرياني الوريدي أقصر في المدة من تجارب ECMO الوريدي الوريدي بسبب ارتفاع خطر تكوين الجلطة.
التاريخ
تم تطوير ECMO في الخمسينيات من قبل جون جيبون ، ثم بواسطة C. Walton Lillehei . أول استخدام لحديثي الولادة كان عام 1965 .[27][28]
أثبت بان غراي لاري ، دكتوراه في الطب ، أن الأكسجين الوريدي يمكن أن يحافظ على الحياة. نُشرت نتائجه في The Surgical Forum ، نوفمبر 1951 .[29] وعلق الدكتور لاري على عمله الأولي في عرض تقديمي عام 2007 حيث كتب: "بدأ بحثنا بتجميع جهاز ، لأول مرة ، أبقى الحيوانات على قيد الحياة أثناء استنشاق النيتروجين النقي. تم تحقيق ذلك مع فقاعات صغيرة جدًا من الأكسجين المحقون في مجرى الدم. صنعت هذه الفقاعات عن طريق إضافة "عامل ترطيب" إلى الأكسجين يتم إجباره من خلال مرشح الخزف في مجرى الدم الوريدي. بعد فترة وجيزة من عرضها الأولي للكلية الأمريكية للجراحين ، تمت مراجعة هذا الجهاز من قبل والتون ليلهي الذي صنع مع DeWall أول جهاز عملي لرئة القلب يعمل باستخدام مكساج فقاعي. مع اختلافات تم استخدام هذه الآلات للسنوات العشرين المقبلة."
المجتمع والثقافة
الشركات المصنعة
 مدترونيك[30]
مدترونيك[30] ماكيه[30] (مجموعة Getinge)
ماكيه[30] (مجموعة Getinge) Xenios AG[30] (فريزينيوس للرعاية الطبية)
Xenios AG[30] (فريزينيوس للرعاية الطبية) مجموعة سورين[30]
مجموعة سورين[30] تيرومو[30]
تيرومو[30] نيبرو[30]
نيبرو[30] ميكروبورت[30]
ميكروبورت[30]
الاتاحة
This section requires expansion. (March 2020) |
| الدولة/المنطقة | القارة | تجهيز المستشفيات | الوحدات |
|---|---|---|---|
| أمريكا الشمالية | 264 (in 2019)[31] | ||
| أمريكا الشمالية | 32 (in 2020)[32] | ||
| أوروبا | 5 (in 2020)[33] | 15 (in 2020)[33] | |
| أوروبا | 0 (in 2020)[34] | 0 (in 2020)[34] | |
| قالب:Country data SCTScotland | أوروبا | 0 (in 2020)[34] | 0 (in 2020)[34] |
| أوروبا | 214 (in 2020)[35] | 755 (in 2020)[36] | |
| أوروبا | 47 (in 2020)[37] | ||
| أوروبا | ≥7 (in 2020)[38] | ||
| أوروبا | 0 (in 2020)[39] | 0 (in 2020)[39] | |
| أوروبا | 124 + 17 (in 2020)[40] | ||
| أوروبا | 16 (in 2020)[41] | ||
| أوروبا | 7 | 19 (in 2020)[42] | |
| اسيا | 2,208 (in 2020)[43] | ||
| اسيا | approx. 400 (in 2020)[44] |
البحث
أظهرت دراسة أجريت عام 2014 أن الجسم المضاد المثبط للعامل XIIa يوفر الحماية من الجلطات في الدورة الدموية خارج الجسم دون زيادة خطر النزيف .[45] وأظهرت التجارب على الحيوانات حديثي الولادة أن علاج ECMO يمكن أن يؤدي إلى استموات للخلايا المعوية ، و تلف حاجز المخاطي المعوي والإزفاء البكتيري. قد يفسر هذا شدة أكبر لمتلازمة الاستجابة الالتهابية الجهازية عند حديثي الولادة .[46] كما رأى ECMO استخدامه في الجثث على أنه قادر على زيادة معدل صلاحية الأعضاء المزروعة .[47]
المراجع
- ^ "General Guidelines for all ECLS Cases" (PDF). Extracorporeal Life Support Organization. Retrieved أبريل 15, 2015.
- ^ State of New Hampshire Patient Care Protocols v7. New Hampshire: NH Medical Control Board. 2018. p. 2.10.
- ^ Ouweneel, DM; Schotborgh, JV; Limpens, J; Sjauw, KD; Engström, AE; Lagrand, WK; Cherpanath, TG; Driessen, AH; de Mol, BA; Henriques, JP (سبتمبر 19, 2016). "Extracorporeal life support during cardiac arrest and cardiogenic shock: a systematic review and meta-analysis". Intensive Care Medicine. 42 (12): 1922–34. doi:10.1007/s00134-016-4536-8. PMC 5106498. PMID 27647331.
- ^ "30 to 39 pct of severe COVID-19 patients discharged from Wuhan hospitals: official - Xinhua | English.news.cn". xinhuanet.com. Retrieved فبراير 16, 2020.
- ^ CDC (فبراير 11, 2020). "2019 Novel Coronavirus (2019-nCoV)". Centers for Disease Control and Prevention (in الإنجليزية الأمريكية). Retrieved فبراير 16, 2020.
- ^ Melhuish, Thomas M.; Vlok, Ruan; Thang, Christopher; Askew, Judith; White, Leigh (مايو 2020). "Outcomes of extracorporeal membrane oxygenation support for patients with COVID-19: A pooled analysis of 331 cases". The American Journal of Emergency Medicine. doi:10.1016/j.ajem.2020.05.039.
- ^ Peek, GJ; Moore, HM; Moore, N; Sosnowski, AW; Firmin, RK (1997). "Extracorporeal membrane oxygenation for adult respiratory failure". Chest. 112 (3): 759–64. doi:10.1378/chest.112.3.759. PMID 9315812.
- ^ Lewandowski, K.; Rossaint, R.; Pappert, D.; Gerlach, H.; Slama, K.-J.; Weidemann, H.; Frey, D. J. M.; Hoffmann, O.; Keske, U. (1997). "High survival rate in 122 ARDS patients managed according to a clinical algorithm including extracorporeal membrane oxygenation". Intensive Care Medicine. 23 (8): 819–35. doi:10.1007/s001340050418. PMID 9310799.
- ^ Paden, Matthew L.; Conrad, Steven A.; Rycus, Peter T.; Thiagarajan, Ravi R. (أبريل 1, 2017). "Extracorporeal Life Support Organization Registry International Report 2016". ASAIO Journal. 63 (1): 60–67. doi:10.1097/MAT.0000000000000475. PMID 27984321.
- ^ Hemmila, Mark R.; Rowe, Stephen A.; Boules, Tamer N.; Miskulin, Judiann; McGillicuddy, John W.; Schuerer, Douglas J.; Haft, Jonathan W.; Swaniker, Fresca; Arbabi, Saman (2004). "Extracorporeal Life Support for Severe Acute Respiratory Distress Syndrome in Adults". Annals of Surgery. 240 (4): 595–605, discussion 605–07. doi:10.1097/01.sla.0000141159.90676.2d. PMC 1356461. PMID 15383787.
- ^ Brogan, Thomas V.; Thiagarajan, Ravi R.; Rycus, Peter T.; Bartlett, Robert H.; Bratton, Susan L. (2009). "Extracorporeal membrane oxygenation in adults with severe respiratory failure: A multi-center database". Intensive Care Medicine. 35 (12): 2105–14. doi:10.1007/s00134-009-1661-7. PMID 19768656.
- ^ Kolla, S; Awad, SS; Rich, PB; Schreiner, RJ; Hirschl, RB; Bartlett, RH (1997). "Extracorporeal life support for 100 adult patients with severe respiratory failure". Annals of Surgery. 226 (4): 544–64, discussion 565–66. doi:10.1097/00000658-199710000-00015. PMC 1191077. PMID 9351722.
- ^ Rich, PB; Awad, SS; Kolla, S; Annich, G; Schreiner, RJ; Hirschl, RB; Bartlett, RH (1998). "An approach to the treatment of severe adult respiratory failure". Journal of Critical Care. 13 (1): 26–36. doi:10.1016/S0883-9441(98)90026-0. PMID 9556124.
- ^ Ullrich, R; Lorber, C; Röder, G; Urak, G; Faryniak, B; Sladen, RN; Germann, P (1999). "Controlled airway pressure therapy, nitric oxide inhalation, prone position, and extracorporeal membrane oxygenation (ECMO) as components of an integrated approach to ARDS". Anesthesiology. 91 (6): 1577–86. doi:10.1097/00000542-199912000-00007. PMID 10598597.
- ^ Lich, Byran (2004). The Manual of Clinical Perfusion (2nd ed.). Fort Myers, Florida: Perfusion.com. ISBN 978-0-9753396-0-2.
- ^ Mateen, Farrah J.; Muralidharan, R.; Shinohara, R. T.; Parisi, J. E.; Schears, G. J.; Wijdicks, E. F. (2011). "Neurological Injury in Adults Treated With Extracorporeal Membrane Oxygenation". Archives of Neurology. 68 (12): 1543–49. doi:10.1001/archneurol.2011.209. PMID 21825216.
- ^ Cornell, Timothy; Wyrick, Polly; Fleming, Geoffrey; Pasko, Deborah; Han, Yong; Custer, Joseph; Haft, Jonathan; Annich, Gail (2007). "A Case Series Describing the Use of Argatroban in Patients on Extracorporeal Circulation". ASAIO Journal. 53 (4): 460–63. doi:10.1097/MAT.0b013e31805c0d6c. PMID 17667231.
- ^ Jobe, Alan H. (2004). "Post-conceptional age and IVH in ECMO patients". The Journal of Pediatrics. 145 (2): A2. doi:10.1016/j.jpeds.2004.07.010.
- ^ أ ب Van Meurs, Krisa; Lally, Kevin; Zwischenberger, Joseph B.; Peek, Giles, eds. (2005). ECMO: Extracorporeal Cardiopulmonary Support in Critical Care. Ann Arbor: Extracorporeal Life Support Organization. ISBN 978-0-9656756-2-8.[صفحة مطلوبة]
- ^ أ ب ت Madershahian, Navid; Nagib, Ragi; Wippermann, Jens; Strauch, Justus; Wahlers, Thorsten (2006). "A Simple Technique of Distal Limb Perfusion During Prolonged Femoro-Femoral Cannulation". Journal of Cardiac Surgery. 21 (2): 168–69. doi:10.1111/j.1540-8191.2006.00201.x. PMID 16492278.
- ^ Wang, Dongfang; Zhou, Xiaoqin; Liu, Xiaojun; Sidor, Bill; Lynch, James; Zwischenberger, Joseph B. (2008). "Wang-Zwische Double Lumen Cannula – Toward a Percutaneous and Ambulatory Paracorporeal Artificial Lung". ASAIO Journal. 54 (6): 606–11. doi:10.1097/MAT.0b013e31818c69ab. PMID 19033774.
- ^ Lich, Bryan (2004). The Manual of Clinical Perfusion (2nd ed.). Fort Myers, Florida: Perfusion.com. p. 143. ISBN 978-0-9753396-0-2.
- ^ Chierichetti, M.; Santini, A.; Pagan, F.; Crotti, S.; Lissoni, A.; Gattinoni, L. (2012). "ECMO in nonintubated patients as a bridge to lung transplant: Our experience". Critical Care. 16: 97. doi:10.1186/cc10704.
- ^ Cohen, Gordon; Permut, Lester (2005). "Decision making for mechanical cardiac assist in pediatric cardiac surgery". Seminars in Thoracic and Cardiovascular Surgery: Pediatric Cardiac Surgery Annual. 8: 41–50. doi:10.1053/j.pcsu.2005.02.004. PMID 15818357.
- ^ Vural, Kerem M. (2008). "Ventricular assist device applications". Anadolu Kardiyoloji Dergisi. 8 (Suppl 2): 117–30. PMID 19028644.
- ^ Lich, Bryan (2004). The Manual of Clinical Perfusion (2nd ed.). Fort Myers, Florida: Perfusion.com. p. 149. ISBN 978-0-9753396-0-2.
- ^ "Pediatric Extracorporeal Membrane Oxygenation".
- ^ Mosier, Jarrod M.; Kelsey, Melissa; Raz, Yuval; Gunnerson, Kyle J.; Meyer, Robyn; Hypes, Cameron D.; Malo, Josh; Whitmore, Sage P.; Spaite, Daniel W. (2015). "Extracorporeal membrane oxygenation (ECMO) for critically ill adults in the emergency department: history, current applications, and future directions". Critical Care. 19: 431. doi:10.1186/s13054-015-1155-7. hdl:10150/621244. PMC 4699333. PMID 26672979.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Lary, Banning Gray (نوفمبر 1951). "Experimental Maintenance of Life by Intravenous Oxygen: Preliminary Report (from the Department of Surgery, University of Iliniois College of Medicine, and St Luke's Hospital, Chicago, Illinois)". Surgical Forum: 30–35 – via W.B. Saunders Company, Philadelphia 1952 (publisher) The Proceedings of the Forum Sessions 37th Clinical Congress of the American College of Surgeons, San Francisco, California, November, 1951.
- ^ أ ب ت ث ج ح خ "ExtraCorporeal Membrane Oxygenation Market 2020 Recent Trends, Analysis, Business Growth, Share Estimation and Regional Overview Forecast by 2026". MarketWatch. أبريل 16, 2020.
- ^ Miracle medical machine ECMO makes heroic rescues, but leaves patients in limbo. USA Today. June 17, 2019.
- ^ Coronavirus outbreak: B.C. health officials confirm 11 new cases of COVID-19 (14:40-). Global News. March 14, 2020.
- ^ أ ب Coronavirus: England only has 15 beds for worst respiratory cases. The Guardian. February 27, 2020.
- ^ أ ب ت ث Northern Ireland, Scotland and Wales rank amongst the lowest countries in the developed world for the number of intensive care beds. Slugger O'Toole. March 4, 2020.
- ^ Intensivregister قالب:LL. May 10 2020
- ^ "Intensivregister Tagesreport 2020-05-18" (PDF). DIVI Intensivregister. Retrieved مايو 20, 2020.
{{cite news}}: CS1 maint: url-status (link)[dead link] - ^ Walka z koronawirusem. Ile w Polsce jest urządzeń do wspomagania oddychania? قالب:LL. TVN24. March 12, 2020.
- ^ Få Ecmo-platser för svårt coronasjuka på Nya Karolinska قالب:LL. Dagens Nyheter. March 10, 2020.
- ^ أ ب Mjeku shqiptar në Gjermani: Ka disa kushte për vetizolimin, në Shqipëri nuk ka aparat ECMO, rreziku është i madh قالب:LL. Ora News. March 12, 2020.
- ^ Голикова заверила, что медики в РФ готовы к любому развитию ситуации с COVID-19 قالب:LL. Department of health of Moscow. March 16, 2020.
- ^ НОВАЯ ИНФЕКЦИОННАЯ БОЛЬНИЦА СМОЖЕТ ПРИ НЕОБХОДИМОСТИ ПРИНЯТЬ ДО 500 ЧЕЛОВЕК قالب:LL. Department of health of Moscow. March 13, 2020.
- ^ "Свободны 400 аппаратов": в Смольном опровергли дефицит ИВЛ в Петербурге قالب:LL. Department of health of Moscow. April 12, 2020.
- ^ "国内の病院における人工呼吸器等の取扱台数推計値" [Estimated number of ventilators handled in domestic hospitals] (PDF). Japanese Association for Acute Medicine. مايو 2020.
- ^ 疫情关键时刻救命的ECMO:全国只有400台 为何这么少? قالب:LL. Sina Corp. February 10, 2020
- ^ Larsson M, Rayzman V, Nolte MW, et al. (يناير 2014). "A Factor XIIa Inhibitory Antibody Provides Thromboprotection in Extracorporeal Circulation Without Increasing Bleeding Risk". Sci. Transl. Med. 6 (222): 222. doi:10.1126/scitranslmed.3006804. hdl:10616/42281. PMID 24500405.
- ^ MohanKumar K (فبراير 2014). "Intestinal epithelial apoptosis initiates gut mucosal injury during extracorporeal membrane oxygenation in the newborn piglet". Lab. Invest. 94 (2): 150–60. doi:10.1038/labinvest.2013.149. PMC 3946757. PMID 24365747.
- ^ Magliocca, JF; Magee, JC; Rowe, SA; Gravel, MT; Chenault Rh, 2nd; Merion, RM; Punch, JD; Bartlett, RH; Hemmila, MR (2005). "Extracorporeal support for organ donation after cardiac death effectively expands the donor pool". The Journal of Trauma. 58 (6): 1095–101, discussion 1101–02. doi:10.1097/01.ta.0000169949.82778.df. PMID 15995454.
{{cite journal}}: CS1 maint: numeric names: authors list (link)
وصلات خارجية
- American Thoracic Society, Patient Education: What is ECMO? (Online-PDF)
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- مقالات بالمعرفة بحاجة لذكر رقم الصفحة بالمصدر from November 2012
- CS1 maint: unflagged free DOI
- CS1 maint: url-status
- Articles with dead external links from July 2020
- CS1 maint: numeric names: authors list
- Short description is different from Wikidata
- Use mdy dates from May 2012
- Articles with unsourced statements from April 2015
- Articles to be expanded from March 2020
- All articles to be expanded
- Articles with hatnote templates targeting a nonexistent page
- Portal-inline template with redlinked portals
- Pages with empty portal template
- طب العناية المركزة
- معدات طبية
- تقانة الأغشية