مضاد حيوي
مضاد حيوي بالإنجليزية Antibiotic ، هي مواد عضوية تنتجها الكائنات الدقيقه كالبكتيريا و الفطريات اثناء نموها وهي قادره بتركيز منخفض ان تبيد او تهبط نمو الكائنات الدقيقه غير الكائنات التي أنتجتها.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
تعريف
الصادات أو المضادات الحيوية أو المرديات antibiotics مواد تثبط نمو بعض الأحياء المجهرية التي تدخل فيها، فتسبب اضطراباً في استقلابها metabolism أو تؤدي إلى تلفها.
اقتصرت حدود الصادات في البدء على مواد من منشأ حيوي تنتجها الفطور mycoses، ثم اتسع هذا المفهوم حتى أصبح يشمل أجساماً تنتج تركيبياً ولها التأثير المضاد للجراثيم نفسه. وتصنف الصادات وفق مجموعات تبعاً لتركيبها الكيماوي، وطريقة تأثيرها في الأحياء المجهرية، وانتشارها في البدن، وآثارها السريرية، وطريقة طرحها: اللكتمينات بتاbeta lactamin وهي أنواع البنسلينات والأمينوزيدات aminosides والفنيكولات phenicols والتتراسكلينات tetracylins وعديدات الببتيد polypeptides والمكروليدات macrolides والريفاميسينات rifamycines والببتيدات السكرية glycopeptides والنيتروإميدازول nitroimidazoles ومشتقات الأكسي كينولين oxyquinoleineومضادات التدرن ومضادات الفطريات ومضادات الانقسام الخلوي antimitotics.
نبذة تاريخية
على مدى أكثر من 2500عام، ظل الناس يعالجون بعض الأخماج الجلدية باستعمال الفطريات العفنية، التي تكون المضادات الحيوية. غير أن الدراسة العلمية الحديثة لهذه المواد لم تبدأ إلا في أواخر القرن التاسع عشر الميلادي. في ذلك الوقت، اكتشف الكيميائي الفرنسي لويس باستير، أن البكتيريا تنشر الأمراض المعدية. ثم طور عالم البكتيريا الألماني روبرت كوخ طرق فصل وتحضير مختلف أنواع البكتيريا. وقد تعرف كوخ أيضًا على بكتيريا معينة تسبب أمراضًا معينة.
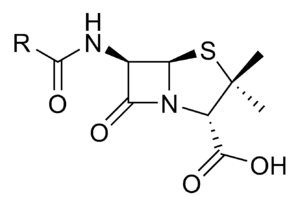
البنسلين أصبح أول مضاد حيوي فعال. تم الحصول عليه من عفن البنيسليوم عن طريق عمليات تنقية وبلورة. وتوضح هذه الصورة الفوتوغرافية الشكل المجهري لفطر بنيسليوم.
بدأ العلماء بعد ذلك في العمل على إيجاد أدوية لها القدرة على تدمير الأحياء المجهرية الممرضة، ولكن ثبت أن المواد التي أنتجوها إما عديمة الفاعلية أو ضارة. وجاء الكشف العلمي التاريخي عام 1928م، حينما لاحظ عالم البكتيريا البريطاني ألكسندر فليمنج أن فطرًا عفنيًا من جنس بنيسليوم، ينتج مادة تدمر البكتيريا. وأطلق على هذه المادة اسم البنسلِّين. تعرف فليمنج على إمكانية استعمال البنسلين في علاج المرض، ولكن صعوبة استخلاصه من الفطر العفني، حالت دون إجراء المزيد من التجارب.
وفي أواخر الثلاثينيات استحدث العالمان البريطانيان، إيرنست تشين وهوارد فلوري، طريقة لاستخلاص وتنقية كميات قليلة من البنسلين. وفي عام 1941م، تحقق أول علاج طبي ناجح بالبنسلين، حينما تناول الدواء رجل شرطة بريطاني، كان يعاني من حالة تسمم بكتيري في الدم. وفي عام 1943م، تم اكتشاف نوع من عفن البنسلين، يعطي إنتاجًا وفيرًا، ومن ثم زاد إنتاج البنسلين زيادة كبيرة.
وفي أوائل الأربعينيات، اختبر عالم الكيمياء الأمريكي سلمان واكسمان نحو عشرة آلاف نوع من بكتيريا التربة، وذلك من أجل التوصل إلى مضادات حيوية فعالة. وفي عام 1943م، اكتشف واكسمان أن بعض ميكروبات المتسلسلة، وهي نمط من الفطريات، تنتج مادة لها خواص المضاد الحيوي القوي. ونتج عن بحثه مضاد حيوي جديد، أطلق عليه اسم ستربتومايسين. وبالرغم من أن آلاف المضادات الحيوية قد وجدت في الطبيعة أو أنتجت كيميائيًا، إلا أن قليلاً منها ثبت أنه مأمون وفعال. كما ثبت إضافة إلى ذلك، أن بعض الأنماط من الأحياء المجهرية الممرضة، قد اكتسبت مقاومة ضد بعض المضادات الحيوية
إكتشاف المضاد الحيوي
حين بدأ البحث العلمي عن دواء فعال ضد الزهري ، تم منذ ذلك التاريخ اكتشاف العديد من الأدوية الفعالة ضد معظم الامراض الناجمه عن البكتيريا و الطفيليات وحيدة [الخليه] وكان اهم هذه الأدوية السلفونامايدات ثم المضادات الحيويه وهي مواد عضويه تنتجها الكائنات الدقيقه كالبكتيريا و الفطريات اثناء نموها وهي قادره بتركيز منخفض ان تبيد او تهبط نمو الكائنات الدقيقه غير الكائنات التي انتجتها. وكان البنسلين هو اول اكتشاف في عالم المضادات الحيويه وكان عام 1929 م وقد توسع التعبير ليشمل المواد المشتقه التي تنتج بالتخليق جزئيا اوكليا وهناك بعض المضادات الحيويه الفعاله ضد انواع الاورام الخبيثه كالبكتريا و الفيروسات و الحيونات الاوليه . مضادات واسعة المفعول (broad spectruim) ,ومنها الامبيسلين و الكلورامفينكول و التتراسيكلين وهي مفيدفي علاج الانتانات المختلطه ( mixed infection) . واخرى تسمى مضادات ضيقة المفعول (narrow spectrum) مثل البنسلين و الاريثرومايسين.
آلية تأثير الصادات
تؤثر الصادات في الجراثيم في جهة منها أو أكثر، فيمكنها أن تمنع تركيب غشائها الخلوي كما تفعل البنسلينات، في حين يؤثر بعضها الآخر في النواحي الوراثية فيمنعها من تركيب الدنا DNA. ويكون تأثير قسم منها كالمكروليدات والفنيكولات على تركيب البروتينات في حدود الريباسات ribosomes. وتفعل الصادات عديدات الببتيد في الغشاء الهيولي. ويكون تأثير الصادة بتثبتها على جزيء مما يحول دون قيامه بوظيفته. وهناك صادات ذات بنية تماثل بنية أحد العوامل الأساسية في الجرثوم، فتحل مكانها وتنهي عملها الاستقلابي.
التأثيرات الثانوية للصادات
تصنف التأثيرات الثانوية التي تنجم عن الصادة نفسها إلى أرجية allergic وسُمّية ومتنوعة، تعود إلى التغير الجرثومي.
تشاهد التأثيرات الأرجية في الصادات كلها ولاسيما في اللكتمينات بيتا والسلفاميدات. ولتربة المريض دور كبير في ذلك إذ غالباً ما تلاحظ الأرجية في أكثر من صادة من مجموعة واحدة حينما يكون المريض مصاباً بأحدها، وتزداد شدة الأرج في كل معالجة جديدة، وتكون الأعراض إما جلدية تتظاهر بحمامات أو حكة، أو عامة فتسبب صدمة shock خطرة، أو تبدو على هيئة آلام مفصلية أو بيلة بروتينية أو آفة كلوية. وقد تكون هذه التأثيرات الثانوية دموية، فتسبب فقر دم انحلاليّاً بالمناعة الذاتية، أو نقصاً في الكريات البيض.
وتعود التأثيرات السمية إلى المقادير التي يتناولها المريض كاستمرار المعالجة وحالة تربته ووظائف بعض أجهزته (كالكليتين والكبد وغيرها)؛ فبعضها يسبب نقصاً في الكريات الحمر، وينجم عن بعضها الآخر اضطراب في تكديس الصفيحات الدموية. وهناك الصادات التي تؤثر في قوقعة الأذن ودهليزها، والصادات التي تسبب اختلاجات، والصادات التي تسبب التهاب العصب الصدغي وارتفاع الضغط داخل القحف واضطرابات في النوم.
ومن النتائج السمّية لبعض الصادات تأثيرها في الكبد والجهاز الهضمي وإحداثها غثياناً وإقياءً وآلاماً معدية.
ومن التأثيرات المتنوعة: الآلام المفصلية والعضلية، والتحسس للضياء التي أكثر ما تشاهد في التترسكلينات والكينولونات.
وهناك بعض الطوارئ التي تنشأ عن الجراثيم نفسها بانحلالها بعد أخذ مقادير كبيرة من الصادات دفعة واحدة مما يسبب وهطاً collapse، وهذا ما كان يحصل في الإصابات التيفية الشديدة بعد تناول المريض مركبات الفينيكول. وقد دفع هذا لإعطاء الصادات في مثل هذه الحالات بمقادير متدرجة. ومن الطوارئ الكثيرة المشاهدة إصابة المريض بفطور في الجهاز الهضمي (غالباً ما تصيب الفم والمري) عند المصابين بتدني المناعة، وغالباً ما ترى هذه الحالة حين استعمال اللكتمينات بيتا والسيكلينات، كما يمكن أن تسبب الصادات التهاب الأمعاء ذات الغشاء الكاذب، وتلاحظ هذه في معظم الصادات، وسببها تكاثر جراثيم لا هوائية في لمعة الأمعاء. كما يمكن للصادات أن تسبب ظهور ذراري strains مقاومة لعدة صادات في وقت واحد، وغالباً ما يرى ذلك في المشافي حين إعطاء الصادات بهدف وقائي.
عمل المضادات الحيوية
إن المضاد الحيوي منه مايهبط نمو البكتريا ( Bacterio static) وذلك بتاثيره على النمو بمنع التخليق الحيوي لبروتينات الخليه واحماضها النووية.
ومنه مبيد للجراثيم ( Bacterioidal) وذتك بمنع تكوين جدار الخليه او غشائها السيتوبلازمي(الهيولي cytoplasm) وقد يؤثر المضاد موقفا للنمو بجرعته الادنى ومبيد بجرعته الأعلى ويعتمد استمرار المفعول على الجرعه المناسبه وكذلك نفاذية المضاد الحيوي الى الانسجه.
لذا فإنه يفضل قبل البدء في المعالجه فحص حساسية الجرثوم للمضادات الحيويه لاستعمال المضاد المؤثر في المرض المعالج.
التأثيرات الجانبية المرتبطة بتربة المريض
يُفضَّل، إذا كان المريض مصاباً بقصور كلوي، الابتعادُ عن الصادات المعروف عنها أنها ذات تأثير سٌمي على الكليتين كالأمينوزيدات، ولابد للمرأة الحامل أن تبتعد عن تناول بعض الصادات ذات الأثر المشوه للجنين، ولاسيما في الأشهر الثلاثة الأولى. وهناك بعض الصادات التي يجب ألا تتناولها الحامل طوال مدة حملها كالتتراسكلينات والأمينوزيدات والسلفاميدات والكينولونات.
كما يجب عدم إعطاء بعض الصادات كالبنسلين بروكائين والكلورامفنيكول والسكلينات والكينولونات والريفامبسين والنيوميسين للخُدَّج والولدان. ولابد عند الشيوخ من الابتعاد عن الصادات السامة للكليتين.
طوارئ تعود إلى طريق إعطاء الصادة
يمكن للصادات التي تعطى عن طريق الزرق العضلي أن تشكل في موضع الإعطاء لويحة قاسية أو خراجا،ً كما يمكن أن تسبب الصادات التي تعطى عن طريق الوريد تخريشاً موضعياً أو التهاب وريد خثارياً.
مقاومة الجراثيم للصادات
لكل مادة طيف action spectrum، ويعني طيف الفعالية الأنواع الجرثومية التي تتحسس بهذه الصادة فتَتَثبط، حينما تكون الصادة بتركيز معين في الجسم الحي in vivo إن أعطيت بالمقادير المعيارية standard.
وحينما يقال: طيف الفعالية، فإن ذلك يدل على أن الأنواع الجرثومية غير الحساسة تقاوم هذه الصادة مقاومة طبيعية، وترجع هذه المقاومة إلى الصفات الوراثية لنوع الجرثوم.
إن آليات هذه المقاومة الطبيعية عديدة منها: عدم دخول الصادة إلى الجرثوم، وتعذر وجود هدف جزيئي molecular لفعل الصادة، وإنتاج الجرثوم لأنزيمات تُبطل فعل الصادة.
ولكن استعمال الصادات قد أسهم في حدوث عملية اختيار لذرار مقاومة تقع ضمن النوع الذي يتحسس بها عادة. وهذا نمط آخر من المقاومة، ويوصف بأنه مقاومة مكتسبة. وهذه المقاومة المكتسبة تدفع إلى معرفة الذراري المقاومة بغية انتقاء الصادة التي تؤثر فيها حين المعالجة.
من الناحية الجرثومية تصبح الذرية الجرثومية مقاومة حينما تستطيع التكاثر على الرغم من وجود تركيز أعلى من التركيز الذي يثبط عادة الذراري الأخرى التي ما زالت تتحسس بهذه الصادة. وهناك عدة آليات تؤثر في هذه المقاومة المكتسبة منها التوضع الجيني.
ويمكن تلخيص شروط فعالية صادة ما على النحو التالي:
دخول الصادة، وإيجادها الجزيء الهدف لفعلها، ووصولها بشكلها الفاعل إليه، وبقاؤها على تماس مع هذا الهدف وبتركيز كاف.
وقد تعود آليات المقاومة المكتسبة إلى مخالفة أي شرط من الشروط السالفة الذكر؛ كعدم دخول الصادة بسبب نقصان (أو انعدام) نفوذية جدار الجرثوم، أو نقصان نفوذية أغشيته، وتخرب الجزيء الهدف بتغير جهة التثبيت، أو بحدوث تدرك degradation أنزيمي في الهدف. وخروج الصادة بكمية كبيرة من الجرثوم، مما ينتج منه تركيز غير كاف للصادة فلا تؤثر في منطقة الهدف. وقد تتدمر الصادة بالحلمهة hydrolysis كما يفعل إنزيما البنسليناز والسيفالوسبوريناز مع اللكتمينات بيتا، أو تتغير بناها الكيمياوية، وهذه الأنزيمات التي تعطل فعل الصادات عديدة جداً.
إن الدنا DNA هو الحامل الوراثي للمقاومة، ويشاهد في بنيات عديدة في الجراثيم: في الصبغي chromosome، وفي البلسميدplasmid، والبلسميد هو قطعة دنا تقع خارج الصبغي، وغالباً ما توجد في هيولى الجرثوم وهي تتنسخ ويمكن أن تنتقل لجرثوم آخر.
كما يمكن أن تُكتسب المقاومة بظهور طفرة صبغية، أو باكتساب معلومات تأمر بمقاومة الصادة عن طريق انتقال بلسميد من جرثومة مقاومة إلى جرثومة حساسة، ويمكن للطفرة أن تصيب الجين gene الذي يراقب دخول الصادة، أو بنية الهدف الذي ترمي إليه الصادة. ولا تصيب الطفرة إلا صفة واحدة، ولكن إذا تعلق الهدف بعدة صادات من فصيلة واحدة، حينئذٍ تشمل المقاومة مختلف مركبات هذه الفصيلة.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
اختبار وإنتاج المضادات الحيوية
كيفية إنتاج المضادات الحيوية ينتج صناع الدواء ملايين الأطنان من المضادات الحيوية سنويًا، وتختلف عمليات الإنتاج باختلاف الشركات. وعلى أية حال، فإن بعض الشركات تستخدم العملية الموضحة أدناه. تجري الشركات اختبارات موسعة أثناء الإنتاج وبعده، وذلك للتأكد من أن المضادات الحيوية مأمونة الجانب وفعالة.
الاختبار. يختبر العلماء، في كل عام، الآلاف من المواد الميكروبية الطبيعية والمواد المحورة كيميائيًا، لإمكانية استعمالها مضادات حيوية. ففي البداية، تختبر هذه المواد ضد الأحياء المجهرية الممرضة التي يتم تحضيرها في أنابيب اختبار أو في أطباق مختبرية.
والمادة التي تبدي فعالية قوية ضد الأحياء المجهرية الممرضة، يتم اختبارها على نطاق واسع، باستخدام حيوانات التجارب. وإذا لم تحدث آثار ضارة في الحيوانات، يجرب المضاد الحيوي على البشر. وفي المملكة المتحدة، لابد أن توافق وكالة الرقابة الدوائية، على إجراء الاختبارات على الإنسان. فإذا ثبت أن الدواء أكثر أمانًا وفاعلية من المضادات الحيوية المستعملة من قبل، فإنه يعرض على وكالة الرقابة الدوائية للموافقة. وفي النهاية، إذا وافقت الوكالة على المضاد الحيوي، تبدأ شركات الأدوية في إنتاجه تجاريًا.
الإنتاج. وهو يشمل عدة خطوات. تحضر أولاً مزارع من الأحياء المجهرية المنتجة للمضاد الحيوي في قوارير، ثم تنقل محتويات هذه القوارير بعد ذلك إلى أوعية كبيرة للتخمر. انظر: التخمر. وتتكاثر الأحياء المجهرية سريعًا في الأوعية الكبيرة حيث توجد بيئة مناسبة لتنشيط نموها، وتستخلص مادة المضاد الحيوي من المزرعة بعد التخمّر وتنقى. وتحوَّر بعض المضادات الحيوية كيميائيًا لإنتاج مضادات حيوية شبه اصطناعية. وفي الواقع، فإن كثيرًا من هذه الأدوية تكون أكثر فاعلية من المضادات الحيوية الطبيعية التي جاءت منها.
التقنية الحيوية
تولى صناع التقنية الحيوية قدرا كبيرا من نشاطها الى اكتشاف عقاقير جديدة ، ومن إحدى هذه العقاقير تأتي المضادات الحيوية. ويوجد هناك ثلاث طرق لتطوير المضادات الحيوية (بالإضافة إلى تطوير المضادات الحيوية الحالية) عن طريق العناصر التقني حيوية. ومعظم المضادات الحيوية الموجودة حاليا هي إما من الأنواع التخليقية أو شبه التخليقية – ومن النادر تماما أن يتم إكتشاف مضاد حيوي بحالة طبيعية من الطبيعة.[1]
والمضادات الحيوية الحالية وخصوصا البنسلين، كانت أول منتجات الصناعة الدوائية، والتي تعتبر الآن منتجا من منتجات التقنية الحيوية. والتي يتم انتاجها بواسطة الفطريات في أجهزة التخمير. والبنسيلينيات والأستربتوميسينات، وحشد كبير من المضادات الحيوية، التي غزت الأسواق في فترة الأربعينيات والخمسينيات، لا تزال المنتاج الرئيسية لصناعة التخمير. ومنذ ذلك الحين، فقد أسس علماء التقنية الحيوية على هذه القاعدة وقاموا بتطوير سلسلة من المضادات الحيوية الجديدة.
1- المضادات الحيوية المهجنة: إن تخليق المضاد الحيوي، هو نتيجة عدد من المراحل الإنزيمية داخل بكتريا أو فطر معين. وتتجه بعض الأبحاث الحالية إلى إنتاج المضادات الحيوية المهجنة – وهي الجزيئات التي تتكون من أجزاء صغيرة من مضادين حيويين مختلفين، ويتم هذا بوضع الإنزيمات المختارة من خليتين منتجتين للمضادات الحيوية داخل بكتريا واحدة. وقد تطور هذا العمل بعد ذلك باستخدام الأستربتوميسينات المهندسة وراثيا.
2- الأيضيات الجديدة: ومن المتوقع أن يتم إنتاج المزيد من المضادات الحيوية بواسطة الكائنات العضوية الدقيقة والنباتات أكثر من تلك التي إكتشفها الإنسان حتى الآن. وتستخدم صناعة التقنية الحيوية إمكاناتها الهائلة في تنمية أنواع جديدة من البكتريا والفطريات بكميات كبيرة لفصل أنواع جديدة من البكتريا من أجل صنع المركبات التي لها أنشطة دوائية مفيدة. وتعتبر شركة كازانوفا متخصصة في هذا المجال.
3- الحيوان المضاد للبكتريا: والحيوانات على وجه الخصوص الحيوانات اللافقارية (التي ليس لها أجهزة مناعية معقدة مثل الثدييات)، تقوم بإنتاج سلسلة كبيرة من المواد التي تقتل البكتريا. ومعظم هذه المواد من البروتينات أو الببتيدات. وتبحث تقنية استنساخ الجين التقليدية، في إمكانية استنساخ جين لمثل هذه الببتيدات داخل البكتريا أو الخميرة التي تستطيع أن تنتج هذه المواد بكميات كبيرة. ويهتم علماء التقنية الحيوية بصفة خاصة بالبروتينات المنتجة عن طريق خلايا الجهاز المناعي. والتي تقوم بتدمير البكتريا الغازية بطرق طبيعية، والخلايا التي تنتج بروتينات الجهاز المكمل. وهي مجموعة البروتينات التي تحدث ثقوبا في الخلايا المصابة بالفيروس. وبعض من هذه الببتيدات لا تدمر الخلايا بنفسها. لكنها تعطي الفرصة لخلايا الدم البيضاء لكي تقوم بتدميرها (وتسمى هذه العملية بعملية الحصاد OPSONIZATION . وهناك طرق أخرى مثل الببتيدات المدافعة، والمسامية البكتيرية التي تزيد البروتين، ببتيدات البكتنسين، أزوروسيدين، وإنزيم اللايسوزيم الذي يقوم فعلا بقتل الخلايا البكتيرية. وهناك مجموعة ثالثة، تعرف باللكتوفيرن التي تعوق النمو البكتيري عن طريق التخلص من الحديد الحر الذي تحتاجه هذه البكتريا من البيئة المحيطة بها. وتربطه بشكل معقد يصعب الوصول إليه.
كيفية وشروط استخدامها
المضادات الحيويه هي مواد عضويه تنتجها الكائنات الدقيقه كالبكتريا و الفطريات فيجب عند الاستخدام ان نستخدمها الاستخدام الصحيح لانها قد تضر:
- يجب قبل البد في المعالجه عمل زراعه للجرثومه المسببه للمرض لمعرفة المضاد المؤثر لها.
- يجب استخدام المضاد الحيوي حتى الشفاء كاملاً وغالبا في الاصابات البسيطه من5ايام_7أيام حتى لايحدث عند المكروب مناعه من الدواء المستخدم.
- مراعات مدة تاثير الجرعه فالبعض يكون كل 6ساعات والبعض كل 8ساعات هذ بالنسبه للدواء الذي يوخذ عن طريق الفم وهي قصيرة المفعول.
النتائج السريرية
توجد الجراثيم المقاومة بين الجراثيم المتحسسة قبل تناول أي دواء. وحينما تؤخذ الصادة فإن فعلها هو كفعل عامل انتقاء للجراثيم المقاومة بين المجموعة المتحسسة، أي إنها تقضي على الجراثيم المتحسسة وتُبقي المقاومة. ومن الممكن اتقاء خطر ظهور طافرات مقاومة (أو إنقاص نسب حدوثها على الأقل) بإعطاء معالجة تضم صادتين من فصيلتين مختلفتين.
المقاومة باكتساب جينات
تم وصف هذا النوع من المقاومة للمرة الأولى عام 1955 في اليابان أثناء وباء بزحار عصوي bacillus dysentery سببته شيغلات فلكسنري Shigella Flexneri. فظهرت مقاومة في وقت واحد للستربتوميسين والكلورامفنيكول والتتراسكلين والسلفاميدات. ولا تفسر هذه المقاومة بعملية انتخاب للطافرات المقاومة، لأن معالجة المصابين جرت بصادة واحدة فقط. وقد شوهدت في براز المرضى جراثيم الإشريكيات القولونية Escherichia coli التي قاومت الصادات نفسها، مما دعا إلى وضع فرضية إمكان انتقال المقاومة بين الجراثيم ذاتها. وقد تم البرهان العملي على هذه الفرضية مخبرياً. إن المقاومة المتعددة والمكتسبة تنتقل كتلة واحدة (المقاومات جميعها معاً) من جرثوم يتصف بهذه المقاومات إلى جرثوم آخر كان حساساً لها وبوساطة بلسميد.
إن الجينات التي ترمِّز encode المقاومات المتعددة تتوضع في البلسميد، ولذا فإن صفات هذا النمط مرتبط بالصفات العامة للبلسميد.
وهكذا تستطيع الجرثومة الواحدة أن تجمع عدة معلومات تأمر بالمقاومة عن طريق آلية اكتساب «دنا» يقع خارج الصبغي (أي بلسميد)، فيصبح من المتعذر معالجتها بالصادات. وتصيب المقاومة الناجمة عن البلسميدات معظم الصادات، كما تستطيع الأنواع الجرثومية كلها أن تُسكن بلسميدات.
ينتقل البلسميد بين الجراثيم التي هي من أنواع مختلفة، وحتى بين مجموعات جرثومية بعيدة جداً بعضها عن بعض. وللعصيات سلبية الغْرام النسبة الأولى في انتقال البلسميدات، وبهذه الآلية، وعلى مر السنين، اكتسب العديد من الأنواع الجرثومية خواص مقاومة. وهذه الصفة تثير القلق في المستشفيات خاصة لأن الجراثيم المقاومة المقيمة فيها تتبادل العناصر الوراثية بسهولة فائقة.
هناك جراثيم لم تكتسب ذراريها مقاومة كبيرة، وبقي تحسسها بالصادات على نحو يشبه ما كانت عليه في السابق، كالعقديات المقيحة (العقديات A) والعقديات الرئوية والنيسريات السحائية والبروسيلات. لكنّ هناك أنواعاً أخرى ازدادت فيها نسب الذراري المتعددة المقاومة ازدياداً كبيراً كما هو الأمر في العنقوديات والعصيات السلبية الغرام. لقد سبب هذا التغير تجاه التحسس بالصادات تغيرات في أسباب الأمراض الخمجية وفي مظاهرها السريرية. وتناقصت نسبة الأمراض الخمجية التي كانت الشغل اليومي الشاغل لبعض الأقسام في المستشفيات، كالحمى الرثوية، والحمى القرمزية scarlatina، والخناق diphtheria. وحدث نقيض ذلك في أمراض خمجية أخرى، فقد ازدادت نسبة الإصابات بالجراثيم الانتهازية ذات المنشأ المطاعم commensal والتي كانت تشكل جزءاً من نبيت flora الجلد والأغشية المخاطية، كالعنقوديات والمكورات المعوية والعصيات السلبية الغْرام. والأسوأ من ذلك مشاهدة أخماج بجراثيم ممرضة انتهازية من منشأ رمّام saprophyte، أي من النبيت الجرثومي للوسط الذي نعيش فيه. فالأمراض الناجمة عن هذه الجراثيم كانت مجهولة في الطب البشري، وهذه الجراثيم قادرة على مقاومة العديد من الصادات. وأكثر ما تشاهد الإصابات بها في المرضى الذين يخضعون لتقنيات معقدة حديثة في مراكز الإنعاش، وتعد تربة هؤلاء وسطاً ملائماً لتكاثر هذه الجراثيم. وقد أصبح اللجوء إلى المخبر لدراسة حساسية الذرية الجرثومية المسببة للمرض ضرورة ملحة.
طرق دراسة المخابر لفعالية الصادات
بسبب وجود حوادث «مقاومة مكتسبة» تجري عن طريق الطفرات أو باكتساب بلسميد، لا يمكن انتقاء معالجة بالصادات استناداً إلى الطيف النظري وحده لهذه الصادات، فالاستعانة بالمخبر ضرورة في أحوال عديدة لتوجيه الوصفة الدوائية أو تعديلها. ولا بد للتوصل إلى ذلك من استفراد الذرية الجرثومية التي سببت الحالة الخمجية؛ وباستفرادها يستطيع المخبر أن يحدد بدقة الصادات التي تُحسس الجرثوم المسبب عن طريق زرعه في الزجاج in vitro، والإرشاد إلى المقادير التي تؤثر فيه، ويحول الطبيب ذلك إلى ما يكافئ هذه المقادير حين استعمالها في الحي in vivo. فيتعرف الصادات التي تثبط نمو هذا الجرثوم، أي التأثير الكابح للجراثيم bacteriostatic أو الصادات التي توقف انقسامها وتكاثرها، كما يستطيع أن يتعرف من بين الصادات الفعالة في كبح تكاثر الجراثيم، على الصادات التي تستطيع أن تميت تلك الجراثيم أي ذات التأثير المبيد للجراثيم bactericide الذي يُقدر بدراسة التركيز الأدنى الذي يسبب القضاء النهائي على الجرثوم، كما يمكن تعرف الصادات التي، إن تمت مشاركتها معاً، استطاعت أن تكوِّن تأثيراً مبيداً للجراثيم.
التفسير السريري
إن مقابلة التركيز الأدنى المثبط مع خصائص الحرائك الدوائية pharmacokinetics للصادات، يسمح بتصنيف الجرثوم الذي تمت دراسته في أحد الزمر التالية:
حينما يكون تركيز الصادة، التي تستطيع أن تثبط نمو الجرثوم في الزجاج، عالياً لا يمكن التوصل إليه في الحي مهما يكن طريق إعطاء الصادة، حينئذٍ توصف هذه الذرية الجرثومية بأنها «مقاومة». وتنتهي نتيجة المداواة بهذه الصادة بإخفاق المعالجة. ولكن حينما يكون تركيز الصادة المثبط للنمو في الزجاج أدنى من التركيز الذي يمكن الحصول عليه في الحي حين إعطاء مقادير دوائية مألوفة، فإن هذا الجرثوم «حساس» sensible سريرياً، ويمكن القضاء عليه بمداواته بتلك المقادير. وإذا وقع التركيز الأدنى المثبط بين هاتين الحالتين (القيمتين) وصفت حساسية الجرثوم بأنها «متوسطة». وفي مثل هذه الحالة لا يتم القضاء على الجرثوم إن أعطيت الصادة بالمقادير المألوفة، ولكن يمكن القضاء عليه بإعطاء معالجة بالطريق العام وبمقادير عالية إن أمكن ذلك أو بالطريق الموضعي، أو بالطريق العام، إذا كان الخمج متوضعاً في أجهزة فيها تركيز الصادة مرتفع بصورة فيزيولوجية (البول، الصفراء).
التقنيات بالانتشار في الأوساط الزرعية الصلبة
إن طريقة «الأقراص» هي أقدم تقنية، وتجري كما يأتي: تفرش الذرية الجرثومية المراد دراستها على مستنبت غراء agar، ويتألف مصدر الصادات من أقراص من ورق النشاف مشربة كل واحدة منها بمقدار معروف من صادة معينة، وتوضع هذه الأقراص على سطح الغراء المزروع، ثم تحضن العلبة بكاملها بحرارة 37درجة مدة 18ساعة، فتظهر مناطق لا تنمو فيها الجراثيم حول القرص الذي يحتوي صادة تثبط نمو الجرثوم. وقد تكون هذه المنطقة كبيرة أو صغيرة. والواقع أن تكاثر الجراثيم يتوقف حينما تلاقي في الغراء تركيزاً للصادة يساوي التركيز الأدنى المثبط. ولذا فإن قياس قطر المنطقة يعكس قيمة التركيز الأدنى المثبط للصادة، وحسب اتساع القطر أو صغره تصنف الصادة، وتعرف فيما إذا كانت الجراثيم تجاهها متحسسة أو مقاومة أو متوسطة الحساسية.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التقنيات بالتمديد في وسط سائل
هناك أجهزة آلية ترتكز على أوساط زرعية سائلة تحوي صادات تسمح بمعرفة التأثير المثبط لصادة في النمو الجرثومي. وقد يجري التقدير مباشرة بقياس العكر turbidimetry أو قياس الكَدَر nephelometry، أو بشكل غير مباشر بقياس النشاط الأنزيمي، أو إنتاج CO2، أو المقاومة الظاهرية الكهربائية impedance. وهناك قارئات آلية متصلة بحاسوب، تستطيع جمع النتائج وطبعها على ورقة. ومن الأجهزة ما يستطيع أن يعطي النتائج بعد عدة ساعات فقط.
مشاركة الصادات
هناك عدة أسباب تدعو في بعض الحالات إلى تطبيق مشاركة بين الصادات هي:
ـ توسيع طيف التأثير: وهي إما حالة مواجهة خمج يرجح أن سببه عدة جراثيم، كبعض الأخماج التنفسية والنسائية والهضمية؛ أو حالة تستدعي فيها الإصابة معالجة إسعافية كما يحدث عند ذوي المناعة المتدنية.
يضاف إلى ما سبق الحصول على تأثير مبيد أشد (فعل تآزري synergetic بين الصادتين) في الجرثوم المسبب للحالة الخمجية الوخيمة مما لو أعطي صادة واحدة. ويمكن القول إن هذا هو الاستطباب الرئيسي لإعطاء أكثر من صادة واحدة في وقت واحد.
الطرق الجرثومية لمراقبة المعالجة بالصادات
إن الشرط اللازم لتكون الصادة فعالة في الحي in vivo هو وصولها إلى بؤرة الخمج بتركيز فعال.
ومن الممكن للمخبر أن يجري فحوصاً تؤكد جدوى المعالجة المعطاة. يؤخذ النموذج الأول مباشرة قبل إعطاء الجرعة الدوائية، ويؤخذ النموذج الثاني بعد نصف ساعة من إعطائها إذا كانت تعطى وريدياً، وبعد ساعة إذا كانت تعطى عضلياً، وساعتين إذا كانت تعطى فموياً.
وهناك عدة طرق تقنية جرثومية تستعمل لمعايرة الصادات الحيوية. بيد أن التقنيات غير الجرثومية كالتي تستند إلى الدراسة المناعية الأنزيمية، وإلى الاستشراب chromatography، تعطي نتائج في زمن أقصر، وهذه الطرق سريعة الإنجاز ودقيقة.
ولا بد من الإشارة إلى أن هناك بؤراً لا تستطيع الصادات أن تدخلها، أو أن فعل الصادات ضعيف فيها كالبؤر المتكيسة، والمجامع القيحية، وغير ذلك.
طرائق إعطاء الصادات
تشمل مشكلة إعطاء الصادات ناحيتين: أولاهما معالجة خمج ظاهر، وثانيتهما استعمال الصادات وقائياً. ولا بد من مواجهة المراحل التالية أمام كل حالة خمجية: استطباب المعالجة، واختيار الصادة، وتحديد المقادير الدوائية، وطريق إعطاء الدواء، ومراقبة المعالجة، ومدة بقائها، وزمن إيقافها.
لاتبيح سميّة بعض الصادات، وإن كانت نسبة الطوارئ الناجمة عنها ضعيفة نسبياً، تعريض المريض لخطر لا فائدة منه. ولذا فإن القرار الذي يتخذ بوصف المعالجة بالصادات يجب أن يرتكز على معلومات توصّل إليها من الفحص السريري والفحوص الجرثومية التي أدت إلى وضع تشخيص دقيق، أو على الأقل فرضية تشخيص مرجحة.
ويجب أن يستند انتقاء الصادة إلى ثلاثة معطيات هي: نوع الجرثوم المسبب وحساسيته للصادة، وموضع الخمج، وحالة المريض.
ويكون الاختيار من بين الصادات الأكثر فعالية، تلك التي، بحكم خصائص حرائكها الدوائية، تستطيع أن تصل إلى البؤرة الخمجية بتركيز كاف.
يختلف انتشار الصادات في النسج والأجهزة اختلافاً كبيراً ويرجع ذلك إلى نوع الصادة نفسها، فبعضها ذات تركيز شديد في البول، وأخرى في الصفراء، وبعضها في السائل الدماغي الشوكي إلى غير ذلك.
ولكن قد لا تسمح حالة المريض باستعمال بعض الصادات الفعالة نظراً إلى بعض خصائصها السُّمية أو للأخطار السمية التي يمكن أن تتفاقم نتيجة إصابته بقصور في جهازٍ من أجهزته، كأن يكون مصاباً بقصور كلوي أو آفة كبدية أو غير ذلك.
سبب إخفاق المعالجة بالصادات
هناك حالات تبدو فيها المعالجة غير مجدية سريرياً، مع أنها فاعلة في الزجاج. وفي مثل هذه الحالات يجب إعادة الفحص الجرثومي للنماذج ومناقشة الحالات الآتية:
- نقص في المقادير المعطاة، مما ينجم عنه قصور في مقدار الصادة في الدم والنسج.
- مثابرة بقاء البؤرة الخمجية نظراً إلى مكان توضعها، أو تبعاً لبنيتها التشريحية اللذين لايسمحان بدخول الصادات بمقادير مجدية.
- خطأ في تقدير الجرثوم المسبب للخمج، أو ظهور مقاومة مكتسبة للجرثوم.
تقضي الأخطار السمية للصادات القيام بمراقبة شديدة، وعلى الخصوص في حالة إصابة المريض بقصور كلوي أو كبدي. وتجري المراقبة السريرية بتحرّي العلامات الأولى للأعراض الجانبية الخاصة بالصادة التي تم انتقاؤها للمعالجة كالدوار، والأعراض السمعية، والاندفاعات الجلدية، وظهور يرقان خفيف، وما إلى ذلك. ولكن يجب أن تجرَى إلى جانب هذه المراقبة السريرية فحوص مخبرية تتيح كشف العلامات الشاذة الأولى، كتعداد البيض والصيغة، ومعايرة البولة الدموية والكرياتنين، والبليروبين، وناقلات الأمين transaminases، والاختبارات القوقعية الدهليزية، وغيرها.
يجب أن توقف المعالجة دوماً دفعة واحدة، أي دون تخفيض المقادير تخفيضاً تدريجياً؛ لأن المقادير المستعملة في معظم الأحيان هي المقادير الدوائية التي تكون في حدودها الدنيا. ولذا فإن كل تخفيض يسبب نقصان كمياتها في الدم والنسج إلى حدود تقل عن حدود جدوى الصادة.
الوقاية بالصادات
إن الأخطاء التي ترتكب بإعطاء الصادات وقائياً كثيرة. ويجب التمييز بين إعطاء الصادات وقائياً من غير هدف محدد، وهذه الطريقة سيئة، وإعطاء الصادات وقائياً ولاسيما في الأقسام الجراحية ودواعي الإعطاء هنا محددة.
ولذا فإن إعطاء الصادات غير مسوَّغ إلا في حالات معينة وهي: وجود خطورة محددة بالإصابة بخمج كثير الظهور، وبوخامة الإصابة به، وبحساسيته المعروفة للصادات، وإمكان شفائه بإعطاء صادات معروفة التأثير فيه، فإن دواعي اللجوء إلى هذه الحالة قليلة في المجال الطبي؛ بيد أن نسبة وجود هذه الدواعي تزداد في المجال الجراحي.
أنواع المضادات الحيوية
يمكن تقسيم عمل المضادات الحيويه. مع اسماء الادويه:
- مضادات حيويه تعمل على جدار خلية البكتريا Bacterial cell wall. مثل:
- البنسلين.
- سيكلوسبرين.
- الباستراسين.
- الفانكوميسين.
- الرستوستين.
- مضادات حيويه تعمل على جدار السيتوبلازمي Cytoplasmic. membrane. مثل:
- البوليكسين.
- الجراسدين.
- الامفوترسين.
- النيساتين.
وهذه المضادات الحيويه تؤثر على خلية البكتريا وخلايا العائل ولذا فان لها تاثير ضار على الخليه.
- مضادات حيويه تعمل على تكون البروتينات داخل الخلية. مثل:
- التتراسكلين.
- الارثروميسين.
- النيوميسين.
- الكاناميسين.
- الباروميسين.
- مضادات حيويه تعمل على حمض النيوكليك (Nucleic acid). مثل:
- الرفيامبسين.
- لاكيتنوميسين.
وهذه المضادات تهبط تكون الدنا(D.N.A) ولذا فانه يمكن اعتبارهم مضادات للأورام(Cytotoxic Drugs) ، تتكون هذه المجموعه من الأدوية الأتية:
- الكاناميسين.
- النيوميسين.
- الباروموميسين(الهيماثين).
- الأميكاسين.
- الجنتاميسين.
- التوبراميسين(البنسن).
| الاسم العام | الأسماء التجارية | الاستعمالات الشائعة | الأعراض الجانبية المحتملة |
|---|---|---|---|
| Aminoglycosides | |||
| Amikacin | Amikin | Infections caused by Gram-negative bacteria, such as Escherichia coli and Klebsiella particularly Pseudomonas aeruginosa. Effective against Aerobic bacteria (not obligate/facultative anaerobes). | |
| Gentamicin | Garamycin | ||
| Kanamycin | Kantrex | ||
| Neomycin | |||
| Netilmicin | Netromycin | ||
| Streptomycin | |||
| Tobramycin | Nebcin | ||
| Paromomycin | Humatin | ||
| Ansamycins | |||
| Geldanamycin | Experimental, as antitumor antibiotics | ||
| Herbimycin | |||
| Carbacephem | |||
| Loracarbef | Lorabid | ||
| Carbapenems | |||
| Ertapenem | Invanz | Bactericidal for both Gram-positive and Gram-negative organisms via inhibition of cell wall synthesis and therefore useful for empiric broad-spectrum antibacterial coverage. (Note MRSA resistance to this class.) |
|
| Doripenem | Finibax | ||
| Imipenem/Cilastatin | Primaxin | ||
| Meropenem | Merrem | ||
| Cephalosporins (First generation) | |||
| Cefadroxil | Duricef |
| |
| Cefazolin | Ancef | ||
| Cefalotin or Cefalothin | Keflin | ||
| Cefalexin | Keflex | ||
| Cephalosporins (Second generation) | |||
| Cefaclor | Ceclor |
| |
| Cefamandole | Mandole | ||
| Cefoxitin | Mefoxin | ||
| Cefprozil | Cefzil | ||
| Cefuroxime | Ceftin, Zinnat | ||
| Cephalosporins (Third generation) | |||
| Cefixime | Suprax |
| |
| Cefdinir | Omnicef | ||
| Cefditoren | Spectracef | ||
| Cefoperazone | Cefobid | ||
| Cefotaxime | Claforan | ||
| Cefpodoxime | |||
| Ceftazidime | Fortaz | ||
| Ceftibuten | Cedax | ||
| Ceftizoxime | |||
| Ceftriaxone | Rocephin | ||
| Cefdinir | |||
| Cephalosporins (Fourth generation) | |||
| Cefepime | Maxipime |
| |
| Glycopeptides | |||
| Teicoplanin | |||
| Vancomycin | Vancocin | ||
| Macrolides | |||
| Azithromycin | Zithromax, Sumamed, Zitrocin | Streptococcal infections, syphilis, respiratory infections, mycoplasmal infections, Lyme disease |
|
| Clarithromycin | Biaxin | ||
| Dirithromycin | |||
| Erythromycin | |||
| Roxithromycin | |||
| Troleandomycin | |||
| Telithromycin | Ketek | Pneumonia | Visual Disturbance, LIVER TOXICITY. This medication's approval in the U.S. was controversial, and one doctor went to jail in followup attempts to ascertain its safety because she falsified the results of her part of the testing precisely because it seemed to cause liver problems, including liver failure, to a greater extent than would be expected of a common-use antibiotic.[3] |
| Spectinomycin | Antimetabolite, Anticancer | ||
| Monobactams | |||
| Aztreonam | |||
| Penicillins | |||
| Amoxicillin | Novamox | Wide range of infections; penicillin used for streptococcal infections, syphilis, and Lyme disease |
|
| Ampicillin | |||
| Azlocillin | |||
| Carbenicillin | |||
| Cloxacillin | |||
| Dicloxacillin | |||
| Flucloxacillin | |||
| Mezlocillin | |||
| Nafcillin | |||
| Penicillin | |||
| Piperacillin | |||
| Ticarcillin | |||
| Polypeptides | |||
| Bacitracin | Eye, ear or bladder infections; usually applied directly to the eye or inhaled into the lungs; rarely given by injection | Kidney and nerve damage (when given by injection) | |
| Colistin | |||
| Polymyxin B | |||
| Quinolones | |||
| Ciprofloxacin | Ciproxin, CiploxESTECINA | Urinary tract infections, bacterial prostatitis, community-acquired pneumonia, bacterial diarrhea, mycoplasmal infections, gonorrhea | Nausea (rare), tendinosis (rare) |
| Enoxacin | |||
| Gatifloxacin | Tequin | ||
| Levofloxacin | Levaquin | ||
| Lomefloxacin | |||
| Moxifloxacin | Avelox | ||
| Norfloxacin | NOROXIN | ||
| Ofloxacin | Ocuflox | ||
| Trovafloxacin | Trovan | ||
| Sulfonamides | |||
| Mafenide | Urinary tract infections (except sulfacetamide and mafenide); mafenide is used topically for burns |
| |
| Prontosil (archaic) | |||
| Sulfacetamide | |||
| Sulfamethizole | |||
| Sulfanilimide (archaic) | |||
| Sulfasalazine | |||
| Sulfisoxazole | |||
| Trimethoprim | |||
| Trimethoprim-Sulfamethoxazole (Co-trimoxazole) (TMP-SMX) | Bactrim | ||
| Tetracyclines | |||
| Demeclocycline | Syphilis, chlamydial infections, Lyme disease, mycoplasmal infections, acne rickettsial infections |
| |
| Doxycycline | Vibramycin | ||
| Minocycline | Minocin | ||
| Oxytetracycline | Terracin | ||
| Tetracycline | Sumycin | ||
| Others | |||
| Arsphenamine | Salvarsan | Spirochaetal infections (obsolete) | |
| Chloramphenicol | Chloromycetin | ||
| Clindamycin | Cleocin | acne infections, prophylaxis before surgery | |
| Lincomycin | acne infections, prophylaxis before surgery | ||
| Ethambutol | Antituberculosis | ||
| Fosfomycin | |||
| Fusidic acid | Fucidin | ||
| Furazolidone | |||
| Isoniazid | Antituberculosis | ||
| Linezolid | Zyvox | ||
| Metronidazole | Flagyl | Giardia | |
| Mupirocin | Bactroban | ||
| Nitrofurantoin | Macrodantin, Macrobid | ||
| Platensimycin | |||
| Pyrazinamide | Antituberculosis | ||
| Quinupristin/Dalfopristin | Syncercid | ||
| Rifampin or Rifampicin | Binds to the β subunit of "RNA polymerase" to inhibit transcription of mostly "Gram-positive" and "mycobacteria" | Reddish-orange sweat, tears, and urine | |
| Tinidazole | |||
| Generic Name | Brand Names | Common Uses | Possible Side Effects |
انظر أيضا
وصلات خارجية
- Antibiotic News from Genome News Network (GNN)
- Are Antibiotics Killing Us? -Discover Magazine
- JAAPA: New antibiotics useful in primary care
- A new method for controlling bacterial activity without antibiotics - Research conducted at the Hebrew University
- BURDEN of Resistance and Disease in European Nations
- Antibiogram technique video
المصادر
عدنان تكريتي. "الصادات". الموسوعة العربية.
- ^ قالب:معجم التكنولوجيا الحيوية
- ^ Robert Berkow (ed.) The Merck Manual of Medical Information - Home Edition. Pocket (September 1999), ISBN 0-671-02727-1.
- ^
Splete, Heidi (2006). "Liver toxicity reported with Ketek". Internal Medicine News.
{{cite journal}}:|access-date=requires|url=(help); Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help)



