ثلاثي أكسيد التلوريوم
| |
| الأسماء | |
|---|---|
| أسماء أخرى
tellurium(VI) oxide
| |
| المُعرِّفات | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.033.277 |
| رقم EC |
|
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | TeO3 |
| كتلة مولية | 175.6 g/mol |
| المظهر | yellow-orange crystals (α-TeO3) |
| الكثافة | 5.07 g/cm3, solid |
| نقطة الانصهار | |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
ثلاثي أكسيد تلوريوم Tellurium trioxide هو مركب كيميائي له الصيغة TeO3 ، ويكون على شكل بلورات صفراء برتقالية. في هذا المركب، تلوريوم يتواجد في حالة الأكسدة +6.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
تعدد الأشكال
توجد صيغتان، أصفر مائل للاحمرار α-TeO3 ورمادي معيّن الأسطح، β-TeO3 وهو أقل تفاعلاً.[1]
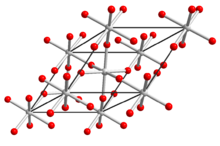
α-TeO3 له بنية مشابهة لـ FeF3 مع وحدات ثمانية الأسطح TeO6 تتشارك في كل الرؤوس.[2]
التحضير
α-TeO3 يمكن تحضيره بتسخين حمض التلوريك المتعامد، Te(OH)6، لدرجة حرارة أعلى من 300 °س .[1] الشكل β-TeO3 يمكن تحضيره بتسخين α-TeO3 في أنبوب محكم الإغلاق مع O2 و H2SO4.
α-TeO3 هو غير متفاعل مع الماء ولكنه عامل مؤكسد قوي حين يُسخـَّن.[2] ويشكـِّل مع القلويات تليورات.[2]
وحين يُسخـَّن α-TeO3 فإنه يفقد الأكسجين ليشكل أولاً Te2O5 ثم TeO2.[1]
المصادر
الهامش
- ^ أ ب ت Inorganic Chemistry,Egon Wiberg, Arnold Frederick Holleman Elsevier 2001 ISBN 0-12-352651-5
- ^ أ ب ت Greenwood, N. N. (1997). Chemistry of the Elements (2nd Edition ed.). Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
{{cite book}}:|edition=has extra text (help); Unknown parameter|coauthors=ignored (|author=suggested) (help)