نكاف
| Mumps | |
|---|---|
| الأسماء الأخرى | Epidemic parotitis |
 | |
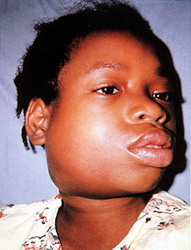
| Child with mumps showing characteristic facial swelling | |
| التخصص | Infectious disease |
| الأعراض | Parotitis and non-specific symptoms such as fever, headache, malaise, muscle pain, and loss of appetite |
| المضاعفات | Deafness, inflammatory conditions such as orchitis, oophoritis, and pancreatitis, and rarely sterility |
| البداية المعتادة | 7–25 days after exposure |
| المدة | Usually less than two weeks |
| المسببات | Mumps virus |
| عوامل الخطر | Exposure to someone with mumps |
| الطريقة التشخيصية | Antibody testing, viral cultures, and reverse transcription polymerase chain reaction |
| الوقاية | Vaccination |
| العلاج | Supportive |
| الدواء | Pain medication, intravenous immunoglobulin |
| Prognosis | Usually excellent; case fatality rate of 1.6–3.8 people per 10,000 |
| التردد | Most common in childhood and in countries that do not vaccinate |
النكاف (بالإنگليزية: Mumps) هو مرض ڤيروسي حاد، وقد وصف أبقراط التهاب الغدة النكفية، والتهاب الخصية في القرن الخامس قبل الميلاد. Initial symptoms of mumps are non-specific and include fever, headache, malaise, muscle pain, and loss of appetite. These symptoms are usually followed by painful swelling of the parotid glands, called parotitis, which is the most common symptom of a mumps infection. Symptoms typically occur 16 to 18 days after exposure to the virus and resolve within two weeks. About one third of infections are asymptomatic.
Complications are rare but include deafness and a wide range of inflammatory conditions, of which inflammation of the testes, breasts, ovaries, pancreas, meninges, and brain are the most common. Testicular inflammation may result in reduced fertility and, rarely, sterility.
Humans are the only natural host of the mumps virus. The mumps virus is an RNA virus in the family Paramyxoviridae. The virus is primarily transmitted by respiratory secretions such as droplets and saliva, as well as via direct contact with an infected person. Mumps is highly contagious and spreads easily in densely populated settings. Transmission can occur from one week before the onset of symptoms to eight days after. During infection, the virus first infects the upper respiratory tract. From there, it spreads to the salivary glands and lymph nodes. Infection of the lymph nodes leads to presence of the virus in blood, which spreads the virus throughout the body. Mumps infection is usually self-limiting, coming to an end as the immune system clears the infection.
In places where mumps is common, it can be diagnosed based on clinical presentation. In places where mumps is less common, however, laboratory diagnosis using antibody testing, viral cultures, or real-time reverse transcription polymerase chain reaction may be needed. There is no specific treatment for mumps, so treatment is supportive in nature and includes rest and pain relief. Prognosis is usually excellent with a full recovery as death and long-term complications are rare. Infection can be prevented with vaccination, either via an individual mumps vaccine or through combination vaccines such as the MMR vaccine, which also protects against measles and rubella. The spread of the disease can also be prevented by isolating infected individuals.
Mumps historically has been a highly prevalent disease, commonly occurring in outbreaks in densely crowded spaces. In the absence of vaccination, infection normally occurs in childhood, most frequently at the ages of 5–9. Symptoms and complications are more common in males and more severe in adolescents and adults. Infection is most common in winter and spring in temperate climates, whereas no seasonality is observed in tropical regions. Written accounts of mumps have existed since ancient times, and the cause of mumps, the mumps virus, was discovered in 1934. By the 1970s, vaccines had been created to protect against infection, and countries that have adopted mumps vaccination have seen a near-elimination of the disease. In the 21st century, however, there has been a resurgence in the number of cases in many countries that vaccinate, primarily among adolescents and young adults, due to multiple factors such as waning vaccine immunity and opposition to vaccination.[1]
التاريخ
According to Chinese medical literature, mumps was recorded as far back as 640 B.C.[2] The Greek physician Hippocrates documented an outbreak on the island of Thasos in approximately 410 B.C. and provided a fuller description of the disease in the first book of Epidemics in the Corpus Hippocraticum.[3][4] In modern times, the disease was first described scientifically in 1790 by British physician Robert Hamilton in Transactions of the Royal Society of Edinburgh.[5] During the First World War, mumps was one of the most debilitating diseases among soldiers.[6] In 1934, the etiology of the disease, the mumps virus, was discovered by Claude D. Johnson and Ernest William Goodpasture. They found that rhesus macaques exposed to saliva taken from humans in the early stages of the disease developed mumps. Furthermore, they showed that mumps could then be transferred to children via filtered and sterilized, bacteria-less preparations of macerated monkey parotid tissue, showing that it was a viral disease.[3][4]
In 1945, the mumps virus was isolated for the first time. Just a few years later, in 1948, an inactivated vaccine using killed viruses was invented. This vaccine provided only short-term immunity and was later discontinued. It was replaced in the 1970s with vaccines that have live but weakened viruses, which are more effective at providing long-term immunity than the inactivated vaccine. The first of these vaccines was Mumpsvax, licensed on 30 March 1967, which used the Jeryl Lynn strain. Maurice Hilleman created this vaccine using the strain taken from his five-year-old daughter, Jeryl Lynn. Mumpsvax was recommended for use in 1977, and the Jeryl Lynn strain continues to be used.[7][4]
Hilleman worked to combine the attenuated mumps vaccines with measles and rubella vaccines, creating the MMR-1 vaccine. In 1971, a newer version, MMR-2, was approved for use by the US Food and Drug Administration.[7] In the 1980s, the benefit of multiple doses was recognized, so a two-dose immunization schedule was widely adopted.[7][8] With MMR-2, four other MMR vaccines have been created since the 1960s: Triviraten, Morupar, Priorix, and Trimovax. Since the mid-2000s, two MMRV vaccines have been in use: Priorix-Tetra and ProQuad.[9]
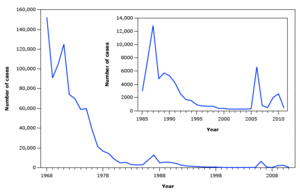
The United States began to vaccinate against mumps in the 1960s, with other countries following suit.[3] From 1977 to 1985, 290 cases per 100,000 people were diagnosed each year worldwide.[10] Although few countries recorded mumps cases after they began vaccination, those that did reported dramatic declines. From 1968 to 1982, cases declined by 97% in the U.S., in Finland cases were reduced to less than one per 100,000 people per year,[11] and a decline from 160 cases per 100,000 to 17 per 100,000 per year in England was observed from 1989 to 1995.[12] By 2001, there had been a 99.9% reduction in the number of cases in the U.S. and similar near-elimination in other vaccinating countries.[3]
In Japan in 1993, concerns over the rates of aseptic meningitis following MMR vaccination with the Urabe strain prompted the removal of MMR vaccines from the national immunization program, resulting in a dramatic increase in the number of cases.[9][3] Japan provides voluntary mumps vaccination separately from measles and rubella.[13] Starting in the mid-1990s, controversies surrounding the MMR vaccine emerged. One paper connected the MMR vaccine to Crohn's disease in 1995, and another in 1998 connected it to autism spectrum disorders and inflammatory bowel disease. These papers are now considered to be fraudulent and incorrect, and no association between the MMR vaccine and the aforementioned conditions has been identified. Despite this, their publication led to a significant decline in vaccination rates, ultimately causing measles, mumps, and rubella to reemerge in places with lowered vaccination rates.[10][14][4]
Outbreaks in the 21st century include more than 300,000 cases in China in 2013[2] and more than 56,000 cases in England and Wales in 2004–2005. In the latter outbreak, most cases were reported in 15–24 year olds who were attending colleges and universities. This age group was thought to be vulnerable to infection because of the MMR vaccine controversies when they should have been vaccinated or MMR vaccine shortages that had also occurred at that time.[10] Similar outbreaks in densely crowded environments have frequently occurred in many other countries, including the U.S., the Netherlands, Sweden, and Belgium.[7]
Resurgence
| Year(s) | Location | Number of cases |
|---|---|---|
| 2005–2006 | Czech Republic | 5,998 |
| 2006 | U.S. | 6,584 |
| 2009 | New York (U.S.) | 1,521 |
| 2009–2011 | Jerusalem | 3,130 |
| 2012–2013 | Belgium | 4,061 |
| 2013 | Poland | 2,436 |
| 2014 | U.S. | 1,151 |
| 2016–2017 | Arkansas (U.S.) | 2,706 |
| 2017 | U.S. | 5,629 |
In the 21st century, mumps has reemerged in many places that vaccinate against it, causing recurrent outbreaks. These outbreaks have largely affected adolescents and young adults in densely crowded spaces, such as schools, sports teams, religious gatherings, and the military, and it is expected that outbreaks will continue to occur. The cause of this reemergence is subject to debate, and various factors have been proposed, including waning immunity from vaccination, low vaccination rates, vaccine failure, and potential antigenic variation of the mumps virus.[9][3][7][11]
Waning immunity from vaccines is likely the primary cause of the mumps resurgence. In the past, subclinical natural infections provided boosts to immunity similar to vaccines. As time went on with vaccine use, these asymptomatic infections declined in frequency, likely leading to a reduction in long-term immunity against mumps. With less long-term immunity, the effects of waning vaccine immunity became more prominent, and vaccinated individuals have frequently fallen ill from mumps. A third dose of the vaccine provided in adolescence has been considered to address this as some studies support this. Other research indicates that a third dose may be useful only for short-term immunity in responding to outbreaks,[15][7] which is recommended for at-risk persons by the Advisory Committee on Immunization Practices of the Centers for Disease Control and Prevention.[9]
Low vaccination rates have been implicated as the cause of some outbreaks in the UK, Canada, Sweden, and Japan, whereas outbreaks in other places, such as the U.S., the Czech Republic, and the Netherlands, have occurred mainly among the vaccinated. Compared to the measles and rubella vaccines, mumps vaccines appear to have a relatively high failure rate, varying depending on the vaccine strain. This has been addressed by providing two vaccine doses, supported by recent outbreaks among the vaccinated having primarily occurred among those who received only one dose. Lastly, certain mumps virus lineages are highly divergent genetically from vaccine strains, which may cause a mismatch between protection against vaccine strains and non-vaccine strains, though research is inconclusive on this matter.[9][7]
أصل الاسم الإنجليزي
The word "mumps" is first attested circa 1600 and is the plural form of "mump", meaning "grimace", originally a verb meaning "to whine or mutter like a beggar". The disease was likely called mumps in reference to the swelling caused by mumps parotitis, reflecting its impact on facial expressions and the painful, difficult swallowing that it causes. "Mumps" was also used starting from the 17th century to mean "a fit of melancholy, sullenness, silent displeasure".[10][16] Mumps is sometimes called "epidemic parotitis".[17][18][2]
فيروس النكاف
ينتمي ڤيروس النكاف إلى الڤيروسات نظيرة المخاطية Paramyxovirus، وهي المجموعة التي تنتمي لها أيضا ڤيروسات البار إنفلونزا والحصبة وفيروس داء نيوكاسل. وتؤدي الإصابة ڤيروس داء نيوكاسل، وڤيروس البارا إنفلونزا إلى إنتاج أضداد تتفاعل بشكل متصالب مع ڤيروس النكاف. يحتوي مجين Genome ڤيروس النكاف على شريط واحد من RNA.
يمكن عزل الڤيروس أو زرعه على مزارع النسج البشرية أو الفردية المختلفة أو في بيض الدجاج المخصب، ويمكن عزله من المرضى من اللعاب، والسائل الدماغي الشوكي، والبول، والدم، والحليب والنسج المخموجة. يتعطل ڤيروس النكاف بسرعة بالحرارة والفورمالين والإيثرو الكلوروفورم والأشعة فوق البنفسجية.
الإمراض
ينتقل ڤيروس النكاف عن طريق القطيرات التنفسية، حيث يتكاثر في البلعوم الأنفي والعقد اللمفاوية الناحية. وبعد حوالي 12-25 يوماً يحدث انتشار الڤيروس إلى الدم (تفيرس الدم) Viremia ويدوم ذلك 3-5 أيام. وخلال هذه المرحلة ينتشر الڤيروش إلى النسج المتعددة بما فيها السحايا، والغدد مثل الغدد اللعابية، والپنكرياس، والخصيتين، والمبيضين. ويؤدي التهاب النسج المخموجة إلى أعراض مميزة لالتهاب الغدة النكفية والتهاب السحايا العقيم.
فترة الحضانة
تبلغ فترة الحضانة 14-18 يوماً (يتراوح المجال بين 14-25 يوماً).
المظاهر السريرية
تكون الأعراض البادرية غير نوعية وتشمل، الألم العضلي، ونقص الشهية، والتعب، والصداع، والحمى الخفيفة. ويكون التهاب الغدة النكفية Parotitis أشيع التظاهرات ويحدث عند 30-40% من المرضى ويكون وحيد الجانب أو ثنائي الجانب، وقد تصاب أي من الغدد اللعابية الأخرى. يحدث التهاب الغدة النكفية خلال اليومين الأوليين من المرض. وقد يتظاهر في البداية على شكل ألم بالأذن وإيلام عند جس زاوية الفك. تخف الأعراض بعد أسبوع وتختفي بعد 10 أيام. تكون 20% من حالات النكاف لاعرضية وفي 50-40٪ من الحالات قد تكون الأعراض غير نوعية أو أعراض تنفسية بشكل رئيس.
المضاعفات
• إصابة الجملة العصبية المركزية: يتظاهر ذلك بشكل شائع على شكل التهاب السحايا العقيم ويكون لاعرضياً (وجود الخلايا الالتهابية في السائل الدماغي الشوكي) في 50-60 % من الحالات.
أما التهاب السحايا العرضي (الصداع ، صلاة النقرة) فيحدث عند 15٪ من المرضى ويزول دون أي عقابيل خلال 3-10 أيام. إن البالغين معرضون لهذا الاختلاط بشكل أكبر من الأطفال وتكون إصابة الذكور أكثر من إصابة الإناث (النسبة 3 : 1). قد يكون التهاب الغدة النكفية غائباً في 50٪ من هؤلاء المرضى. أما التهاب الدماغ فهو نادر (أقل من 2 لكل 100 الف). لقد كان ڤيروس النكاف قبل عصر التلقيح واحداً من أشيع أسباب التهاب السحايا العقيم.
• التهاب الخصية Orchitis: وهو أشيع اختلاط عند الذكور بعد البلوغ، ويحدث عند 50٪ من الذكور بعد البلوغ ويلي عادة التهاب الغدة النكفية لكن قد يسبقه أو يحدثان معاً بنفس الوقت أو قد يحدث لوحده. يكون التهاب الخصية ثنائي الجانب في 30% من الذكور المصابين.
يتظاهر التهاب الخصية عادة على شكل بداية حادة لتورم الخصية مع الإيلام والغثيان والإقياء والحمى. قد يختفي التورم والألم خلال أسبوع واحد لكن قد يستمر الإيلام لعدة أسابيع. يحدث عند حوالي 50٪ من المرضى المصابين بالتهاب الخصية درجة ما من الضمور الخصوي لكن العقم نادر.
• التهاب المبيض Oophoritis: يحدث عند 5٪ من الإناث بعد البلوغ وقد يقلد التهاب الزائدة وليس هناك علاقة مع نقص الخصوبة.
• التهاب الپنكرياس: وهو نادر لكن يحدث أحياناً دون التهاب النكفة. يكون فرط سكر الدم عابراً وعكوساً. ورغم أن بعض التقارير ذكرت حدوث الداء السكري لكن لم يثبت وجود العلاقة السببية بشكل حاسم بعد. وقد ذكر حدوث جائحات من الداء السكري بعد عدة أشهر أو سنوات من جائحات النكاف.
• الصمم : لقد كان الصمم الناجم عن النكاف السبب الرئيس للصمم الحسي العصبي المكتسب في الطفولة في عصر ما قبل اللقاح. تقدر نسبة حدوث الصمم تقريباً بحوالي حالة واحدة من كل 20 ألف حالة نكاف، يكون فقدان السمع وحيد الجانب في 80% من الحالات وقد يترافق مع ارتكاسات دهليزية. تكون البداية مفاجئة عادة ويؤدي إلى ضعف دائم في السمع.
• يحدث عند 3-15٪ من مرضى النكاف تبدلات تخطيطية على تخطيط القلب الكهربي ECG تتوافق مع التهاب العضلة القلبية. لكن نادراً ما تكون الحالة عرضية. إن الشفاء التام هو القاعدة لكن ذکر حدوث وفيات.
• من الاختلاطات الأقل شيوعاً للنكاف ألم المفاصل، والتهاب المفاصل،والتهاب الكلية.
• تم تسجيل حدوث وفاة واحدة وسطية في السنة بسبب النكاف في الولايات المتحدة في الفترة بین 1980-1999.
التشخيص المخبري
يُشك بتشخيص النكاف عادة اعتماداً على التظاهرات السريرية خاصة بوجود التهاب النكفة. ويمكن عزل ڤيروس النكاف من العينات السريرية وتشمل اللعاب، والبول والسائل الدماغي الشوكي، ويجب عند عزل الڤيروس جمع العينات خلال الأيام الخمسة الأولى من المرض.
إن الفحوص المصلية هي أشيع طريقة لتشخيص النكاف. إن تثبيت المتممة Complement Fixation CF وتثبيط التراص الدموي طريقتان غير حساستين نسبياً. وقد لا تكون النتائج موثوقة.
تشمل الاختبارات التي أظهرت مصداقية: تعديل الأضداد Neutralization، والمقايسة المناعية الأنزيمية EIA، والانحلال الدموي الشعاعي Radial.
إن المقايسة المناعية الأنزيمية متوفرة تجارياً بشكل واسع. وهي أكثر حساسية من CF وتثبيط التراص الدموي وهي متوفرة لكل من IgG و IgM.
تصبح الأضداد من نوع IgM قابلة للكشف عادة خلال الأيام القليلة الأولى من المرض وتصل إلى ذروتها بعد أسبوع من بداية المرض أما اختبار IgG فيحتاج عادة إلى عينتين يفصل بينهما عدة أسابيع. ويجب أن تظهر العينة الثانية (عينة النقاهة) زيادة هامة في الأضداد مقارنة مع العينة الأولى (عينة المرحلة الحادة).
الوبائيات
يحدث النكاف في كل أنحاء العالم. وهو مرض بشري ولايوجد حملة للمرض، ينتقل النكاف عن طريق الهواء أو التماس المباشر مع اللعاب أو القطيرات المحمولة بالهواء. تحدث ذروة الإصابة في الشتاء والربيع. إن سراية المرض مشابهة لسراية الإنفلونزا والحصبة الألمانية لكنها أقل من الحصبة أو الحماق. تحدث العدوى قبل 3 أيام من ظهور المرض وحتى 4 أيام بعد المرض الفعال وقد تم عزل الڤيروس من اللعاب قبل 7 أيام من ظهور المرض وحتى 9 أيام بعد حدوث التهاب النكفة.
الاتجاهات العامة في الولايات المتحدة
انخفضت حالات النكاف بسرعة بعد الترخيص باستخدام لقاح النكاف، وقد تم تسجيل حوالي 3000 حالة سنوياً في الفترة بين عام 1983-1985 (1.3-1.55 حالة لكل 100 الف من السكان) مقارنة مع حوالي 212 ألف حالة عام 1964.
ومنذ عام 1989 حدث انخفاض ثابت في حالات النكاف المسجلة حتى وصل العدد إلى 231 حالة عام 2001 وهو أقل معدل سنوي تم تسجيله.
كانت معظم الحالات قبل ترخيص لقاح النكاف عام 1967 تحدث عند الأطفال بين عمر 5 -9 سنوات وكانت 90% من الحالات تحدث عند الأطفال بعمر 15 سنة فما دون. وفي أواخر الثمانينيات حدث انزياح باتجاه الأطفال الأكبر سناً. وقد شكل الأطفال بعمر 15 سنة فما فوق 30-40% من الحالات سنوية منذ عام 1990 (42% من الحالات عام 2002).
تعريف الحالة السريرية للنكاف
الحالة السريرية للنكاف هي تورم مؤلم في الغدة النكفية أو أي غدة لعابية ذو بداية حادة، وحيد أو ثنائي الجانب محدد لذاته يدوم يومين على الأقل دون وجود سبب ظاهر.
لقاح النكاف
- الخصائص:
تم عزل فيروس النكاف عام 1945 وتم تطوير اللقاح المعطل عام 1948 ولكن المناعة الناجمة عن هذا اللقاح كانت قصيرة الأمد، وقد توقف استخدامه في منتصف السبعينات. أما اللقاح المستخدم حالياً والذي يحتوي على ڤيروس النكاف الحي المضعف من ذرية Jeryl Lynn فقد تم السماح باستخدامه عام 1967.
يتوفر لقاح النكاف على شكل مستحضر وحيد المستضد (لقاح النكاف فقط) أو مشركاً مع لقاح الحصبة الألمانية أو مع لقاحي الحصبة ولقاح الحصبة الألمانية. وتوصي ACIP باستخدام لقاح MMR في حال وجود استطباب لإعطاء أي من مكونات هذا اللقاح.
يتم تحضير لقاح النكاف من مزارع ڤيروس النكاف على الأرومات الليفية لجنين الدجاج. يتوفر لقاح MMR على شكل بودرة مجفدة Lyophilized (أي مجففة بالتجميد) ويحل عند الاستخدام بماء معقم خال من المواد الحافظة. يحتوي لقاح MMR على كميات صغيرة من الألبومين البشري والنيوميسين والسوربيتول والهلام Gelatin.
فعالية اللقاح وقدرته الاستمناعية
يؤدي لقاح النكاف إلى حدوث خمج خفيف غير ظاهر وغير معدٍ، ويتطور عند أكثر من 97% من الأشخاص الملقحين أضداد قابلة للقياس بعد جرعة وحيدة من اللقاح. وتقدر الفعالية السريرية اللقاح بحدود 95٪ ( لمجال من 90-97 ٪) ويعتقد أن فترة بقاء المناعة الناجمة عن اللقاح أكثر من 25 سنة، ومن المرجح أنها مدى الحياة عند معظم الأشخاص الملقحين.
جدول التلقيح والاستخدام
يوصي بإعطاء جرعتين من لقاح النكاف لكل الأطفال على شكل لقاح مشترك مع لقاحي الحصبة والحصبة الألمانية (MMR) بفاصل 4 أسابيع على الأقل. تعطي الجرعة الأولى من MMR بعمر السنة أو بعد ذلك وإن لقاح النكاف الذي يعطي قبل عمر السنة يجب عدم اعتباره جزء من سلسلة التلقيح، وبالتالي فالأطفال الذين أعطوا لقاح MMR قبل عمر السنة يجب إعادة تلقيحهم بجرعتين من لقاح MMR بحيث تكون الجرعة الأولى بعمر السنة على الأقل.
ويوصي بإعطاء الجرعة الثانية لإحداث المناعة للحصبة عند الأشخاص الذين لم يستجيبوا للجرعة الأولى. وتشير المعلومات إلى أن كل الأشخاص الذين لم يستجيبوا للجرعة الأولى من لقاح الحصبة سوف يستجيبون للجرعة الثانية من لقاح MMR، في حين تتوافر معلومات قليلة عن الاستجابة المناعية لمكونتي الحصبة الألمانية والنكاف بعد إعطاء الجرعة الثانية من لقاح MMR. ومع ذلك فمن المتوقع أن معظم الأشخاص الذين لم يستجيبوا لمكونتي الحصبة الألمانية والنكاف بعد الجرعة الأولى من لقاح MMR سوف يستجيبون للجرعة الثانية من لقاح MMR.
إن الجرعة الثانية من لقاح MMR لا تعتبر جرعة داعمة بصورة عامة؛ لأن الاستجابة المناعية المبدئية للجرعة الأولى من اللقاح تمنح الجسم مناعة طويلة الأمد. ورغم أن الجرعة الثانية من MMR قد تزيد عيار الأضداد عند بعض الأشخاص الذين استجابوا للجرعة الأولى فإن المعلومات المتوفرة تشير إلى أن هذه الزيادة في عيار الأضداد ليست ثابتة.
يجب أن تعطي الجرعة الثانية من MMR روتينياً بعمر 4-6 سنوات قبل دخول الطفل إلى دور الحضانة أو المدرسة. ويمكن إعطاء الجرعة الثانية من لقاح MMR بعد فترة 4 أسابيع (أي 28 يوماً من الجرعة الأولى).
المناعة ضد النكاف
يعتبر الشخص ممنعاً ضد النكاف في الحالات التالية:
1. الإصابة بالنكاف (التي تم تشخيصها من قبل الطبيب).
2. التلقيح بجرعة واحدة على الأقل من لقاح النكاف الحي المضعف بعمر السنة أو بعد ذلك.
3. وجود أضداد النكاف من نوع IgG.
4.إذا كان مولوداً قبل عام 1957.
الوقاية بعد التعرض
لا يعتبر الغلوبولين المناعي للنكاف، ولا الغلوبولين المناعي IG فعالين في الوقاية من النكاف بعد التعرض. وإن التلقيح بعد التعرض ليس مؤذياً وقد يفيد في منع حدوث المرض لاحقاً.
الارتكاسات الجانبية التالية للتلقيح
إن لقاح النكاف لقاح آمن جداً، ومعظم التأثيرات الجانبية التي تحدث بعد إعطاء لقاح MMR مثل (الحمى والطفح والأعراض المفصلية) ناجمة عن مكونتي الحصبة والحصبة الألمانية.
ذكر في حالات نادرة حدوث الحمى والتهاب النكفة، كما ذكر حدوث حالات نادرة من خلل وظيفة الجملة العصبية المركزية CNS بما فيها الصمم قد ذكر حدوثها خلال شهرين من إعطاء لقاح النكاف. وتقدر نسبة حدوث الارتكاسات العصبية المركزية بحوالي 1 من كل مليون جرعة من اللقاح.
وقد خلص معهد الطب عام 1993 إلى أن الأدلة غير كافية لقبول أو رفض العلاقة السببية بين لقاح النكاف من ذرية Jeryl Lynn والتهاب السحايا العقيم أو التهاب الدماغ أو الصمم الحسي العصبي أو التهاب الخصية.
تشمل الارتكاسات الأليرجيائية، الطفح والحكة والفرفريات. وهذه الارتكاسات تترافق بشكل مؤقت مع التلقيح لكنها تكون عابرة وخفيفة عادة.
مضادات استطبابات التلقيح ومحاذيره
يجب بصورة عامة عدم التلقيح بلقاح MMR للأشخاص الذين حدث لديهم ارتكاس أليرجيائي شديد (أي الشرى أو توذم الشفتين أو الحلق أو صعوبة التنفس وهبوط التوتر الشرياني والصدمة) بعد جرعة سابقة من لقاح النكاف أو ارتكاس لأحد مكونات اللقاح (مثل الهلام Gelatin والنيوميسين).
في الماضي كان الأشخاص الذين لديهم ارتكاسات تأقانية تالية لتناول البيض يعتبرون معرضين لزيادة خطر حدوث الارتكاسات الخطيرة بعد إعطاء لقاح الحصبة أو لقاح النكاف (أو أي لقاح يحوي أي منهما) حيث إن هذين اللقاحين ينتجان في الأرومات الليفية لجنين الدجاج. ولكن المعلومات الحديثة تقترح أن معظم الارتكاسات التأقانية للقاحات الحاوية على لقاح الحصبة أو لقاح النكاف ليست ناجمة عن فرط الحساسية لمستضدات البيض ولكن تنجم عن مكونات أخرى في اللقاح (مثل الهلام Gelatin).
إن خطر الارتكاسات الأليرجيائية الخطيرة مثل التأق بعد إعطاء هذه اللقاحات للأشخاص المتحسسين للبيض منخفض جداً، وإن الاختبار الجلدي قبل إعطاء اللقاح لا يتنبأ بحدوث الارتكاس الأليرجيائي للقاح، وبالنتيجة يمكن إعطاء لقاح MMR للأطفال المتحسسين للبيض دون إجراء الاختبار الجلدي روتينياً قبل إعطاء اللقاح أو استخدام أي بروتوكولات اخرى.
لا يحتوي لقاح MMR على البنسلين، ولذلك فإن قصة الحساسية للبنسلين لا تعتبر مضاد استطباب للتلقيح بلقاح MMR.
لا يعطى لقاح النكاف للنساء الحوامل لأسباب نظرية. ولكن ليس هناك دليل على أن ڤيروس لقاح النكاف يسبب أذية جنينية، ويجب تجنب حدوث الحمل لمدة 4 أسابيع بعد التلقيح بلقاح MMR.
لا يعطى اللقاح للأشخاص المصابين بالعوز المناعي أو التثبيط المناعي الناجم عن الابيضاض أو اللمفوما أو الخبائة المعممة أو داء العوز المناعي أو المعالجة المثبطة للمناعة. في حين لا تعتبر المعالجة بمستحضرات الستيروئيدات القشرية بجرعة منخفضة (أقل من 2 ملغ / كغ / اليوم) أو المعالجة المناوبة (كل ثاني يوم) أو المعالجة الموضعية أو المعالجة الضبوبية aeroslized مضاد استطباب للتلقيح بلقاح النكاف. ويمكن تلقيح الأشخاص الذين تم إيقاف المعالجة المثبطة للمناعة بالستيروئيدات لمدة شهر.
يجب عدم تلقيح الأشخاص المصابين بمرض حاد شديد أو متوسط الشدة حتى يتحسن المرض. أما الأمراض الخفيفة (مثل التهاب الأذن الوسطى والأخماج النفسية العلوية الخفيفة) والمعالجة المرافقة بالصادات والتعرض أو الشفاء من أمراض أخرى. كل ذلك لا يعتبر مضاد استطباب للتلقيح بلقاح النكاف.
إن تلقى الشخصي لمنتجات الدم الحاوية على الأضداد (مثل الفلوبولين المناعي أو كامل الدم أو الكريات الحمر المكدسة أو الغلوبولين المناعي الوريدي) قد يتداخل مع الانقلاب المصلي بعد التلقيح بلقاح النكاف، ويجب إعطاء اللقاح قبل أسبوعين من إعطاء هذه المنتجات أو تأخير إعطائه لمدة 3 أشهر على الأقل.
إن القصة العائلية للسكري لا تعتبر مضاد استطباب للتلقيح.
تخزين اللقاح والتعامل معه
يجب نقل لقاح MMR ضمن برادات خاصة للمحافظة على حرارة 10 درجات مئوية (50 درجة فهرنهايت) أو أقل طيلة الوقت، ويجب تبريد اللقاح مباشرة عند الوصول، ووقايته من الضوء طيلة الوقت.
يجب تخزين اللقاح بدرجة حرارة البراد (2-8 درجات مئوية أو 4635 فهرنهايت) ويمكن أيضاً تجميد اللقاح. أما بالنسبة للمادة المحلة قيمكن تخزينها بدرجة حرارة البراد أو درجة حرارة الغرفة.
ويجب بعد حل اللقاح تخزينه بدرجة حرارة البراد ووقايته من الضوء. ويجب استعماله مباشرة وإذا لم يستخدم خلال 8 ساعات من حله فيجب التخلص منه.
المصادر
- [19].
- ^ Barskey, Albert E.; Glasser, John W.; LeBaron, Charles W. (19 أكتوبر 2009). "Mumps resurgences in the United States: A historical perspective on unexpected elements". Vaccine. Elsevier BV. 27 (44): 6186–6195. doi:10.1016/j.vaccine.2009.06.109. ISSN 0264-410X. PMID 19815120.
- ^ أ ب ت خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةshu - ^ أ ب ت ث ج ح خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةrubin - ^ أ ب ت ث "Tracing the story of mumps: a timeline". Pharmaceutical Technology. Pharamaceutical Technology. 25 أبريل 2018. Retrieved 30 أكتوبر 2020.
- ^ Hamilton R (1790). "IX. An Account of a Distemper, by the common People in England vulgarly called the MUMPS". Transactions of the Royal Society of Edinburgh. 2 (2): 59–72. doi:10.1017/S0263593300027280. PMC 5550187. PMID 29139995.
- ^ Van-Way CW, Marble WS, Thompson G. "Diseases in World War I". The United States World War I Centennial Commission. United States Foundation for the Commemoration of the World Wars. Retrieved 30 أكتوبر 2020.
- ^ أ ب ت ث ج ح خ د خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةramanathan - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةpeltola - ^ أ ب ت ث ج خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةsu - ^ أ ب ت ث خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةdavis - ^ أ ب خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةbeleni - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةdemicheli - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةjapan - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةmasarani - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةlatner - ^ "mumps (n.)". Etymonline. Online Etymology Dictionary. Retrieved 30 أكتوبر 2020.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةkutty - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةpmh - ^ د. عماد محمد زوكار، د. أحمد محمد نوح: الرجع الشامل في اللقاحات، دار علوم القدس، الطبعة الأولى 2005
انظر أيضاً
المراجع
وصلات خارجية
| Classification | |
|---|---|
| External resources |
- الصفحات بخصائص غير محلولة
- Short description is different from Wikidata
- Use dmy dates from October 2020
- Use American English from October 2020
- All Wikipedia articles written in American English
- Pages with empty portal template
- Mumps
- Pediatrics
- Wikipedia medicine articles ready to translate
- Salivary gland pathology
- Wikipedia emergency medicine articles ready to translate
- Vaccine-preventable diseases