حصبة
| Measles | |
|---|---|
| الأسماء الأخرى | Morbilli, rubeola, red measles, English measles[1][2] |
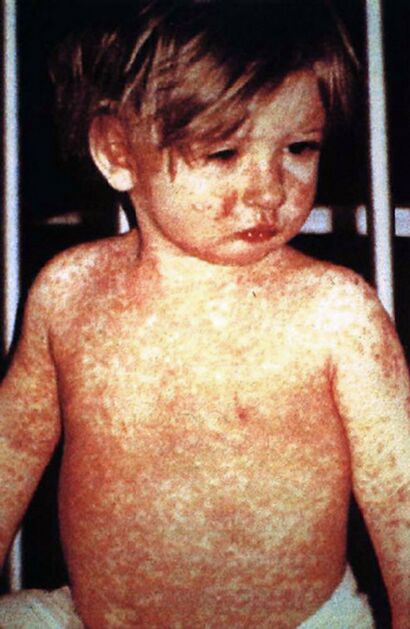 | |
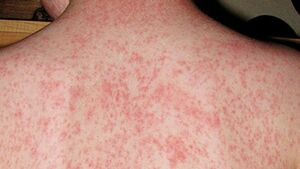
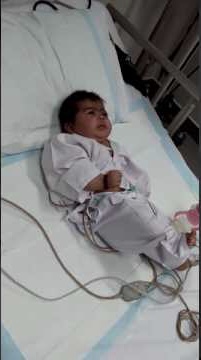
| A child showing a day-four measles rash | |
| التخصص | Infectious disease |
| الأعراض | Fever, cough, runny nose, inflamed eyes, rash[3][4] |
| المضاعفات | Pneumonia, seizures, encephalitis, subacute sclerosing panencephalitis, immunosuppression, hearing loss, blindness[5][6] |
| البداية المعتادة | 10–12 days after exposure[7][8] |
| المدة | 7–10 days[7][8] |
| المسببات | Measles virus[3] |
| الوقاية | Measles vaccine[7] |
| العلاج | Supportive care[7] |
| التردد | 20 million per year[3] |
| الوفيات | 140,000+ (2018)[9][10] |
الحصبة Measles مرض خمجي ڤيروسي حاد، ورد ذكرها في مراجع قديمة ترجع إلى القرن التاسع عشر الميلادي، وقد وصفها الرازي في القرن العاشر الميلادي بأنها (مفزعة أكثر من الجدري).
في عام 1846 وصف بيتر بانوم طور حضانة الحصبة والمناعة الدائمة الناجمة منها. وفي عام 1954، عزل أندرس وبيبلس الڤيروس من الإنسان ومن مزرعة نسيج كلية القرد. وفي عام 1963، تم الترخيص باستخدام أول لقاح حي مضعف في الولايات المتحدة (سلالة إيدمونستون B).
كان الخمج بڤيروس الحصبة قبل توفر اللقاح يصيب كل الأطفال تقريباً، وكان أكثر من 90% من الأطفال بعمر 15 سنة ممنعين ضد الحصبة.
إن الحصبة مرض شائع ومميت في البلاد النامية، وحسب تقديرات منظمة الصحة العالمية حدث عام 2001 حوالي 30-40 مليون حالة حصبة و750,000 وفاة ناجمة عنها.
Measles is an airborne disease which spreads easily from one person to the next through the coughs and sneezes of infected people.[7] It may also be spread through direct contact with mouth or nasal secretions.[11] It is extremely contagious: nine out of ten people who are not immune and share living space with an infected person will be infected.[5] Furthermore, measles's reproductive number estimates vary beyond the frequently cited range of 12 to 18.[12] The NIH quote this 2017 paper saying: "[a] review in 2017 identified feasible measles R0 values of 3.7–203.3".[13] People are infectious to others from four days before to four days after the start of the rash.[5] While often regarded as a childhood illness, it can affect people of any age.[14] Most people do not get the disease more than once.[7] Testing for the measles virus in suspected cases is important for public health efforts.[5] Measles is not known to occur in other animals.[11]
Once a person has become infected, no specific treatment is available,[11] although supportive care may improve outcomes.[7] Such care may include oral rehydration solution (slightly sweet and salty fluids), healthy food, and medications to control the fever.[7][8] Antibiotics should be prescribed if secondary bacterial infections such as ear infections or pneumonia occur.[7][11] Vitamin A supplementation is also recommended for children.[11] Among cases reported in the U.S. between 1985 and 1992, death occurred in only 0.2% of cases,[5] but may be up to 10% in people with malnutrition.[7] Most of those who die from the infection are less than five years old.[11]
The measles vaccine is effective at preventing the disease, is exceptionally safe, and is often delivered in combination with other vaccines.[7][15] Vaccination resulted in an 80% decrease in deaths from measles between 2000 and 2017, with about 85% of children worldwide having received their first dose as of 2017.[11] Measles affects about 20 million people a year,[3] primarily in the developing areas of Africa and Asia.[7] It is one of the leading vaccine-preventable disease causes of death.[16][17] In 1980, 2.6 million people died from measles,[7] and in 1990, 545,000 died due to the disease; by 2014, global vaccination programs had reduced the number of deaths from measles to 73,000.[18][19] Despite these trends, rates of disease and deaths increased from 2017 to 2019 due to a decrease in immunization.[20][21][22]
فيروس الحصبة
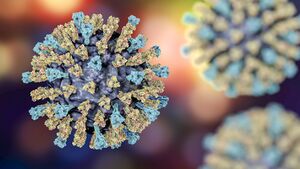
هو ڤيروس نظير مخاطي من جنس الڤيروسة الحصبية، يبلغ قطره 100 - 200 نانومتر. وله لب من نوع RNA وحيد الجديلة، يتكون ڤيروس الحصبة من 6 پروتينات بنيوية، ثلاثة منها مركبة مع الـ RNA، وثلاثة تشارك في بناء غشاء الڤيروس. ويلعب اثنان من پروتينات الغلاف دوراً كبيراً في الإمراض وهما پروتين الالتحام F (Fusion) المسؤول عن التحام الفيروس مع أغشية خلايا المضيف وعن الاختراق الفيروسي للخلية والانحلال الدموي، وبروتين الراصة الدموية Hemagglutinin) H) المسؤول عن امتزاز ]]الفيروس[[ إلى الخلية. يوجد نمط مستضدي واحد فقط لفيروس الحصبة. ورغم أن بعض الدراسات اثبتت حدوث تبدلات في البروتين السكري H لكن لا يبدو أن لهذه التبدلات أهمية من الناحية الوبائية (أي لم يلاحظ حدوث تغير بفعالية اللقاح).
يتعطل فيروس الحصبة بسرعة بعد التعرض للحرارة أو الضوء أو الـ pH الحمضية أو الإثير ether أو التريبسين، ويبقى حياً لفترة قصيرة (أقل من ساعتين في الهواء وعلى الأشياء والسطوح).
الإمراض
الحصبة مرض جهازي، والمكان الرئيس للخمج هو البطانة التنفسية للبلعوم الأنفي، وبعد يومين أو ثلاثة من الغزو والتنسخ في البطانة التنفسية والعقد البلغمية الموضعية، يحدث تفيرس الدم الأولي مع خمج لاحق في الجهاز الشبكي البطاني. وبعد حدوث تنسخ فيروسي آخر في المناطق الموضعية والبعيدة للجهاز الشبكي البطاني يحدث تفيرس دم الثانوي في اليوم 5 - 7 بعد [[الخمج] البدني. وقد يحدث خمج الطرق التنفسية والأعضاء الأخرى خلال هذا التفيرس.
يبدأ طرح فيروس الحصبة من البلعوم الأنفي منذ بداية الطور البادري ويستمر حتى اليوم 3 - 4 بعد بدء الطفح.
فترة الحضانة
يتراوح طور حضانة الحصبة من التعرض وحتى ظهور البوادر بین 10 - 12 يوماً، ومن التعرض حتى بداية الطفح 14 يوماً (يتراوح بين 7 - 18 يوماً).
العلامات والأعراض

يدوم الطور البادري 2 - 4 أيام (يتراوح بين 1-7 أيام)، وهو يتميز بالحمى التي تزداد تدريجياً، وغالباً ما تبلغ ذروتها 103 - 105 فهرنهايت (39.4-40.5) درجة مؤية، يتلوها السعال والزكام (سيلان الأنف) مع أو بدون التهاب الملتحمة.
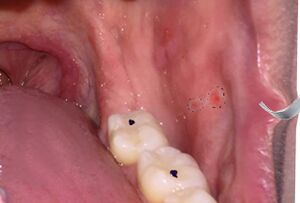
إن بقع كوبليك (Koplik) هي طفح داخلي enanthem، يظهر على الأغشية المخاطية، ويعتبر علامة واصمة pathognomonic للحصبة. تحدث بقع كوبليك قبل يوم أو يومين من ظهور الطفح الجلدي وتستمر لمدة يوم أو يومين بعد ظهوره، وتبدو على شكل بقع منقطة بيضاء مزرقة على خلفية حمراء لماعة في مخاطية الفم.
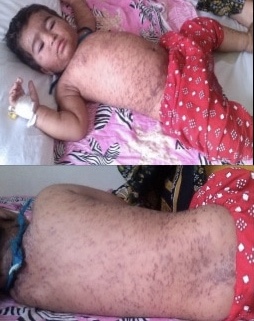
أما طفح الحصبة فهو اندفاع بقعي حطاطي يدوم عادة 5 - 6 أيام، يبدأ عادة من خط الشعر ثم يمتد ليشمل الوجه والقسم العلوي من العنق، وخلال الأيام الثلاثة التالية يمتد الطفح تدريجياً باتجاه الأسفل والخارج وصولاً لليدين والقدمين. تكون الآفات البقمية الحطاطية بشكل عام متميزة منفصلة عن بعضها) وقد تندمج مع بعضها خاصة في الجزء العلوي من الجسم. تبيض هذه الآفات في البداية عند الضغط عليها برأس الإصبع لكن خلال 3-4 أيام تصبح معظم الآفات فاقدة لهذه الخاصية. يحدث توسف دقيق فوق المناطق الأشد إصابة، ويختفي الطفح بنفس الطريقة التي ظهر فيها بداية من الرأس وحتى الأطراف.
تشمل الأعراض الأخرى للحصبة، فقد الشهية والإسهال خاصة عند الرضع واعتلال العقد اللمفية المعمم.
المضاعفات
يحدث اختلاط واحد أو أكثر في حوالي 30% من حالات الحصبة المسجلة، وتكون هذه الاختلاطات أشيع عند الأطفال الأصغر من 5 سنوات وعند البالغين الأكبر من 20 سنة.
حدث الإسهال في 8% من حالات الحصبة المسجلة بين عامي 1985 و 1992، مما يجعله أكثر اختلاطات الحصبة. وسجل التهاب الأذن الوسطى في 7% من الحالات وهو يقتصر تقريباً على الأطفال. أما ذات الرئة فقد سجلت في 6٪ من الحالات وقد تكون فيروسية أو جرثومية، وتعتبر أشيع سبب للوفاة.
سجل التهاب الدماغ الحاد عند حوالي 0,1٪ من الحالات، ويحدث عموماً بعد 6 أيام من بداية الطفح (تراوح الفترة بين 1- 15 يوما)، ويتميز بالحمى والصداع والإقياء وصلابة العنق والتخريش السحائي والنعاس والاختلاجات والسبات.
يبدي فحص السائل الدماغي الشوكي كثرة الخلايا وارتفاع البروتين، وقد تصل نسبة الوفيات إلى ما يقارب 15٪ من الحالات، ويترك الالتهاب بعض أشكال الأذية العصبية عند نسبة تصل إلى 25% من الحالات. أما الاختلاجات (مع أو بدون حرارة) فقد سجلت في 0.6 ٪ - 0.7 ٪ من الحالات.
شكلت نسبة الوفيات الناجمة عن الحصبة في الولايات المتحدة في السنوات الأخيرة ما يقارب 1 - 2 وفاة لكل 1000 حالة حصبة مسجلة، وكبقية اختلاطات الحصبة يكون خطر الوفيات أعلى لدى صفار الأطفال والبالغين. تشكل ذات الرئة 60% من حالات الوفيات، وإن أشيع سبب للوفيات هو ذات الرئة عند الأطفال والتهاب الدماغ الحاد عند البالغين.
إن التهاب الدماغ الشامل المصلب تحت الحاد (SSPE) مرض تنكسي نادر، يصيب الجملة العصبية المركزية، ويعتقد بأنه ناجم عن استمرار خمج الدماغ بفيروس الحصبة. يبلغ وسطي سن البدء 7 سنوات بعد الحصبة (تتراوح المدة بين شهر واحد و27 سنة)، وتبلغ نسبة الحدوث 5 - 10 حالات لكل مليون حالة حصبة مسجلة، وهو يبدأ بشكل مخاتل بتدهور مترق في السلوك والذكاء يليه حدوث الرنح (الخرق awkwardness) والاختلاجات الرمعية العضلية، واخيراً الوفاة. وقد أصبح ال SSPE نادراً جداً منذ بداية ثمانينيات القرن الماضي.
تؤدي الإصابة بالحصبة أثناء الحمل لزيادة خطر حدوث الخداج والإجهاض العفوي ونقص وزن الولادة عند الرضع. وقد ذكر حدوث العيوب الخلقية (ليس لها نموذج تشوه معين) بشكل نادر دون وجود دليل على أن الحصبة هي السبب.
قد تكون الحصبة عند الأشخاص ناقصي المناعة شديدة وذات سير مديد، وهي تقتصر في معظم الحالات على الأشخاص الذين لديهم عوز بالخلايا التائية (بعض مرضى ابيضاض الدم أو اللمفوما أو متلازمة نقص المناعة المكتسب)، وقد تحدث بدون طفح نموذجي، وقد يستمر المرضى بطرح الفيروس لعدة أسابيع بعد المرض الحاد.
لقد أدت الحصبة في البلاد النامية لحدوث معدلات عالية من الهجمات عند الأطفال الذين تقل أعمارهم عن السنة. تكون الحصبة أكثر شدة عند الأطفال سيئي التغذية خاصة المصابين بعوز الفيتامين A. وتتضمن اختلاطاتها الإسهال والجفاف والتهاب الفم وعدم القدرة على تناول الطعام والإنتانات الجرثومية في الجلد وأماكن أخرى. يكون معدل الوفيات عالياً وقد يصل إلى 25% من الحالات. تجدر الإشارة إلى أن الحصبة هي سبب رئيس للعمى أيضا عند الأطفال في افريقيا.
الحصبة اللانموذجية
تحدث الحصبة اللانموذجية فقط عند الأشخاص الذين تلقوا لقاح الحصبة المعطل (المقتول) KMV ثم تعرضوا لاحقاً للنمط البري من فيروس الحصبة. ويقدر أن نحو 600.000 - 900.000 شخص في الولايات المتحدة قد تلقوا اللقاح المقتول KMV بين عامي 1963 - 1967. يؤدي لقاح الحصبة المقتول KMV إلى تحسيس الشخص الملقح تجاه مستضدات لقاح الحصبة دون إعطائه التحصين. ويؤدي الخمج التالي بفيروس الحصبة لحدوث علامات التهاب المصليات المتعدد بفرط التحسس hypersensitivity polyserositis. ويتميز هذا المرض بالحمى وذات الرئة وانصباب الجنب والوذمة، ويكون الطفح عادة بقعياً أو نمشياً petechial، لكن قد يكون له مكونات شروية أو فرفرية أو وعائية، وهو يبدأ في المعصمين أو الكاحلين. يمكن الوقاية من الحصبة اللانموذجية بإعادة التلقيح بلقاح الحصبة الحي. وقد يحدث بعد التلقيح ارتكاسات موضعية معتدلة الشدة أو شديدة مع أو بدون الحمى، وتكون هذه الارتكاسات أقل شدة من تلك المرافقة للخمج بفيروس الحصبة البري.
الحصبة المعدلة
تحدث الحصبة المعدلة بشكل أساسي عند المرضى الذين أعطوا الغلوبولين المناعي IG للوقاية من الحصبة بعد التعرض، وعند صغار الرضع الذين لديهم بعض الأضداد المتبقية من الأم. وهي تتميز بتطاول طور الحضانة وبوادر خفيفة وظهور طفح قليل متناثر لا يستمر إلا فترة قصيرة. وقد سجلت حالات تشبه المرض الخفيف حدثت عند الأشخاص الملقحين سابقاً.
الحصبة النزفية
إن الحصبة النزفية نادراً ما سجل حدوثها في الولايات المتحدة، وهي تميز بالحمى العالية والاختلاجات والهذيان والعسرة التنفسية والنزوف في الجلد والأغشية المخاطية.
التشخيص المخبري
لا يوصي بعزل فيروس الحصبة كطريقة روتينية للتشخيص، ومع ذلك فإن عزل الفيروس هام جداً في الترصد الوبائي الجزيئي. حيث يساعد على تحديد المنشأ الجغرافي للفيروس والسلالات الفيروسية المنتشرة في الولايات المتحدة.
يمكن عزل الفيروس من البول أو رشافات البلعوم الأنفي أو الدم المهبرن heparinized أو مسحات البلعوم.
يجب الحصول على عينات لزرع الفيروس من كل حالة اشتباه سريري بالحصبة وإرسالها إلى المختبر المختص. ولا بد من أخذ العينات السريرية اللازمة لعزل الفيروس في نفس الوقت الذي تؤخذ فيه عينات الفحوص المصلية.
يكون احتمال عزل الفيروس أكبر عندما تؤخذ العينات خلال الأيام الثلاثة الأولى من ظهور الطفح لذلك يجب عدم تأخير اخذ هذه العينات إلى أن يتم تأكيد الحالة بالفحوص المصلية. لا بد من أخذ العينات السريرية خلال 7 ايام من ظهور الطفح، ولا تؤخذ بعد 10 أيام من ظهوره. وهناك بروتوكول خاص لطريقة أخذ هذه العينات.
إن اشيع الفحوص المصلية هو المقايسة المناعية المرتبطة بالإنزيم ELISA أو EIA وهي متوفرة بشكل كبير ومشخصة فيما لو أجريت في الوقت المناسب. وبصورة عامة إذا تعرض الشخص المستعد للإصابة لفيروس اللقاح أو للنمط البري من فيروس الحصبة فإن الأضداد من نوع ال IgM سترتفع عنده في البداية ثم ترتفع الـ IgG. وتكون استجابة IgM عابرة (1 - 2 شهر)، بينما تستمر استجابة IgG عدة سنوات. أما الأشخاص غير المخموجين فيجب ان يكون IgM سلبياً عندهم في حين يكون ال IgG إما سلبياً أو إيجابياً حسب سوابق الإصابة بالخمج.
تحتاج اختبارات ELISA لتحري IgM إلى عينة مصلية واحدة، وتكون مشخصة إذا كانت إيجابية. إن الفحص المرجعي المفضل هو اختبار التقاط IgM الذي تم تطويره في مراكز السيطرة على الأمراض، و يجب استخدامه لإثبات كل حالة حصبة لديها إثبات مخبري آخر . غالباً ما تكون فحوص التقاط IgM الحصبة إيجابية يوم ظهور الطفح، ولكن قد تحدث السلبية الكاذبة في 20% من الحالات خلال الأيام الثلاثة الأولى من ظهور الطفح، ولا بد من إعادة هذه الفحوص السلبية. يبقى IgM قابلاً للكشف لمدة 28 يوماً على الأقل من ظهور الطفح وغالباً ما يبقى لفترة أطول.
توجد عدة فحوص لأضداد الحصبة من نوع IgG و تشمل ELISA، وتثبيط التراص الدموي، واختبارات الأضداد المتألقة غير المباشرة، واختبار التعديل الدقيق microneutralization، واختبار تعديل إرجاع اللويحة plaque reduction neutralization. أما اختبار تثبيت المتممة والذي استعمل بكثرة في السابق فلم يعد يوصى به.
إن اختبار IgG الخاص بالحصبة يتطلب إثبات ارتفاع عيار أضداد فيروس الحصبة، لذلك يجب دوماً أخذ عينتين من المصل، حيث تسحب العينة الأولى بعد ظهور الطفح مباشرة، فيما تسحب العينة الثانية بعدها ب 10 - 30 يوماً. ويجب أن تجرى اختبارات أضداد IgG على كلتا العينتين معاً بنفس الوقت، كما يجب استعمال نفس نموذج الاختبار على كلتا العينتين. هذا وتعتمد المعايير النوعية لإثبات زيادة العيار على الاختبار .
تتطلب اختبارات أضداد IgG أخذ عينتين من المصل، ولا يمكن تأكيد التشخيص إلا بعد أخذ العينة الثانية، لذلك تعتبر اختبارات IgM هي المفضلة بشكل عام لتأكيد تشخيص الحصبة.
الوبائيات
- الحدوث: تنتشر الحصبة في جميع أنحاء العالم، ومع ذلك فقد تم تحقيق انقطاع الانتقال الواطن (المحلي indigenous) للحصبة في الولايات المتحدة و الأجزاء الأخرى لنصف الكرة الأرضية الغربي.
- المستودع: إن الحصبة مرض إنساني، ولا يوجد لها مستودع حيواني معروف، كذلك لم تسجل حالات حمل لا عرضية.
- الانتقال: تنتقل الحصبة مبدئياً من شخص لآخر عبرالقطيرات droplets التنفسية الكبيرة، وقد سجل حدوث الانتقال الهوائي عبر ارذاذ النويات الدقيقة في الأماكن المغلقة (مثل غرفة الفحص) لمدة تصل إلى الساعتين بعد مغادرة مريض الحصبة.
- النموذج الفصلي: يحدث مرض الحصبة في المناطق الحارة بشكل رئيس في أواخر الشتاء والربيع.
- السراية: الحصبة مرض عالي السراية، حيث يصل معدل الهجمات الثانوية عند الأشخاص المستعدين لأكثر من 90%. يمكن للحصبة أن تنتقل خلال مدة 4 أيام قبل ظهور الطفح ولمدة 4 أيام بعده، وتحدث السراية الكبرى في الفترة بين بداية البوادر وحتى اليوم الثالث أو الرابع من ظهور الطفح.
الاتجاهات العامة في الولايات المتحدة
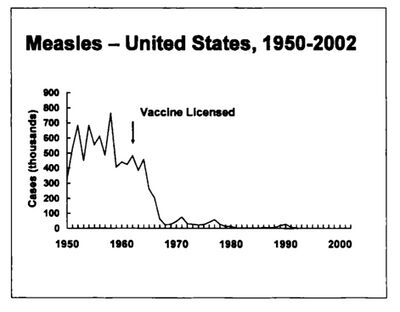
سجل سنوياً قبل عام 1963 ما يقارب 500.000 حالة حصبة و 500 حالة وفاة مع دورات وبائية كل 2 - 3 سنوات. و قدر عدد الحالات الحقيقي ب 3-4 مليون حالة سنوياً، تكون الحصبة في عمر 6 سنوات قد حدثت عند أكثر من 50% من الأطفال وتصل هذه النسبة إلى أكثر من 95% بعمر 15 سنة، ووجد اكبر انتشار للحصبة بعمر 5- 9 سنوات حيث تشكل نسبة تفوق 50% من الحالات المسجلة.
وبعد الترخيص باستعمال اللقاح عام 1963 انخفض انتشار الحصبة بأكثر من 98٪، ولم تعد تحدث الدورات الوبائية كل 2 - 3 سنوات. وبسبب هذا النجاح فقد تم في عام 1978 وضع برنامج للتخلص من الحصبة في الولايات المتحدة بحلول الأول من تشرين الأول 1982. لم يتحقق هذا الهدف عام 1982، لكن في عام 1983 لم يسجل إلا 1497حالة (6 ,0 حالة لكل 100 ألف نسمة)، وهذا أخفض عدد إجمالي الحالات الحصبة سجل حتى ذلك الوقت.
في الفترة بين 1980 - 1988 حدث 57% من الحالات وسطياً عند أشخاص بسن المدرسة أعمارهم بين 5 – 19 سنة)، و 29% من الحالات وسطياً عند الأطفال دون عمر 5 سنوات، و 78 من الحالات وسطياً عند الرضع دون عمر السنة من العمر.
أما في الفترة بين 1985 - 1988 فحدثت 42% من الحالات عند أشخاص تلقحوا بعمر السنة أو بعده. وخلال هذه المدة أيضاً وجد أن 68% من الحالات التي حدثت لدى الأطفال بسن المدرسة (5 - 19 سنة) قد تلقت تلقيحاً مناسباً، وأن حدوث الحصبة عند أطفال ملقحين سابقاً يستدعي وضع توصية بإعطاء جرعة ثانية من اللقاح لهذه الفئة العمرية.
حدثت زيادة مفاجئة في حالات الحصبة بين عامي 1989 – 1991 وكان السبب الرئيس لذلك هو التغطية الناقصة للتلقيح عند الأطفال بسن ما قبل المدرسة، حيث تبين أن 50% فقط من الأطفال تلقوا تلقيح ضد الحصبة بعمر سنتين. وربما تكون هناك زيادة في استعداد الرضع دون عمر السنة من العمر، فقد وجد أن العديد من أمهات الرضع الذين أصيبوا بالحصبة كن من الشابات، وفي معظم الحالات كانت المناعة ضد الحصبة لديهن ناجمة عن التلقيح وليس عن الخمج بفيروس الحصبة البري. ونتيجة لذلك كانت كمية الأضداد التي انتقلت عبر المشيمة للجنين قليلة مقارنة مع الأضداد في حالة الخمج الطبيعي (التي تكون مرتفعة). تؤدي كمية الأضداد القليلة المناعة تتناقص بسرعة كبيرة مما يجعل الرضع مستعدين للإصابة بأعمار أصغر مما كانت عليه في السابق.
لقد أدت الجهود المكثفة المبذولة لتلقيح الأطفال بسن ما قبل المدرسة إلى تناقص حالات الحصبة. حيث ازدادت مستويات التلقيح ضد الحصبة عند الأطفال بعمر السنتين من 70 ٪ عام 1990 إلى 91٪ عام 1997.
ومنذ عام 1993 لم تسجل إلا حالات قليلة (أقل من 500 حالة في السنة، وبدءاً من عام 1997 لم يسجل إلا أقل من 200 حالة سنوياً، وفي عام 2002 انخفض إجمالي الحالات إلى 44 حالة في السنة .
إن الوبائيات المتوفرة ومعطيات علم الفيروسات اقترحت بقوة أن انتقال الحصبة في الولايات المتحدة قد توقف. وأن معظم الحالات الآن مستوردة من بلدان أخرى أو مرتبطة بحالات مستوردة، حيث تأتي معظم الحالات المستوردة من [[آسيا]٢ وأوروبا، وتحدث الإصابات عند الأمريكيين المسافرين للخارج وعند القادمين للولايات المتحدة من بلدان أخرى. لقد أصبح انتشار الحصبة الآن قليلاً جداً في أمريكا اللاتينية ومنطقة البحر الكاريبي بفضل برنامج التلقيح المشدد ضد الحصبة المطبق من قبل منظمة الصحة الأمريكية العامة، وعلى ما يبدو فإن التخلص من الحصبةفي [[أمريكا]٢ أصبح هدفاً قابلاً للتحقيق.
منذ منتصف تسعينيات القرن الماضي لم يعد هناك مجموعة عمرية مسيطرة على حالات الحصبة المسجلة. و أصبح معدل الحالات المرتفع الآن يحدث عند البالغين مقارنة مع السابق ففي عام 1973 كان الأشخاص الذين تزيد أعمارهم عن 20 سنة يشكلون ما يقارب 3% من الحالات فقط، مقارنة مع 24% عام 1994، و 48% في عام 2001.
لقد تغير حجم وتركيب جائحات الحصبة منذ ثمانينيات القرن الماضي. وحدثت أغلبية الحائحات قبل عام 1989 عند طلاب المرحلتين المتوسطة والثانوية وطلاب الكليات، وكان (95 %) من الأشخاص الذين أصيبوا بالخمج خلال تلك الجائحات قد تلقوا سابقاً جرعة واحدة من لقاح الحصبة. وفي عام 1989 وضعت توصية بإعطاء جرعة ثانية من لقاح الحصبة للأطفال الذين هم في سن المدرسة. وبالنتيجة أصبحت جائحات الحصبة الآن غير شائعة في المدارس.
التصنيف السريري لحالات الحصبة
- الحالة المشتبهة Suspect case: هي الشخص المصاب بمرض مترافق مع حمى وطفح بقعي
حطاطي معمم .
- الحالة المرجحة Probable case: توافق تعریف حالة الحصبة وهي طفح بقعي حطاطي
معمم، يستمر 3 أيام مع حمى تعادل 38.30 درجة مؤية (101) فهرنهايت أو أكثر مع سعال أو زکام أو التهاب ملتحمة دون وجود اختبارات مصلية أو فيروسية مساعدة، ودون وجود ارتباط وبائي مع حالة مؤكدة .
- الحالة المؤكدة Confirmed case: توافق تعریف حالة الحصبة مع وجود ارتباط وبائي مع
حالة أخرى مؤكدة أو مرجحة، أو أنها مثبتة مخبرياً. ولا تحتاج الحالة المثبتة مخبرياً للتوافق مع تعريف الحالة السريرية.
التصنيف الوبائي لحالات الحصبة
- الحالة المستوردة دولياً Imported case: هي التي يكون مصدرها من خارج البلد، يبدأ ظهور الطفح بعد 21 يوماً من دخول البلد، ولا يمكن ربط المرض مع انتقال محلي.
- الحالة الواطنة(المحلية) Indigenous case: هي أية حالة لا يمكن إثبات أنها مستوردة، وتوجد عدة أصناف لها.
لقاح الحصبة
 مقالة مفصلة: لقاح الحصبة
مقالة مفصلة: لقاح الحصبة
هو لقاح يقي من الإصابة بمرض الحصبة، وهو عادة لا يمنح التحصين الكافي للوقاية بعد الجرعة الأولى، وإنما يحتاج إلى جرعة ثانية معززة.
تم عزل فيروس الحصبة أول مرة بواسطة جون أندرس John Anders عام 1954، أما أول لقاح حصبة فتم ترخيصه في عام 1963، وتم في ذلك العام ترخیص استعمال كلا اللقاحين المعطل (المقتول) والحي المضعف (سلالة إيدمونستون ب Edmonston B) في الولايات المتحدة. لقد تم سحب اللقاح المقتول من التداول عام 1967؛ لأنه لم يحصن ضد الخمج بفيروس الحصبة، علاوة على ذلك كثيراً ما تطور لدى الأشخاص الذين تلقوا هذا اللقاح متلازمة خاصة من الحصبة اللانموذجية عندما أصيبوا بفيروس الحصبة البري.
أما القاح إيدمونستون B الأصلي فتم سحبه من التداول عام 1975؛ بسبب شيوع ترافقه مع الحمى والطفح عند الملقحين به. وفي عام 1965 أدخل لأول مرة لقاح حي مضعف آخر هو (سلالة شوارز Schwarz strain)، لكن استعماله لم يدم طويلاً في الولايات المتحدة. وفي عام 1968 تم ترخيص لقاح أخر من سلالة حية مضعفة (سلالة إيدمونستون- أندرس). تحدث هذه اللقاحات الحية المضعفة ارتكاسات أقل بكثير من تلك التي يحدثها لقاح إيدمونستون B الأصلي.
الخصائص
إن لقاح الحصبة الوحيد المتوفر الآن في الولايات المتحدة هو سلالة أدمونستون - أندرس الحية المضعفة بشدة (دعي سابقة موراتن Moraten). وهو يتوفر على شكل مستحضر مستضدي وحيد أو مشترك مع لقاح الحصبة الألمانية أو مشترك مع لقاح النكاف والحصبة الألمانية.
توصي اللجنة الاستشارية حول ممارسات التمنيع ACIP باستعمال اللقاح المشترك المكون من الحصبة والنكاف والحصبة الألمانية MMR عندما يوجد استطباب لأي من مكوناته.
يحضر لقاح الحصبة بزرع الفيروس في الأرومات الليفية لجنين الدجاج. أما لقاح MMR فيكون بشكل بودرة مجفدة lyophylized (مجففة بالتجميد freeze - dried)، ويتم تحضير اللقاح باستعمال ماء معقم خال من المواد الحافظة. يحتوي اللقاح كمية قليلة من الألبومين البشري: نتنيوميسين والسوربيتول والجيلاتين.
جدول التلقيح والاستعمال
يوصي بإعطاء جميع الأطفال روتينياً جرعتين من لقاح الحصبة على شكل اللقاح المشترك MMR وبفاصل لا يقل عن 4 أسابيع بينهما. يجب على كل الأشخاص الذين ولدوا عام 1957 أو بعده أن يكون لديهم مستندات تثبت انهم تلقوا على الأقل جرعة واحدة من لقاح MMR أو اي دليل آخر على تمنيعهم ضد الحصبة. كذلك يجب أن يتلقى بعض المراهقين والبالغين جرعتين من لقاح MMR.
يجب أن تعطي الجرعة الأولى من لقاح MMR بعد عمر السنة، ولا تحسب أية جرعة لقاح يحتوي على الحصبة إذا أعطيت قبل عمر 12 شهراً. حيث لا بد في هذه الحالة من إعادة التلقيح بإعطاء جرعتين من لقاح MMR، على أن تعطى الجرعة الأولى بعمر لا يقل عن 12 شهراً.
يوصي بإعطاء الجرعة الثانية من MMR لإنتاج مناعة عند الأشخاص الذين فشلوا في الاستجابة للجرعة الأولى من اللقاح. ويجب أن تعطي الجرعة الثانية من MMR روتينياً بعمر 4 - 6 سنوات قبل دخول الطفل إلى روضة الأطفال أو المرحلة الابتدائية. يمكن اعتبار الزيارة الصحية ما قبل سن المراهقة بعمر 11 - 12 سنة فرصة سانحة للتحقق من الحالة التلقيحية ولإعطاء الجرعة الثانية من لقاح MMR للأطفال الذين لم يتلقوا بعد جرعتين من MMR.
يمكن إعطاء الجرعة الثانية من لقاح MMR بعد شهر واحد (28 يوما، على الأقل من الجرعة لأولى). وإن الأطفال الذين كانوا قد تلقوا جرعتين من لقاح MMR بفاصل لا يقل عن 4 أسابيع على ألا تكون الجرعة الأولى قد أعطيت قبل عمر السنة ليسوا بحاجة لجرعة إضافية عند دخولهم المدرسة.
أما الأطفال الذين ليس لديهم إثبات على تلقيهم اللقاحات المناسبة ضد الحصبة والحصبة الألمانية]] والنكاف أو دليل أخر مقبول يشير لوجود مناعة لديهم ضد هذه الأمراض فيجب إعطاؤهم الجرعة الأولى من MMR قبل دخولهم المدرسة. أما الجرعة الثانية فتعطى بأسرع وقت ممكن وبفاصل زمني عن الجرعة الأولى لا يقل عن 4 أسابيع.
مصادر
- [23].
الهامش
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةMil2015 - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةStan2002 - ^ أ ب ت ث خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةMM2014 - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةCDC2014SS - ^ أ ب ت ث ج Atkinson W (2011). Epidemiology and Prevention of Vaccine-Preventable Diseases (12 ed.). Public Health Foundation. pp. 301–23. ISBN 9780983263135. Archived from the original on 7 February 2015. Retrieved 5 February 2015.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةRot2016 - ^ أ ب ت ث ج ح خ د ذ ر ز س ش خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةWHO2014 - ^ أ ب ت خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةConn2014 - ^ Joint News Release (2019-12-05). "More than 140,000 die from measles as cases surge worldwide". who.int. Archived from the original on 6 August 2020. Retrieved 4 September 2020.
- ^ "Global Measles Outbreaks". cdc.gov. 2020-08-17. Archived from the original on 7 September 2020. Retrieved 4 September 2020.
- ^ أ ب ت ث ج ح خ "Measles fact sheet". World Health Organization. Archived from the original on 2019-06-01. Retrieved 2019-05-20.
- ^ Guerra, Fiona M.; Bolotin, Shelly; Lim, Gillian; Heffernan, Jane; Deeks, Shelley L.; Li, Ye; Crowcroft, Natasha S. (December 2017). "The basic reproduction number (R0) of measles: a systematic review". The Lancet. Infectious Diseases. 17 (12): e420–e428. doi:10.1016/S1473-3099(17)30307-9. ISSN 1474-4457. PMID 28757186. Archived from the original on 30 March 2023. Retrieved 7 December 2020.
- ^ Delamater, P. L.; Street, E. J.; Leslie, T. F.; Yang, Y. T.; Jacobsen, K. H. (2019). "Complexity of the Basic Reproduction Number (R0)". Emerging Infectious Diseases. NIH website. 25 (1): 1–4. doi:10.3201/eid2501.171901. PMC 6302597. PMID 30560777.
[a] review in 2017 identified feasible measles R0 values of 3.7–203.3
- ^ Chen S.S.P. (22 February 2018). Measles. Medscape. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. https://emedicine.medscape.com/article/966220-overview. Retrieved on 13 May 2020. - ^ Russell, SJ; Babovic-Vuksanovic, D; Bexon, A; Cattaneo, R; Dingli, D; Dispenzieri, A; Deyle, DR; Federspiel, MJ; Fielding, A; Galanis, E (September 2019). "Oncolytic Measles Virotherapy and Opposition to Measles Vaccination". Mayo Clinic Proceedings. 94 (9): 1834–39. doi:10.1016/j.mayocp.2019.05.006. PMC 6800178. PMID 31235278.
- ^ Kabra SK, Lodha R (August 2013). "Antibiotics for preventing complications in children with measles". The Cochrane Database of Systematic Reviews. 8 (8): CD001477. doi:10.1002/14651858.CD001477.pub4. PMC 7055587. PMID 23943263.
- ^ "Despite the availability of a safe, effective and inexpensive vaccine for more than 40 years, measles remains a leading vaccine-preventable cause of childhood deaths" (PDF). Archived (PDF) from the original on 12 December 2019. Retrieved 16 February 2019.
- ^ GBD 2015 Mortality and Causes of Death Collaborators (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ^ GBD 2013 Mortality Causes of Death Collaborators (January 2015). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. 385 (9963): 117–71. doi:10.1016/S0140-6736(14)61682-2. PMC 4340604. PMID 25530442.
- ^ "Measles cases spike globally due to gaps in vaccination coverage". World Health Organization (WHO). 29 November 2018. Archived from the original on 24 December 2018. Retrieved 21 December 2018.
- ^ "U.S. measles cases surge nearly 20 percent in early April, CDC says". Reuters. 16 April 2019. Archived from the original on 15 April 2019. Retrieved 16 April 2019.
- ^ "Measles – European Region". World Health Organization (WHO). Archived from the original on 8 May 2019. Retrieved 8 May 2019.
- ^ د. عماد محمد زوكار، د. أحمد محمد نوح: الرجع الشامل في اللقاحات، دار علوم القدس، الطبعة الأولى 2005
وصلات خارجية
- Initiative for Vaccine Research (IVR): Measles, World Health Organization (WHO)
- Measles FAQ U.S. Centers for Disease Control and Prevention (CDC)
- Case of an adult male with measles (facial photo)
- Pictures of measles Archived 26 يوليو 2010 at the Wayback Machine
- Virus Pathogen Database and Analysis Resource (ViPR): Paramyxoviridae
| Classification | |
|---|---|
| External resources |
قالب:Numbered Diseases of Childhood قالب:Eradication of infectious disease
- الصفحات بخصائص غير محلولة
- Short description is different from Wikidata
- Measles
- Atypical pneumonias
- Airborne diseases
- Infectious diseases with eradication efforts
- Pediatrics
- Vaccine-preventable diseases
- Virus-related cutaneous conditions
- Wikipedia emergency medicine articles ready to translate
- Wikipedia medicine articles ready to translate
- Articles containing video clips
- فيروسات سلبية أحادية
- طب الأطفال
- أمراض معدية
- جسم الإنسان
- الحصبة