ثنائي ثيونات الصوديوم
| |
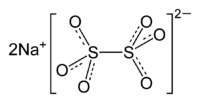
| Ball-and-stick model of the component ions | |
| الأسماء | |
|---|---|
| اسم أيوپاك
Sodium dithionate
| |
| أسماء أخرى
Sodium hyposulfate
| |
| المُعرِّفات | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.028.682 |
| رقم EC |
|
PubChem CID
|
|
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | Na2S2O6 |
| كتلة مولية | 206.106 g/mol |
| المظهر | White crystalline powder |
| الكثافة | 2.19 g/cm3 |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | 6.27 g/100 mL (0 °C) 15.12 g/100 mL (20 °C) 64.74 g/100 mL (100 °C) |
| المخاطر | |
| NFPA 704 (معيـَّن النار) | |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
ثنائي ثيونات الصوديوم Sodium dithionate مركب كيميائي له الصيغة Na2S2O6، ويكون على شكل بلورات بيضاء رمادية. يعرف أيضاً باسم هايپوسلفات الصوديوم (تحت كبريتات الصوديوم)، وميتابايسلفات الصوديوم.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص
- لمركب ثنائي ثيونات الصوديوم ثباتية جيدة، فهو يقاوم المؤكسدات.
- لبلورات ثنائي ثيونات الصوديوم بينية متوازي مستطيلات.
التحضير
يحضر ثنائي ثيونات الصوديوم من تفاعل أكسدة بيكبريتيت الصوديوم بواسطة ثاني أكسيد المنغنيز [1]
- 2 NaHSO3 + MnO2 → Na2S2O6 + Mn(OH)2
أو يمكن أن يحضر من تفاعل كبريتيت الصوديوم مع أيون الفضة.
- Na2SO3 + 2 Ag + + SO −3 → Na2S2O6 + 2Ag
المراجع
- ^ W. G. Palmer (1954). Experimental Inorganic Chemistry. CUP Archive. pp. 361–365. ISBN 052105902X.
الكلمات الدالة:
