لولب ألفا
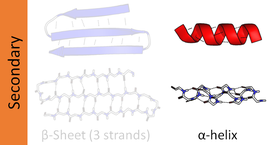
لولب ألفا alpha helix (α-helix)، هو النمط الشائع في البنية الثانوية للپروتينات وعبارة عن تركيبة لولبية-تجاه اليمين (أي لولب) تعطي فيه كل مجموعة أمين-N−H أساسية رابطة هيدروجينية إلى [[مجموعة C=O أساسية من الحمض الأميني الواقع على البقايا الثلاثة أو الأربعة السابقة على امتداد تسلسل الپروتين.
يطلق على لولب ألفا أيضاً لولب ألفا پولينگ-كوري-بارنسن الكلاسيكي. الاسم 3.613-helix يستخدم أيضاً للإشارة إلى هذا النوع من اللوالب، معطياً الرقم المتوسط للبقايا لكل لفة لولبية، حيث يوجد 13 ذرة في كل حلقة ناتجة عن الرابطة الهيدروجينية.
من بين البنى الموضعية للپروتينات، يعتبر لولب ألفا أكثرها انتظاماً والأكثر قابلية للتنبؤ من التسلسل، وكذلك الأكثر انتشاراً.
الاكتشاف
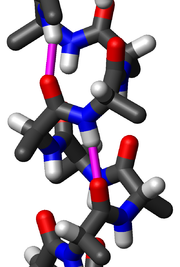
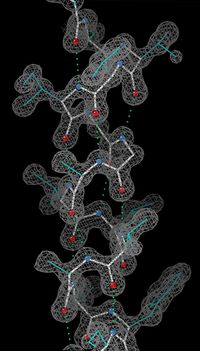
Side view of an α-helix of alanine residues in atomic detail. Two hydrogen bonds for the same peptide group are highlighted in magenta; the H to O distance is about 2 Å (0.20 nm). The proteinhain runs upward here; that is, its N-terminus is at the bottom and its C-terminus at the top. Note that the sidechains (black stubs) angle slightly downward, toward the N-terminus, while the peptide oxygens (red) point up and the peptide NHs (blue with grey stubs) point down.
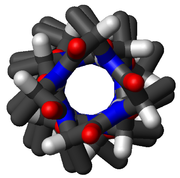
Top view of the same helix shown above. Four carbonyl groups are pointing upwards toward the viewer, spaced roughly 100° apart on the circle, corresponding to 3.6 amino-acid residues per turn of the helix.
البنية
الهندسة والرابطة الهيدروجينية
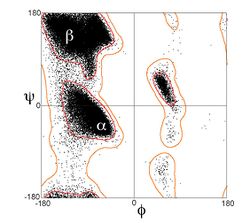
Ramachandran plot (φ, ψ plot), with data points for α-helical residues forming a dense diagonal cluster below and left of center, around the global energy minimum for backbone conformation.[1]
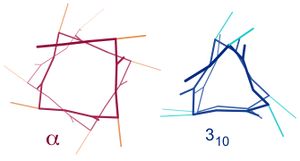
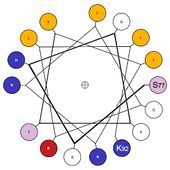
المخططات ثنائية الأبعاد لتمثيل لوالب ألفا
الاستقرار
التحديد التجريبي
نزعات الحمض الأميني
جدول نزعات لولب ألفا تجاه الحمض الأميني القياسي
الفرق في الطاقة الحرة لكل بقية[2] الحمض الأميني 3-
لتر1-
لترالفرق اللولبي ك.س/مول ك.ج/مول ألانين Ala A 0.00 0.00 أرجنين Arg R 0.21 0.88 أسپاراجين Asn N 0.65 2.72 حمض الأسپارتيك Asp D 0.69 2.89 سيستين Cys C 0.68 2.85 حمض الگلوتاميك Glu E 0.40 1.67 گلوتامين Gln Q 0.39 1.63 گليسين Gly G 1.00 4.18 هيستيدين His H 0.61 2.55 آيزوليوسين Ile I 0.41 1.72 ليوسين Leu L 0.21 0.88 ليسين Lys K 0.26 1.09 مثيونين Met M 0.24 1.00 فنايلألانين Phe F 0.54 2.26 پرولين Pro P 3.16 13.22 سيرين Ser S 0.50 2.09 ثريونين Thr T 0.66 2.76 تريپتوفان Trp W 0.49 2.05 تيروسين Tyr Y 0.53 2.22 ڤالين Val V 0.61 2.55
العزم ثنائي الأقطاب
اللفائف الملتفة
التجمعات واسعة النطاق

The Hemoglobin molecule has four heme-binding subunits, each made largely of α-helices.
الأدوار الوظيفية
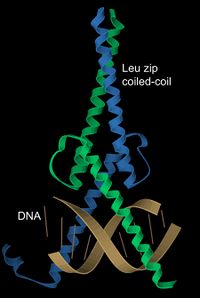
Leucine zipper coiled-coil helices & DNA-binding helices: transcription factor Max (PDB file 1HLO)
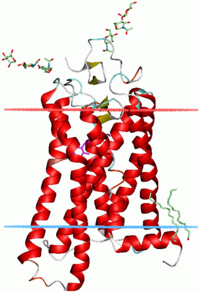
Bovine rhodopsin (PDB file 1GZM), with a bundle of seven helices crossing the membrane (membrane surfaces marked by horizontal lines)
ربط الدنا
مد الغشاء
الخصائص الميكانيكية
السمات الديناميكية
Helix–coil transition
في الفن

Julian Voss-Andreae's Alpha Helix for Linus Pauling (2004), powder coated steel, height 10 ft (3 m). The sculpture stands in front of Pauling's childhood home on 3945 SE Hawthorne Boulevard in Portland, Oregon, USA.
انظر أيضاً
- لولب 310
- لولب پاي
- Beta sheet
- Davydov soliton
- Folding (chemistry)
- Knobs into holes packing
- قالب:Proteopedia
المصادر
- ^ Lovell SC, Davis IW, Arendall WB, de Bakker PI, Word JM, Prisant MG, Richardson JS, Richardson DC (February 2003). "Structure validation by Calpha geometry: phi,psi and Cbeta deviation". Proteins. 50 (3): 437–50. doi:10.1002/prot.10286. PMID 12557186.
- ^ Pace, C. Nick; Scholtz, J. Martin (1998). "A Helix Propensity Scale Based on Experimental Studies of Peptides and Proteins". Biophysical Journal. Vol. 75. pp. 422–427. Bibcode:1998BpJ....75..422N. doi:10.1016/s0006-3495(98)77529-0.
قراءات إضافية
- Tooze, John; Brändén, Carl-Ivar (1999). Introduction to protein structure. New York: Garland Pub. ISBN 0-8153-2304-2.
{{cite book}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help). - Eisenberg D (September 2003). "The discovery of the alpha-helix and beta-sheet, the principal structural features of proteins". Proceedings of the National Academy of Sciences of the United States of America. 100 (20): 11207–10. Bibcode:2003PNAS..10011207E. doi:10.1073/pnas.2034522100. PMC 208735. PMID 12966187.
- Astbury, WT; Woods, HJ (1931). "The Molecular Weights of Proteins". Nature. 127 (3209): 663–665. Bibcode:1931Natur.127..663A. doi:10.1038/127663b0.
{{cite journal}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - Astbury, WT; Street, A (1931). "X-ray studies of the structures of hair, wool and related fibres. I. General". Trans. R. Soc. Lond. A230: 75–101.
{{cite journal}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - Astbury, WT (1933). "Some Problems in the X-ray Analysis of the Structure of Animal Hairs and Other Protein Fibers". Trans. Faraday Soc. 29 (140): 193–211. doi:10.1039/tf9332900193.
{{cite journal}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - Astbury, WT; Woods, HJ (1934). "X-ray studies of the structures of hair, wool and related fibres. II. The molecular structure and elastic properties of hair keratin". Trans. R. Soc. Lond. A232: 333–394.
{{cite journal}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - Astbury, WT; Sisson, WA (1935). "X-ray studies of the structures of hair, wool and related fibres. III. The configuration of the keratin molecule and its orientation in the biological cell". Proceedings of the Royal Society. A150: 533–551.
{{cite journal}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - Sugeta, H; Miyazawa, T (1967). "General Method for Calculating Helical Parameters of Polymer Chains from Bond Lengths, Bond Angles, and Internal-Rotation Angles". Biopolymers. 5 (7): 673–679. doi:10.1002/bip.1967.360050708.
{{cite journal}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - Wada A (1976). "The alpha-helix as an electric macro-dipole". Advances in Biophysics: 1–63. PMID 797240.
- Chothia C, Levitt M, Richardson D (October 1977). "Structure of proteins: packing of alpha-helices and pleated sheets". Proceedings of the National Academy of Sciences of the United States of America. 74 (10): 4130–4. Bibcode:1977PNAS...74.4130C. doi:10.1073/pnas.74.10.4130. PMC 431889. PMID 270659.
- Chothia C, Levitt M, Richardson D (January 1981). "Helix to helix packing in proteins". Journal of Molecular Biology. 145 (1): 215–50. doi:10.1016/0022-2836(81)90341-7. PMID 7265198.
- Hol WG (1985). "The role of the alpha-helix dipole in protein function and structure". Progress in Biophysics and Molecular Biology. 45 (3): 149–95. doi:10.1016/0079-6107(85)90001-X. PMID 3892583.
- Barlow DJ, Thornton JM (June 1988). "Helix geometry in proteins". Journal of Molecular Biology. 201 (3): 601–19. doi:10.1016/0022-2836(88)90641-9. PMID 3418712.
- Murzin AG, Finkelstein AV (December 1988). "General architecture of the alpha-helical globule". Journal of Molecular Biology. 204 (3): 749–69. doi:10.1016/0022-2836(88)90366-X. PMID 3225849.
وصلات خارجية
This article may include material from Wikimedia licensed under CC BY-SA 4.0. Please comply with the license terms.