رحم اصطناعي
 |
الرحم الاصطناعي artificial uterus أو artificial womb هو جهاز سيسمح بالحمل خارج الجسم[2] بإنماء جنين خارج جسم الكائن الحي الذي، في المعتاد، يحمل الجنين حتى يولد.
الرحم الاصطناعي، كعضو بديل، سيكون له العديد من التطبيقات. يمكن استخدامه لمساعدة الأزواج من الذكور أو الإناث في نمو الجنين.[2] يمكن القيام بذلك كتحويل من رحم طبيعي إلى رحم اصطناعي، وبالتالي نقل عتبة قابلية الجنين للحياة إلى مرحلة مبكرة من الحمل.[2] بهذا المعنى، يمكن اعتباره حاضنة لحديث الولادة بوظائف ممتدة للغاية. يمكن استخدامه أيضًا لبدء نمو الجنين.[2] يمكن أن يساعد الرحم الاصطناعي أيضًا في جعل إجراءات جراحة الجنين خيارًا في مرحلة مبكرة بدلاً من الاضطرار إلى تأجيلها حتى نهاية الحمل.[2]
في 2016، نشر العلماء دراستين تتعلقان بتطور الأجنة البشرية لمدة ثلاثة عشر يومًا في بيئة الرحم الخارجي.[3][4]
حاليًا ، تمنع قاعدة الـ 14 يومًا لبقاء الأجنة البشرية في أرحام اصطناعية لمدة تزيد عن 14 يومًا. تم تقنين هذه القاعدة إلى قانون في اثني عشر بلد.[5]
في 2017، نشر باحثو الأجنة في مستشفى الأطفال في فيلادلفيا دراسة تظهر أنهم قد قاموا بإنماء أجنة الحملان المبتسرة لمدة أربعة أسابيع في نظام دعم الحياة خارج الرحم.[1][6][7]
المكونات
الرحم الاصطناعي، يشار له أحياناً باسم "الرحم الخارجي" exowomb)،[8]، يجب أن توفر العناصر الغذائية والأكسجين لتغذية الجنين، وكذلك التخلص من الفضلات. قد يشمل نطاق الرحم الاصطناعي (أو "نظام الرحم الاصطناعي" للتأكيد على نطاق أوسع) أيضًا الواجهة التي تخدم الوظيفة التي توفرها المشيمة، وهو خزان يحيط بالجنين يعمل مثل الكيس الأمنيوسي، وكذلك الحبل السري.
التغذية والإمداد بالأكسجين والتخلص من الفضلات
قد تستمر المرأة في توفير العناصر الغذائية والتخلص من الفضلات إذا كان الرحم الاصطناعي متصلاً بها.[2] قد توفر أيضًا حماية مناعية ضد الأمراض عن طريق تمرير الأجسام المضادة لگلوبولين المناعي ج إلى الجنين الحي أو الجنين.[2]
"الإمداد والتخلص الاصطناعي" لهما ميزة محتملة تتمثل في السماح للجنين بالتطور في بيئة لا تتأثر بوجود مرض أو ملوثات بيئية أو كحول أو عقاقير قد يكون لدى الإنسان في الدورة الدموية.[2] لا يوجد خطر لحدوث رد فعل مناعي تجاه الجنين الحي أو الجنين الذي يمكن أن ينشأ من عدم كفاية التحمل المناعي في الحمل.[2] تتضمن بعض الوظائف الفردية للمورد الاصطناعي والمتخلص:
- يمكن التخلص من الفضلات عن طريق الغسيل الكلوي.[2]
- من أجل إمداد الجنين الحي أو الجنين بالأكسجين، والتخلص من ثاني أكسيد الكربون، تعتبر أكسجة الغشاء خارج الجسم (ECMO) تقنية فعالة، حيث نجحت في الحفاظ على أجنة الماعز على قيد الحياة لمدة تصل إلى 237 ساعة في الخزانات الأمنيوسية.[9] ECMO هي تقنية تستخدم حاليًا في وحدات العناية المركزة لحديثي الولادة لعلاج الرضع الناضجين الذين يعانون من مشاكل طبية معينة تؤدي إلى عدم قدرة الرضيع على البقاء على قيد الحياة من خلال تبادل الغازات باستخدام الرئتين.[10] ومع ذلك، فإن الأوعية الدموية الدماغية والمصفوفة الجرثومية يتطوران بشكل ضعيف في الأجنة، وبالتالي، هناك مخاطر عالية غير مقبولة لحدوث النزف داخل البطيني (IVH) إذا استخدمت ECMO في فترة حمل أقل من 32 أسبوع.[11] أُقترح التنفس السائل كطريقة بديلة للأكسجين، أو على الأقل توفير مرحلة وسيطة بين الرحم والتنفس في الهواء الطلق.[2]
- بالنسبة للتغذية الاصطناعية، تعتبر التقنيات الحالية مشكلة.[2] التغذية الوريدية الكلية، كما تمت دراسته على الرضع المصابين بمتلازمة الأمعاء القصيرة الشديدة، تبلغ نسبة بقائهم على قيد الحياة 5 سنوات إلى 20% تقريباً.[2][12]
- لا تزال القضايا المتعلقة بالاستقرار الهرموني بحاجة إلى المعالجة.[2]
نظرياً، يمكن استخدام "animal suppliers and disposers"، ولكن عند إشراك رحم حيوان، قد تكون التقنية في نطاق الحمل بين الأنواع.[البحث الأصلي؟]
جدار الرحم
في الرحم الطبيعي، يعمل عضل جدار الرحم على طرد الجنين في نهاية الحمل، وتلعب بطانة الرحم دورًا في تكوين المشيمة. قد يشتمل الرحم الاصطناعي على مكونات ذات وظيفة مكافئة. تم التفكير في طرق لربط المشيمة الاصطناعية والمكونات "الداخلية" الأخرى مباشرة بالدورة الدموية الخارجية.[2]
الواجهة (المشيمة الاصطناعية)
قد تكون الواجهة بين المورد والجنين أو الجنين الحي اصطناعية بالكامل، على سبيل المثال باستخدام واحد أو أكثر من الأغشية شبه النافذة مثل المستخدم في "أكسجة الغشاء خارج الجسم" (ECMO).[9]
هناك أيضًا إمكانية لتنمية المشيمة باستخدام خلايا بطانة الرحم البشرية. عام 2002، أُعلن أن عينات الأنسجة المأخوذة من خلايا بطانة الرحم المأخوذة من متبرع بشري قد نمت بنجاح.[13][14]
ثم تمت هندسة عينة الأنسجة لتشكيل شكل رحم طبيعي، ثم زُرعت الأجنة البشرية في الأنسجة. زُرعت الأجنة بشكل صحيح في بطانة الرحم الاصطناعية وبدأت في النمو. ومع ذلك، توقفت التجارب بعد ستة أيام للبقاء ضمن الحدود القانونية المسموح بها لتشريع الإخصاب في المختبر (أطفال الأنابيب) في الولايات المتحدة.[2]
يمكن نظريًا زرع مشيمة بشرية داخل رحم اصطناعي، لكن مرور المغذيات عبر هذا الرحم الاصطناعي يظل مشكلة لم يتم حلها.[2]
الخزان الأمنيوسي (الكيس الأمنيوسي الاصطناعي)
تتمثل الوظيفة الرئيسية "للخزان الأمنيوسي" في القيام بوظيفة الكيس الأمنيوسي في الحماية الجسدية للجنين أو الجنين الحي، مما يسمح له بالتحرك بحرية على النحو الأمثل. يجب أن تكون أيضًا قادرة على الحفاظ على درجة حرارة مثالية. يمكن استخدام محلول رينگر اللاكتاتي كبديل عن السائل الأمنيوسي.[9]
الحبل السري
نظرياً، في حالة الإزالة المبكرة للجنين من الرحم الطبيعي، يمكن استخدام الحبل السري الطبيعي، وإبقائه مفتوحًا إما عن طريق التثبيط الطبي للانسداد الفسيولوجي، عن طريق منع التخثر وكذلك عن طريق دعامة أو إنشاء مجاز للحفاظ على تدفق الدم بين الأم والجنين.[2]
الأبحاث والتطوير
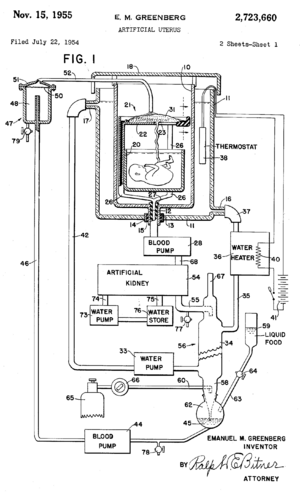
إمانوِل م. گرينبرگ
كتب إمانوِل م. گرينبرگ أوراقًا بحثية مختلفة حول موضوع الرحم الاصطناعي واستخدامه المحتمل في المستقبل.[بحاجة لمصدر]
في 22 يوليو 1954، قدم گرينبرگ براءة اختراع لتصميم رحم اصطناعي.[15] تضمنت براءة الاختراع صورتين لتصميم رحم اصطناعي. تضمن التصميم نفسه خزانًا لوضع الجنين مليئًا بالسائل الأمنيوسي، وآلة متصلة بالحبل السري، ومضخات الدم، وكلية اصطناعية، وسخان ماء. حصل على براءة الاختراع في 15 نوفمبر 1955.[15]
في 11 مايو 1960، كتب گرينبرگ إلى محرري المجلة الأمريكية لأمراض النساء والتوليد. زعم گرينبرگ أن المجلة نشرت مقال بعنوان "محاولات لعمل رحم اصطناعي"، والذي فشل في تضمين أي استشهادات حول موضوع الرحم الاصطناعي.[بحاجة لمصدر] وفقًا لگرينبرگ، فإن هذا يشير إلى أن فكرة الرحم الاصطناعي كانت فكرة جديدة على الرغم من أنه هو نفسه قد نشر عدة أوراق بحثية حول هذا الموضوع.[بحاجة لمصدر]
جامعة جونتندو في طوكيو
عام 1996، طورت جامعة جونتيندو في طوكيو حضانة الجنين خارج الرحم (EUFI).[16] قاد المشروع يوشينوري كوابارا، الذي كان مهتمًا بتنمية حديثي الولادة غير الناضجين. تم تطوير النظام باستخدام أربعة عشر جنينًا من الماعز تم وضعها بعد ذلك في السائل الأمنيوسي الاصطناعي تحت نفس ظروف الماعز الأم.[16][17] نجح كوابارا وفريقه في إبقاء أجنة الماعز في النظام لثلاثة أسابيع.[16][17] ومع ذلك، واجه النظام العديد من المشكلات ولم يكن جاهزًا للاختبار البشري.[16] ظل كوابارا يأمل في تحسين النظام واستخدامه لاحقًا على الأجنة البشرية.[16][17]
مستشفى الأطفال في فيلادلفيا
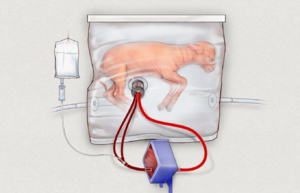
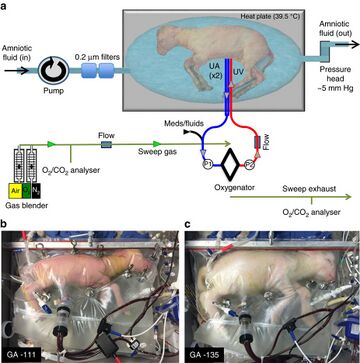
في أبريل 2017، ابتكر العلماء رحمًا اصطناعيًا آملين أن يستخدموا هذا الجهاز يومًا ما لإنقاذ الأطفال المبتسرين. تم اختبار الجهاز فقط على أجنة الخراف. وجدت دراسة شملت ثمانية حيوانات أن الجهاز يبدو فعالًا في تمكين الأجنة المبتسرة للغاية من النمو بشكل طبيعي لمدة شهر تقريبًا.[18]
يقول آلان فليك، جراح الأجنة في مستشفى الأطفال في فيلادلفيا الذي قاد الدراسة المنشورة في مجلة ناتشر كومينيكشن: "لقد حققنا نجاحاً كبيراً في استبدال الظروف الموجودة في الرحم في نموذج الحمل لدينا". وأضاف فليك: "حققت الأجنة نمواً طبيعياً. تطورت رئتيهم بشكل طبيعي، وكذلك حدث تطور طبيعي للمخ. لقد تطوروا بشكل طبيعي بكل الطرق التي يمكننا قياسها". ويقول فليك إن المجموعة تأمل في اختبار الجهاز على الأطفال المبتسرين للغاية في غضون ثلاث إلى خمس سنوات، مضيفاً: "ما حاولنا القيام به هو تطوير نظام يحاكي بيئة الرحم بأكبر قدر ممكن". "إنه رحم اصطناعي في الأساس."
أُجريت التجربة على جنين خروف عمره 107 يوماً، وهو ما يعادل جنينًا بشريًا عمره 23-25 أسبوعًا، أي حمل استمر لنحو 60% من الفترة الطبيعية للحمل، يقع داخل الرحم الاصطناعي. يوضع الجهاز في غرفة مظلمة ودافئة حيث يمكن للباحثين تشغيل أصوات قلب الأم لجنين الحمل ومراقبة الجنين بالموجات فوق الصوتية. أظهرت الأبحاث السابقة أن أجنة الخراف هي نماذج جيدة لنمو الجنين البشري.
يتكون جهاز الرحم الاصطناعي من كيس بلاستيكي شفاف مملوء بسائل أمنيوسي اصطناعي. يتم توصيل جهاز خارج الكيس بالحبل السري ليعمل مثل المشيمة، حيث يوفر التغذية والأكسجين للدم ويزيل ثاني أكسيد الكربون. يقول فليك: "الفكرة كلها هي دعم التطور الطبيعي؛ لإعادة خلق كل ما تفعله الأم بكل طريقة ممكنة لدعم نمو الجنين الطبيعي ونضجه".
وأشاد باحثون آخرون بهذا التقدم، قائلين إنه يمكن أن يساعد آلاف الأطفال المولودين قبل الأوان كل عام، إذا أثبتت الاختبارات نجاحها على البشر. وصف جاي گرينسپان، طبيب الأطفال بجامعة توماس جيفرسون، الجهاز بأنه "معجزة تكنولوجية" تمثل "خطوة كبيرة لمحاولة القيام بشيء كنا نحاول القيام به لسنوات عديدة". ويقول توماس شافر، أستاذ علم وظائف الأعضاء وطب الأطفال في جامعة تمپل، إن الجهاز يمكن أن يساعد العلماء أيضًا في معرفة المزيد عن التطور الطبيعي للجنين. ويضيف شافر: "أعتقد أن هذا إنجاز كبير".
يقول فليك: "إذا كان بإمكانك استخدام هذا الجهاز فقط كجسر للجنين، فيمكن أن يكون لديك تأثير كبير على نتائج الأطفال الخدج للغاية". "ستكون هذه صفقة ضخمة".
جامعة أيندهوڤن للتكنولوجيا (هولندا)
منذ عام 2016، يهدف باحثو جامعة أيندهوڤن للتكنولوجيا وشركاؤهم إلى تطوير رحم اصطناعي، وهو بديل مناسب للبيئة الوقائية لرحم الأم في حالة الولادة المبكرة، مما يمنع المضاعفات الصحية. سيوفر الرحم والمشيمة الاصطناعية بيئة طبيعية للطفل بهدف تسهيل الانتقال به إلى مرحلة حديثي الولادة. سيتم تطوير نظام دعم الحياة في الفترة المحيطة بالولادة (PLS) باستخدام تقنية متطورة: أثناء الاختبار والتدريب سيتم استخدام مانيكان، وستتوافر المراقبة المتقدمة والنمذجة الحاسوبية التوجيه السريري.[19]
سيقم كونسورتيوم من 3 جامعات أوروپية تعمل في المشروع من جامعات آخن وميلان وأيندهوڤن. عام 2019، حصل هذا الكونسورتيوم على دعم قدره 3 ملايين يورو، وهناك منحة ثانية بقيمة 10 ملايين قيد التنفيذ. يوفر شركاء PLS معًا خبرة طبية وهندسية ورياضية مشتركة لتطوير والتحقق من صحة نظام دعم الحياة في الفترة المحيطة بالولادة باستخدام تقنيات محاكاة متطورة. سيدفع الاتحاد متعدد التخصصات تطوير هذه التقنيات إلى الأمام ودمجها لإنشاء أول نظام نضج جنيني خارج الجسم للاستخدام السريري. يجمع هذا المشروع، الذي تنسقه جامعة أيندهوڤن للتكنولوجيا، خبراء عالميين رائدين في طب التوليد وطب حديثي الولادة والتصميم الصناعي والنمذجة الرياضية ودعم الأعضاء خارج الجسم ومراقبة الجنين غير الغازية. يقود هذا الكونسورتيوم البروفيسور فرانز فان دي فوسه والبروفيسور والطبيب گيد أوي. عام 2020، تأسست مجموعة Juno Perinatal Healthcare من قبل المهندستين جسمين كوك وليلا كوك، مما يضمن تثمين البحث الذي تم إجراؤه. يمكن العثور على مزيد من المعلومات حول التوزيع هنا؛[20]
يمكن الاطلاع على مزيد من المعلومات حول مشروع الجامعات التقنية والباحثين فيها هنا:[21]
في برشلونة، إسبانيا
- باحثون إسبان يحاولون إيهام الطبيعة باستخدام الرحم الصناعي.
في 29 يونيو 2023، يحاول الباحثون في برشلونة "خداع الطبيعة" من خلال إنشاء رحم اصطناعي للأطفال الخدج حديثي الولادة، بعد إجراء اختبارات على الحيوانات أبقت الأجنة على قيد الحياة لمدة 12 يوماً. نموذج رحمهم الصناعي يعيد إنشاء بيئة واقية باستخدام حاوية شفافة مصنوعة من مادة متوافقة مع الجسم، داخلها يمكن لرئتي الجنين وأمعائه ودماغه أن يستمروا في التطور.[23]
يتصل الرحم الصناعي بنظام دورة السائل السلوي الذي يحافظ على عزل الجنين عن المحفزات الخارجية ولكنه قابل للوصول من أجل التحكم والمراقبة عن طريق الموجات الفوق صوتية. يُعتبر الأطفال الذين يولدون بعد ستة أشهر من الحمل أو أقل من ذلك خدجاً حديثي الولادة ويواجهون مخاطر عالية للوفاة أو الإعاقة. تشير أحدث أرقام منظمة الصحة العالمية إلى وفاة حوالي 900 ألف طفل من هذا النوع في جميع أنحاء العالم في عام 2019.
وبتصريح من رئيس المشروع إدوارد غراتاكوس: "نحاول تطوير نظام يسمح لنا بالاحتفاظ بالجنين خارج جسم والدته ولكن في ظروف جنينية: أنه يستمر في التنفس عبر الحبل السري... أنه يمكننا إطعامه عبر الحبل السري، وأنه يعيش محاطاً بسائل في درجة حرارة ثابتة". كما أنه يقود فريقاً مكوناً من 35 عضو من مركز البحوث الطبية BCNatal - وهو اندماج بين قسمي طب الأم والجنين وقسم النساء والتوليد في مستشفيين في برشلونة - ومؤسسة لا كايكسا، وهي منظمة خاصة تمولها كايشابانك.[24]
قام الفريق بإجراء دراسات سريرية مسبقة على الحملة، حيث تمكنوا من الحفاظ على أجنة لمدة 12 يوماً، ويخططون أيضاً لإجراء اختبارات على الخنازير قبل اقتراح تجربة سريرية على البشر في غضون بضع سنوات. قال غراتاكوس: "هذا المشروع المعقد للغاية يشمل تخصصات طبية مختلفة ويتطلب مهندسين من أنواع مختلفة. إنه تحدي، إنه أمر شديد الحساسية لتحقيق هذا، لخداع الطبيعة وجعل هذا ممكناً".
ومن بين عدد قليل من المشاريع الشبيهة حول العالم، نجحت مجموعة من العلماء في مستشفى الأطفال في فيلادلفيا في الحفاظ على أجنة الحيوانات على قيد الحياة لمدة 28 يوماً.
اعتبارات فلسفية
الأخلاقيات الحيوية
يثير تطور الرحم الاصطناعي والتخليق الخارجي أخلاقيات علم الأحياء والاعتبارات القانونية، وله أيضًا آثار هامة على الحقوق الإنجابية وجدل الإجهاض.
قد يوسع الرحم الاصطناعي نطاق بقاء الجنين، مما يثير تساؤلات حول الدور الذي تلعبه قابلية بقاء الجنين في قانون الإجهاض. ضمن نظرية الانفصال، على سبيل المثال، تشمل حقوق الإجهاض فقط الحق في التخلص من الجنين، ولا تمتد دائمًا إلى إنهاء حياته. إذا كان نقل الجنين من رحم المرأة إلى رحم اصطناعي ممكنًا، فإن اختيار إنهاء الحمل بهذه الطريقة يمكن أن يوفر بديلاً لإجهاض الجنين.[25][26]
هناك أيضًا مخاوف نظرية من أن الأطفال الذين ينمون داخل الرحم الاصطناعي قد يفتقرون إلى "بعض الروابط الأساسية مع أمهاتهم التي يتمتع بها الأطفال الآخرين".[27]

في أبريل 2017، ابتكر العلماء رحمًا اصطناعيًا آملين أن يستخدموا هذا الجهاز يومًا ما لإنقاذ الأطفال المبتسرين. تم اختبار الجهاز فقط على أجنة الخراف. وجدت دراسة شملت ثمانية حيوانات أن الجهاز يبدو فعالًا في تمكين الأجنة المبتسرة للغاية من النمو بشكل طبيعي لمدة شهر تقريبًا.[28]
يقول آلان فليك، جراح الأجنة في مستشفى الأطفال في فيلادلفيا الذي قاد الدراسة المنشورة في مجلة ناتشر كومينيكشن: "لقد حققنا نجاحاً كبيراً في استبدال الظروف الموجودة في الرحم في نموذج الحمل لدينا". وأضاف فليك: "حققت الأجنة نمواً طبيعياً. تطورت رئتيهم بشكل طبيعي، وكذلك حدث تطور طبيعي للمخ. لقد تطوروا بشكل طبيعي بكل الطرق التي يمكننا قياسها". ويقول فليك إن المجموعة تأمل في اختبار الجهاز على الأطفال المبتسرين للغاية في غضون ثلاث إلى خمس سنوات، مضيفاً: "ما حاولنا القيام به هو تطوير نظام يحاكي بيئة الرحم بأكبر قدر ممكن". "إنه رحم اصطناعي في الأساس."
أُجريت التجربة على جنين خروف عمره 107 يوماً، وهو ما يعادل جنينًا بشريًا عمره 23-25 أسبوعًا، أي حمل استمر لنحو 60% من الفترة الطبيعية للحمل، يقع داخل الرحم الاصطناعي. يوضع الجهاز في غرفة مظلمة ودافئة حيث يمكن للباحثين تشغيل أصوات قلب الأم لجنين الحمل ومراقبة الجنين بالموجات فوق الصوتية. أظهرت الأبحاث السابقة أن أجنة الخراف هي نماذج جيدة لنمو الجنين البشري.
يتكون جهاز الرحم الاصطناعي من كيس بلاستيكي شفاف مملوء بسائل أمنيوسي اصطناعي. يتم توصيل جهاز خارج الكيس بالحبل السري ليعمل مثل المشيمة، حيث يوفر التغذية والأكسجين للدم ويزيل ثاني أكسيد الكربون. يقول فليك: "الفكرة كلها هي دعم التطور الطبيعي؛ لإعادة خلق كل ما تفعله الأم بكل طريقة ممكنة لدعم نمو الجنين الطبيعي ونضجه".
وأشاد باحثون آخرون بهذا التقدم، قائلين إنه يمكن أن يساعد آلاف الأطفال المولودين قبل الأوان كل عام، إذا أثبتت الاختبارات نجاحها على البشر. وصف جاي گرينسپان، طبيب الأطفال بجامعة توماس جيفرسون، الجهاز بأنه "معجزة تكنولوجية" تمثل "خطوة كبيرة لمحاولة القيام بشيء كنا نحاول القيام به لسنوات عديدة". ويقول توماس شافر، أستاذ علم وظائف الأعضاء وطب الأطفال في جامعة تمپل، إن الجهاز يمكن أن يساعد العلماء أيضًا في معرفة المزيد عن التطور الطبيعي للجنين. ويضيف شافر: "أعتقد أن هذا إنجاز كبير".
يقول فليك: "إذا كان بإمكانك استخدام هذا الجهاز فقط كجسر للجنين، فيمكن أن يكون لديك تأثير كبير على نتائج الأطفال الخدج للغاية". "ستكون هذه صفقة ضخمة".
المساواة بين الجنسين والمثليين
في كتاب جدلية الجنس المنشور عام 1970، كتبت الأنثوية سالوميث فيرستون أن الاختلافات في الأدوار التناسلية الحيوية هي مصدر عدم المساواة بين الجنسين. وخصت فيرستون بالذكر الحمل والولادة، مشيرة إلى أن الرحم الاصطناعي سيحرر "النساء من استبداد بيولوجيتهن الإنجابية".[29][30]
تجادل أراتي پراساد في عمودها في "الگارديان" حيق قالت في مقالها "كيف ستغير الأرحام الاصطناعية أفكارنا عن الجنس والأسرة والمساواة" أن "ستعطي الرجال [...] أداة أساسية لإنجاب طفل بدون امرأة تمامًا، إذا اختاروا ذلك. سيطلب منا التساؤل عن مفاهيم الجنس والأبوة". علاوة على ذلك، تدافع عن الفوائد التي تعود على الأزواج من نفس الجنس: "قد يعني ذلك أيضًا أنه يمكن الاستغناء عن الانقسام بين الأم والأب: فالرحم خارج جسد المرأة يخدم النساء والنساء المتحولات والأزواج من نفس الجنس على قدم المساواة دون تحيز".[31]
انظر أيضاً
- السائل السلوي
- الفصادة
- عالم جديد شجاع
- التكون الخارجي
- استعمار الأجنة الفضائية
- أكسجة غشائية خارج الجسم
- ديال دموي
- طفل الأنابيب
- الحمل الذكري
- ما بعد الجندرية
- هندسة الأنسجة
مرئيات
| جنين خروف مبتسر يكمل نموه داخل رحم اصطناعي. |
| يحاول الباحثون في برشلونة "خداع الطبيعة" من خلال إنشاء رحم اصطناعي للأطفال الخدج حديثي الولادة، بعد إجراء اختبارات على الحيوانات أبقت الأجنة على قيد الحياة لمدة 12 يوماً، 29 يونيو 2023. |
المصادر
- ^ أ ب Partridge, Emily A.; Davey, Marcus G.; Hornick, Matthew A.; McGovern, Patrick E.; Mejaddam, Ali Y.; Vrecenak, Jesse D.; Mesas-Burgos, Carmen; Olive, Aliza; Caskey, Robert C.; Weiland, Theodore R.; Han, Jiancheng; Schupper, Alexander J.; Connelly, James T.; Dysart, Kevin C.; Rychik, Jack; Hedrick, Holly L.; Peranteau, William H.; Flake, Alan W. (25 April 2017). "An extra-uterine system to physiologically support the extreme premature lamb". Nature Communications. 8: 15112. Bibcode:2017NatCo...815112P. doi:10.1038/ncomms15112. PMC 5414058. PMID 28440792.
 Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع Bulletti, C.; Palagiano, A.; Pace, C.; Cerni, A.; Borini, A.; De Ziegler, D. (2011). "The artificial womb". Annals of the New York Academy of Sciences. 1221 (1): 124–128. Bibcode:2011NYASA1221..124B. doi:10.1111/j.1749-6632.2011.05999.x. PMID 21401640. S2CID 30872357.
- ^ Shahbazi, M. N., Jedrusik, A., Vuoristo, S., Recher, G., Hupalowska, A., Bolton, V., … Zernicka-Goetz, M. (2016). Self-organization of the human embryo in the absence of maternal tissues. Nature Cell Biology, 18, 700. Retrieved from http://dx.doi.org/10.1038/ncb3347
- ^ Deglincerti, A., Croft, G. F., Pietila, L. N., Zernicka-Goetz, M., Siggia, E. D., & Brivanlou, A. H. (2016). Self-organization of the in vitro attached human embryo. Nature, 533, 251. Retrieved from http://dx.doi.org/10.1038/nature17948
- ^ Morber, Jenny (26 Apr 2017). "Should We Study Human Embryos Beyond 14 Days?". PBS Socal. Retrieved 23 Aug 2018.
- ^ Philadelphia, The Children's Hospital of (28 February 2017). "A Unique Womb-Like Device Could Reduce Mortality and Disability for Extremely Premature Babies". www.chop.edu.
- ^ "Scientists Create Artificial Womb That Could Help Prematurely Born Babies". NPR.org.
- ^ "Top Transhuman Web Sites". Archived from the original on 27 November 2006.
- ^ أ ب ت Sakata M; Hisano K; Okada M; Yasufuku M (May 1998). "A new artificial placenta with a centrifugal pump: long-term total extrauterine support of goat fetuses". J. Thorac. Cardiovasc. Surg. 115 (5): 1023–31. doi:10.1016/s0022-5223(98)70401-5. PMID 9605071.
- ^ Bautista-Hernandez, V.; Thiagarajan, R. R.; Fynn-Thompson, F.; Rajagopal, S. K.; Nento, D. E.; Yarlagadda, V.; Teele, S. A.; Allan, C. K.; Emani, S. M.; Laussen, P. C.; Pigula, F. A.; Bacha, E. A. (2009). "Preoperative Extracorporeal Membrane Oxygenation as a Bridge to Cardiac Surgery in Children with Congenital Heart Disease". The Annals of Thoracic Surgery. 88 (4): 1306–1311. doi:10.1016/j.athoracsur.2009.06.074. PMC 4249921. PMID 19766826.
- ^ Alan H. Jobe (August 2004). "Post-conceptional age and IVH in ECMO patients". The Journal of Pediatrics. 145 (2): A2. doi:10.1016/j.jpeds.2004.07.010.
- ^ Spencer AU; et al. (September 2005). "Pediatric short bowel syndrome: redefining predictors of success". Ann. Surg. 242 (3): 403–9, discussion 409–12. doi:10.1097/01.sla.0000179647.24046.03. PMC 1357748. PMID 16135926. (mean follow-up time was 5.1 years)
- ^ "Ronald O. Perelman and Claudia Cohen Center for Reproductive Medicine | Weill Cornell Medicine". ivf.org.
- ^ "Weill Cornell Research".
- ^ أ ب (in en)Artificial uterus, 1955-11-15, http://www.freepatentsonline.com/2723660.html, retrieved on 2018-05-07
- ^ أ ب ت ث ج Klass, Perri (1996-09-29). "The Artificial Womb Is Born". The New York Times (in الإنجليزية الأمريكية). ISSN 0362-4331. Retrieved 2018-05-07.
- ^ أ ب ت Kuwabara, Yoshinori; Okai, Takashi; Imanishi, Yukio; Muronosono, Etsuo; Kozuma, Shiro; Takeda, Satoru; Baba, Kazunori; Mizuno, Masahiko (June 1987). "Development of Extrauterine Fetal Incubation System Using Extracorporeal Membrane Oxygenator". Artificial Organs (in الإنجليزية). 11 (3): 224–227. doi:10.1111/j.1525-1594.1987.tb02663.x. ISSN 0160-564X. PMID 3619696.
- ^ "Scientists Create Artificial Womb That Could Help Prematurely Born Babies". www.npr.org. 2022-04-25. Retrieved 2022-07-19.
- ^ "Home - Perinatal Life Support".
- ^ "Home | Juno Perinatal Healthcare".
- ^ "Artificial womb".
- ^ La Caixa Foundation/Handout via REUTERS/File Photo
- ^ Horaci Garcia (2023-06-29). "Spanish researchers aim to 'trick nature' with artificial womb". www.reuters.com.
- ^ Navya Beri (2023-06-29). "Spanish researchers aim to trick nature by creating artificial womb for premature babies". www.wionews.com.
- ^ Randall, Vernellia; Randall, Tshaka C. (22 March 2008). "Built in Obsolescence: The Coming End to the Abortion Debate". doi:10.2139/ssrn.1112367. S2CID 57105464.
{{cite journal}}: Cite journal requires|journal=(help) - ^ Chessen, Matt. "Artificial Wombs Could Outlaw Abortion". Mattlesnake.com. Archived from the original on 12 October 2019. Retrieved 2 November 2014.
- ^ Smajdor, Anna (Summer 2007). "The Moral Imperative for Ectogenesis" (PDF). Cambridge Quarterly of Healthcare Ethics. 16 (3): 336–45. doi:10.1017/s0963180107070405. PMID 17695628. S2CID 36754378. Archived from the original (PDF) on 11 سبتمبر 2013.
- ^ "Scientists Create Artificial Womb That Could Help Prematurely Born Babies". www.npr.org. 2022-04-25. Retrieved 2022-07-19.
- ^ Chemaly, Soraya (23 February 2012). "What Do Artificial Wombs Mean for Women?". RH Reality Check.
- ^ Rosen, Christine (2003). "Why Not Artificial Wombs?" (PDF). The New Atlantis. Archived from the original (PDF) on 1 August 2014.
- ^ "How artificial wombs will change our ideas of gender, family and equality". The Guardian (in الإنجليزية البريطانية). 2017-05-01. ISSN 0261-3077. Retrieved 2017-06-16.
المراجع
- Coleman, Stephen (2004). The Ethics Of Artificial Uteruses: Implications For Reproduction And Abortion. Burlington, VT: Ashgate Pub. ISBN 978-0-7546-5051-5.
- Scott Gelfand, ed. (2006). Ectogenesis: Artificial Womb Technology and the Future of Human Reproduction. Amsterdam [u.a.]: Rodopi. ISBN 978-90-420-2081-8.
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- CS1 الإنجليزية البريطانية-language sources (en-gb)
- Short description is different from Wikidata
- Articles using infobox templates with no data rows
- All articles that may contain original research
- Articles that may contain original research from May 2020
- مقالات ذات عبارات بحاجة لمصادر
- تكنولوجيا افتراضية
- طب النساء والتوليد
- تكنولوجيات بازغة
- رحم
- أعضاء اصطناعية
