حمض الپروپيونيك
|
| |||
|
| |||
| الأسماء | |||
|---|---|---|---|
| اسم أيوپاك
حمض الپروپيونيك
| |||
| أسماء أخرى
حمض الإثانوكاربوكسايليك، حمض الپروپيونيك
| |||
| المُعرِّفات | |||
| رقم CAS | |||
3D model (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.001.070 | ||
| E number | E280 (preservatives) | ||
PubChem CID
|
|||
| رقم RTECS |
| ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| الخصائص | |||
| الصيغة الجزيئية | C3H6O2 | ||
| كتلة مولية | 74.07 g mol-1 | ||
| المظهر | سائل عديم اللون | ||
| الكثافة | 0.99 گرام/سم³ | ||
| نقطة الانصهار | |||
| نقطة الغليان | |||
| قابلية الذوبان في الماء | miscible | ||
| الحموضة (pKa) | 4.87 | ||
| اللزوجة | 10 mPa·s | ||
| البنية | |||
| Dipole moment | 0.63 D | ||
| المخاطر | |||
| خطر رئيسي | Corrosive | ||
| توصيف المخاطر | R34 | ||
| تحذيرات وقائية | (S1/2) S23 S36 S45 | ||
| NFPA 704 (معيـَّن النار) | |||
| نقطة الوميض | 327 K, 54 °C | ||
| مركبات ذا علاقة | |||
أنيونات أخرى
|
پروپيونات | ||
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |||
| مراجع الجدول | |||
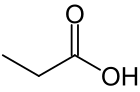
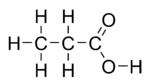
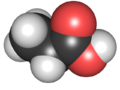
حمض الپروپانيك Propanoic acid (أو حمض الپروپيونيك propionic acid)، هو حمض كربوكسيلي طبيعي صيغته الكيميائية 3CH2COOH. It is a clear liquid ذو رائحة نفاذة. تعرف أنيونات CH3CH2COO− وأملاح وإسترات حمض الپروپانيك بالپروپيونات.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التاريخ
الخصائص الكيميائية
التصنيع
في الصناعة، ينتج حمض الپروپيونيك بصفة رئيسية عن طريق إضافة الكربونيل الهيدروجينية إلى الإثلين باستخدام كربونيل النيكل كحافز:[1]
- H2C=CH2 + H2O + CO → CH3CH2CO2H
وينتج أيضاً عن طريق الأكسدة الهوائي لأيونات المنجنيز، وينجح هذا التفاعل عادة في درجات الحرارة من 40-50 °س:
ينتج حمض الپروپيونيك طبيعياً as its coenzyme A ester, propionyl-CoA, from the metabolic breakdown of fatty acids containing odd numbers of carbon atoms, and also from the breakdown of some amino acids. Bacteria of the genus Propionibacterium produce propanoic acid as the end product of their anaerobic metabolism. This class of bacteria is commonly found in the stomachs of ruminants and the الغدد الغرقية في الإنسان، وهي المسئولة عن انتاج رائحة الجبنة السويسرية والعرق.
الاستخدامات
يمنع حمض الپروپيونيك نمو العفن وبعض أنواع الجراثيم عند المستويات ما بين 0.1 و1% حسب الوزن. As a result, most propanoic acid produced is consumed as a preservative for both animal feed and food for human consumption. For animal feed, it is used either directly or as its ammonium salt. The antibiotic Monensin is added to cattle feed to favor propionibacteria over acetic acid producers in the rumen; this produces less carbon dioxide and feed conversion is better. This application accounts for about half of the world production of propanoic acid. Another major application is as a preservative in baked goods, which use the sodium and calcium salts.[1] As a food additive it is approved for use in the EU,[2] USA[3] and Australia and New Zealand.[4] It is listed by its INS number (280) or E number E280.
Propanoic acid is also useful as an intermediate in the production of other chemicals, especially polymers. Cellulose-acetate-propionate is a useful thermoplastic. Vinyl propionate is also used. In more specialized applications, it is also used to make pesticides and pharmaceuticals. The esters of propanoic acid have fruit-like odors and are sometimes used as solvents or artificial flavorings.[1]
الأيض
The metabolism of propanoic acid begins with its conversion to propionyl coenzyme A (propionyl-CoA), the usual first step in the metabolism of carboxylic acids. Since propanoic acid has three carbons, propionyl-CoA cannot directly enter either beta oxidation or the citric acid cycles. In most vertebrates, propionyl-CoA is carboxylated to D-methylmalonyl-CoA, which is isomerised to L-methylmalonyl-CoA. A vitamin B12-dependent enzyme catalyzes rearrangement of L-methylmalonyl-CoA to succinyl-CoA, which is an intermediate of the citric acid cycle and can be readily incorporated there.
In propanoic acidemia, a rare inherited genetic disorder, propionate acts as a metabolic toxin in liver cells by accumulating in mitochondria as propionyl-CoA and its derivative, methylcitrate, two tricarboxylic acid cycle inhibitors. Propanoate is metabolized oxidatively by glia, which suggests astrocytic vulnerability in propanoic acidemia when intramitochondrial propionyl-CoA may accumulate. Propanoic acidemia may alter both neuronal and glial gene expression by affecting histone acetylation.[5][6] When propanoic acid is infused directly into rodents brains it produces reversible behavior (e.g., hyperactivity, dystonia, social impairment, perseveration) and brain (e.g., innate neuroinflammation, glutathione depletion) changes that may be used as a means to model autism in rats.[5]
تكونه في الإنسان
يحمل جلد الإنسان أنواع عديدة من الجراثيم المعروفة باسم پروپيونيبكتريا، والتي سميت بهذا الاسم لقدرتها على انتاج حمض الپروپيونيك. وأشهرها Propionibacterium acnes، التي تعيش بصفة رئيسية في الغدة الزهمية وهو أحد الأسباب الرئيسية لظهور حب الشباب.
في فبراير 2013، أعلن عن اكتشاف بكتريا بالبطن تشم حمض الپروپيونيك فيها الكلى فتخفض ضغط الدم عبر إنزيم الرِنين.[7]
المصادر
- ^ أ ب ت W. Bertleff; M. Roeper; X. Sava. "Carbonylation". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a05_217.
{{cite encyclopedia}}: Cite has empty unknown parameter:|authors=(help)CS1 maint: multiple names: authors list (link) - ^ "Current EU approved additives and their E Numbers". UK Food Standards Agency. Retrieved 2011-10-27.
- ^ "Listing of Food Additives Status Part II". US Food and Drug Administration. Retrieved 2011-10-27.
- ^ "Standard 1.2.4 - Labelling of ingredients". Australia New Zealand Food Standards Code. Comlaw.au. Retrieved 2011-10-27.
- ^ أ ب D. F. MacFabe; D. P. Cain; K. Rodriguez-Capote; A. E. Franklin; J. E. Hoffman; F. Boon; A. R. Taylor; M. Kavaliers; K.-P. Ossenkopp (2007). "Neurobiological effects of intraventricular propionic acid in rats: Possible role of short-chain fatty acids on the pathogenesis and characteristics of autism spectrum disorders". Behavioral Brain Research. 176 (1): 149–169. doi:10.1016/j.bbr.2006.07.025.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ N. H. T. Nguyen; C. Morland; S. Villa Gonzalez; F. Rise; J. Storm-Mathisen; V. Gundersen; B. Hassel (2007). "Propionate increases neuronal histone acetylation, but is metabolized oxidatively by glia. Relevance for propionic acidemia". Journal of Neurochemistry. 101 (3): 806–814. doi:10.1111/j.1471-4159.2006.04397.x. PMID 17286595.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ "Sniffing out hypertension". إكونومست. 2013-02-16. Retrieved 2012-02-26.
{{cite web}}: Text "a" ignored (help)
وصلات خارجية
- NIST Standard Reference Database
- International Chemical Safety Card 0806
- NIOSH Pocket Guide to Chemical Hazards
- Technical data of propionic acid of BASF
- Neurobiological effects of intraventricular propionic acid in ratsPossible role of short chain fatty acids on the pathogenesis and characteristics of autism spectrum disorders
- The Propionic Acids. Gastrointestinal Toxicity in Various Species
- Propionic Acid Technical Data Sheet{{
- CS1 errors: unrecognized parameter
- ECHA InfoCard ID from Wikidata
- E number from Wikidata
- Chemical articles with unknown parameter in Chembox
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Short description is different from Wikidata
- Articles that show a Medicine navs template
- پروپيونات
- أحماض الپروپيونيك