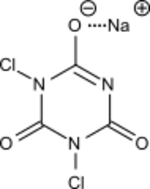
ثنائي كلورو إيزوسيانورات الصوديوم
| |
| الأسماء | |
|---|---|
| اسم أيوپاك
Sodium 3,5-dichloro-2,4,6-trioxo-1,3,5-triazinan-1-ide
| |
| أسماء أخرى
Sodium dichloroisocyanurate, Sodium troclosene, Sodic troclosene
| |
| المُعرِّفات | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.018.880 |
PubChem CID
|
|
| رقم RTECS |
|
| UNII |
|
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | C3Cl2N3NaO3 |
| كتلة مولية | 219.95 g/mol (anhydrous) 255.98 g/mol (dihydrate) |
| المظهر | white, crystalline powder |
| الرائحة | chlorine-like |
| الكثافة | 0.7 g/cm3 (as granules) |
| نقطة الانصهار | |
| قابلية الذوبان في الماء | 22.7 g/100 mL (25 °C) |
| قابلية الذوبان في acetone | 0.5 g/100 mL (30 °C) |
| الحموضة (pKa) | 6.2-6.8 |
| المخاطر | |
| الجرعة أو التركيز القاتل (LD, LC): | |
LD50 (الجرعة الوسطى)
|
(Rat oral) 1670 mg/kg |
| مركبات ذا علاقة | |
كاتيونات أخرى
|
Potassium dichloroisocyanurate Calcium dichloroisocyanurate Lithium dichloroisocyanurate Barium dichloroisocyanurate |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
ثنائي كلورو إيزوسيانورات صوديوم ( Sodium dichloroisocyanurate ؛ INN: sodium troclosene, troclosenum natricum or NaDCC أو SDIC) هو مركب كيميائي يُستخدم على نطاق واسع كعامل تنظيف ومعقم.[1] وهو مادة صلبة عديمة اللون قابلة للذوبان في الماء، وينتج من تفاعل حمض السيانوريك مع الكلور. ثنائي الهيدرات هو أيضاً معروف (51580-86-0 ) كما هو الحال لملح الپوتاسيوم (2244-21-5 ).
له الصيغة المجملة C3Cl2N3NaO3 ، وهو ملح الصوديوم لحمض ثنائي كلورو إيزوسيانوريك. وهو مركب حلقي غير متجانس من مشتقات التيرازين.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الاستخدامات
It is mainly used as a disinfectant, biocide and industrial deodorant. It is found in some modern water purification tablets/filters. It is more efficient than the formerly used halazone water disinfectant. In these applications, it is a slow-release source of chlorine in low concentrations at a relatively constant rate. As a disinfectant, it is used to sterilize drinking water, swimming pools, tableware and air, and to fight against infectious diseases as a routine disinfection agent.
It can be used for disinfection and environmental sterilization, for example in livestock, poultry, fish and silkworm raising, for bleaching textiles, for cleaning industrial circulating water, and to prevent wool from shrinking.
The reaction between NaDCC and a dilute solution of copper (II) sulfate produces an intense lilac precipitate of the complex salt sodium copper dichloroisocyanurate. The reactions between dichloroisocyanurate salts (Na, K, Li, Ba, Ca) and transition metal salts (Ni, Cu, Cd) are described in patent US 3,055,889. The overall reaction is:
- CuSO4 + 4 Na(C3N3O3Cl2) → Na2[Cu(C3N3O3Cl2)4] + Na2SO4
Sodium dichloroisocyanurate reacts with concentrated (130 vol, 35%) hydrogen peroxide to create singlet oxygen which emits red light upon decomposition . [2]
It is considered hazardous according to OSHA 29 CFR 1910.1200. High level exposure can cause reactive airways dysfunction syndrome (RADS) [3]
انظر أيضاً
- Comet (cleanser)
- Dichloroisocyanuric acid (dichlor)
- Trichloroisocyanuric acid (trichlor)
المصادر
- ^ Huthmacher, Klaus; Most, Dieter (2000). "Cyanuric Acid and Cyanuric Chloride". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a08_191. ISBN 3-527-30673-0..
- ^ [Acc. Chem. Res. 2006, 39, 11, 797–804]
- ^ "Sodium dichloroisocyanurate - Material Safety Data Sheet" (PDF). September 30, 2009.