هيدرازين

| |||
|
| |||
| الأسماء | |||
|---|---|---|---|
| اسم أيوپاكs
Hydrazine
Diazane | |||
| المُعرِّفات | |||
| رقم CAS | |||
| ECHA InfoCard | 100.005.560 | ||
| رقم EC |
| ||
| رقم RTECS |
| ||
| UN number | 2029 (anhydrous) 2030 (aq. soln., 37–64%) 3293 (aq. soln., <37%) | ||
CompTox Dashboard (EPA)
|
|||
| الخصائص | |||
| الصيغة الجزيئية | N2H4 | ||
| كتلة مولية | 32.05 g/mol (anhydrous) 50.06 g/mol (hydrate) | ||
| المظهر | سائل عديم اللون | ||
| الكثافة | 1.0045 g/cm3 (anhydrous) 1.032 g/cm3 (hydrate) | ||
| نقطة الانصهار | |||
| نقطة الغليان | |||
| قابلية الذوبان في الماء | miscible | ||
| الحموضة (pKa) | 8.1 | ||
| معامل الانكسار (nD) | 1.46044 (22 °C, anhydrous) [1] 1.4284 (hydrate) | ||
| اللزوجة | 0.876 cP (25 °C) | ||
| البنية | |||
| الشكل الجزيئي | هرمي عند N | ||
| Dipole moment | 1.85 D[2] | ||
| المخاطر | |||
تبويب الاتحاد الاوروپي (DSD)
|
Carc. Cat. 2 Toxic (T) Corrosive (C) خطر على البيئة (N) | ||
| توصيف المخاطر | R45, R10, R23/24/25, R34, R43, R50/53 | ||
| تحذيرات وقائية | S53, S45, S60, S61 | ||
| NFPA 704 (معيـَّن النار) | |||
| نقطة الوميض | 52 °C | ||
| حدود الانفجار | 1.8–100% | ||
| الجرعة أو التركيز القاتل (LD, LC): | |||
LD50 (الجرعة الوسطى)
|
59–60 mg/kg (oral in rats, mice)[3] | ||
| مركبات ذا علاقة | |||
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |||
| مراجع الجدول | |||
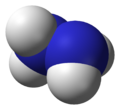
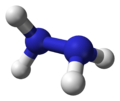
الهيدرازين Hydrazine مركب كيميائي مهم يستعمل في وقود المحركات النفاثة والصواريخ. وتستخدم الصناعة أيضا هذا المركب لإنتاج مواد كيميائية للمنسوجات والزراعة، والمتفجرات، والمواد الخاصة بتظهير الصور الفوتوغرافية، وعوامل نفخ تستخدم في تصنيع المطاط الرغوي. وتستخدم مشتقات الهيدرازين في تنظيم نمو النبات مثل الحشائش التي توجد على جانبي طرق السيارات، إذ إن هذه المواد الكيميائية تمنع نمو الحشائس بطريقة سريعة بحيث لا تحتاج لعناية دائمة.
يوجد الهيدرازين في شكل سائل عديم اللون حاد الرائحة مسبب للتآكل. وهو عبارة عن قاعدة تحتوي على النيتروجين، ويعد عاملاً مختزلاً قويًا. انظر:القاعدة. يمتزج هذا المركب بسهولة مع الماء والكحول، ويغلي عند درجة 114°م، وصيغته الكيميائية H2NNH2. ويشتعل هذا المركب بسهولة في الهواء، ويُولِّد كمية كبيرة من الحرارة مكوناً غاز النيتروجين والماء. وتقوم المصانع بتحضيره بعدة طرق من هيدرات الهيدرازين ذي الصيغة الكيميائية H2NNH2.H2O.
المصادر
|
انظر أيضاً
وصلات خارجية
- Pages using Chembox with unknown parameters
- ECHA InfoCard ID from Wikidata
- Chemical articles with unknown parameter in Chembox
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Short description is different from Wikidata
- هيدرازينات
- قواعد (كيمياء)
- مجموعات وظيفية
- ملوثات الهواء الخطرة
- مركبات النيتروجين
- وقود الصواريخ
- دافعات أحادية
- موانع التآكل
- مثبطات أكسيديز أحادي الأمين
- عوامل مختزلة
- هيدريدات النيتروجين
- IARC Group 2B carcinogens
- سلامة وصحة مهنية