دولوتگراڤير
 | |
 | |
| البيانات السريرية | |
|---|---|
| الأسماء التجارية | تيڤيكاي |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a613043 |
| License data |
|
| مسارات الدواء | شهرياً |
| رمز ATC | |
| الحالة القانونية | |
| الحالة القانونية | |
| بيانات الحركية الدوائية | |
| التوافر الحيوي | n/a[1] |
| ارتباط الپروتين | ≥98.9% |
| الأيض | UGT1A1 وCYP3A |
| Elimination half-life | ~14 ساعة |
| الإخراج | البراز (53%) والبول (18.9%) |
| المعرفات | |
| |
| رقم CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.237.735 |
| Chemical and physical data | |
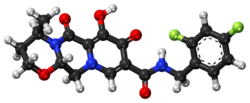
| التركيب | C20H19F2N3O5 |
| الكتلة المولية | 419.38 g/mol |
| 3D model (JSmol) | |
| |
| |
| | |
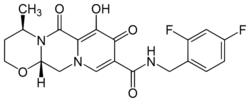
دولوتگراڤير Dolutegravir (DTG)، يباع تحت الاسم التجاري تيڤيكاي Tivicay، هو دواء يستخدم مع أدوية أخرى لعلاج متلازمة نقص المناعة المكتسبة (الإيدز).[2] قد يستخدم أيضاً، كجزء من العلاج الوقائي بعد التعرض للڤيروس، للوقاية من عدوى متلازمة نقص المناعة المكتسبة في أعقاب التعرض المحتمل للڤيروس.[3] يؤخذ هذا الدواء عن طريق الفم.[2]
الآثار الشائعة لدولوتگراڤير هي مشكلات في النوم، الشعور بالإجهاد، الإسهال، فرط سكر الدم، والصداع.[3] قد تتضمن الآثار الجانبية الخطيرة ردود فعل تحسسية ومشكلات في الكبد.[3] لا يوجد تأكيدات على استخدام الدواء بأمان أثناء الحمل أو الرضاعة.[3] دولوتگراڤير هو مثبط للإنزيم المدمج والذي يعمل على منع عمل الإنزيم المدمج المطلوب للتناسخ الڤيروسي.[3]
تمت الموافقة على الاستخدام الطبي لدوتگراڤير في الولايات المتحدة عام 2013.[3] وهو ضمن قائمة الأدوية الأساسية لمنظمة الصحة العالمية، ومن أكثر الأدوية تأثيراً وأماناً المطلوبة ضمن المنظومة الصحية.[4] عام 2015، كانت تكلفة الدواء في المملكة المتحدة 499 جنيه إسترليني شهرياً.[2] ويتوافر أيضاً مجموعة أباكاڤير/دوتگراڤير/لاميڤودين، التي تجمع بين الدوتگراڤير والأباكاڤير واللاميڤودين.[3]
الاستخدام الطبي
تمت الموافقة على استخدام دولوتگراڤير للمرضى المصابين بمتلازمة نقص المناعة البشرية. يمكن استخدامه لعلاج البالغين المصابين بالإيدز ممن لم يسبق لهم تلقي علاج للمرض وللبالغين المصابين بالمرض ممن سبق له تلقي علاج للمرض، من بينهم أولئك الذين خضعوا للعلاج بأنواع أخرى من مثبطات الإنزيم المدمج. كما تمت الموافقة على استخدام الدواء للأطفال في عمر 12 سنة وأكثر ممن لا يقل وزنهم عن 40 كيلوگرام سواء من لم يسبق لهم أو من سبق لهم تلقي أنواع أخرى من مثبطات الإنزيم المدمج.[5]
الآثار الجانبية
الآثار الجانبية الشائعة لدولوتگراڤير في التجارب السريرية تشمل الأرق والصداع. أما الآثار الجانبية الحادة فتشمل ردود الأفعال التحسسية واختلال وظائف الكبد لدى المرضى الذين يعانون من التهاب الكبد الوبائي ب أو ج.[6] تشمل عبوة الدواء تحذيرات من حدوث ارتفاع متوسط في مصل الكرياتينين بنسبة 0.11 ملگ/dL بسبب تثبيط الإفراز الأنبوبي للكرياتين ولا يؤثر الدواء على وظائف الكلى.[1]
التاريخ
التجارب السريرية
المصادر
- ^ أ ب "Tivicay® (dolutegravir) Tablets for Oral Use. Full Prescribing Information" (PDF). ViiV Healthcare, 2013. Archived from the original (PDF) on 3 January 2014. Retrieved 9 February 2014.
{{cite web}}: Unknown parameter|deadurl=ignored (|url-status=suggested) (help) - ^ أ ب ت British national formulary : BNF 69 (69 ed.). British Medical Association. 2015. p. 429. ISBN 9780857111562.
- ^ أ ب ت ث ج ح خ "Dolutegravir Sodium". The American Society of Health-System Pharmacists. Retrieved 8 December 2017.
- ^ "WHO Model List of Essential Medicines (20th List)" (PDF). World Health Organization. March 2017. Retrieved 29 June 2017.
- ^ FDA approves new drug to treat HIV infection http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm364744.htm Aug. 12, 2013
- ^ U.S. FDA approves GlaxoSmithKline's HIV drug Tivicay https://www.reuters.com/article/2013/08/12/us-glaxosmithkline-hivdrug-idUSBRE97B0WU20130812 Mon Aug 12, 2013 6:40pm EDT
- CS1 errors: unsupported parameter
- Template:drugs.com link with non-standard subpage
- Articles with changed CASNo identifier
- ECHA InfoCard ID from Wikidata
- Infobox-drug molecular-weight unexpected-character
- Chemical pages without DrugBank identifier
- Drug has EMA link
- Drugboxes which contain changes to verified fields
- الأدوية الأساسية حسب منظمة الصحة العالمية
- ذيفان الكبد
- مثبطات الإنزيم المدمج
- فلوريدات عضوية