التحفيز العضوي
في الكيمياء العضوية، يشير مصطلح التحفيز العضوي (إنگليزية: organocatalysis، لفظ منحوت من مصطلحي "محفز" و"عضوية") إلى أحد أشكال التحفيز، حيث يتزايد معدل التفاعلات الكيمائية بواسطة المحفز العضوي والذي يتكون من الكربون، الهيدروجين، الكبريت والعناصر الكيميائية الأخرى الموجودة في المركبات العضوية.[3][4][5][6][7][8] بسبب تشابهها في التركيب والوصف، غالبًا ما يُخلط بينها وبين التسمية الخاطئة للإنزيمات نظرًا لتأثيراتها المماثلة على معدلات التفاعل وأشكال التحفيز المتضمن.
يمكن وصف المحفزات العضوية التي تعرض وظيفة الأمين الثانوية بأنها تؤدي إما تحفيز الإينامين (عن طريق تكوين كميات محفزة من نيوكليوفيل الإينامين المنشط) أو الإيمينيوم (عن طريق تكوين تفحيز كميات من إلكتروفيل الإيمينيوم المنشط). هذه الآلية نموذجية للتحفيز العضوي التساهمي. عادة ما يتطلب الارتباط التساهمي للركيزة تحميل محفز عالي (لتحفيز البرولين عادةً 20-30 & nbsp؛ مول٪). تسهل التفاعلات غير التساهمية مثل ترابط-الهيدروجين تحميل المحفز المنخفض (حتى 0.001 & nbsp؛ مول٪).
يوفر التحفيز العضوي العديد من المزايا. ليست هناك حاجة للتحفيز المعدني وبالتالي المساهمة في الكيمياء الخضراء. في هذا السياق، أستخدمت الأحماض العضوية البسيطة كمحفزات لتعديل السليلوز في الماء على نطاق متعدد الأطنان.[9] عندما يكون المحفز العضوي كيرالي (يدوي) يتم فتح طريق للتحفيز الغير متماثل، على سبيل المثال استخدام الپرولين في تفاعل ألدول مثال على الكيرالية و الكيمياء الخضراء.[10]
مقدمة
تعتمد المحفزات العضوية المنتظمة تعتمد على النيتروجين مثل الفلفليدين المستخدم في تكثيف كنوڤيناگل.[11] يستخدم DMAP في تفاعلات الأسترة[12] ويستخدم DABCO في تفاعل بايليس-هيلمان.[13] أما ملح الثيازوليوم فيستخدم في تفاعل ستيتر. لهذه المحفزات والتفاعلات تاريخ طويل ولكن الاهتمام الحالي في التحفيز العضوي يتركز على التحفيز غير المتماثل مع المحفزات الكيرالية، المسماة التحفيز العضوي غير المتماثل أو التحفيز العضوي الانتقائي. تطور رد فعل رائد في السبعينيات يسمى رد فعل هايوس-پاريش-إيدير- سوير-ڤيتشيرت. بين عامي 1968 و1997، لم يكن هناك سوى عدد قليل من التقارير عن استخدام الجزيئات العضوية الصغيرة كمحفزات للتفاعلات غير المتماثلة (ربما يكون تفاعل هايوس-پاريش هو الأكثر شهرة)، ولكن اعتبرت هذه الدراسات الكيميائية تفاعلات كيميائية فريدة أكثر من كونها متكاملة. أجزاء من حقل أكبر مترابط.[14]
في هذا التفاعل، يكون الپرولين الكيرالي الذي يتواجد بشكل طبيعي هو المحفز الكيرالي في تفاعل ألدول. المادة الأولية هي ثلاثي الكيتون الكيرالي وتتطلب 3٪ فقط من الپرولين للحصول على منتج التفاعل، الكيتول في 93٪ فائض متماثل. وهذا هو المثال الأول لتفاعل ألدول غير المتماثل المحفز بالأحماض الأمينية.[15][16]
يعتمد التركيب غير المتماثل لكيتون ڤيلاند-مايشر (1985) أيضًا على الپرولين وكان التطبيق المبكر الآخر أحد التحولات في التخليق الكلي للإريثرومايسين بواسطة روبرت وودوارد (1981).[17] يركز ملخص المراجعة المصغرة على أمثلة حديثة مختارة من التخليق الكلي للمنتجات الطبيعية والدوائية باستخدام التفاعلات التحفيزية العضوية.[18]
تعتبر العديد من المحفزات العضوية اللولبية تكيفاً للربيطة الكيرالية (والتي تحفز مع مركز معدني أيضًا تفاعلات غير متماثلة) ويتداخل كلا المفهومين إلى حد ما.
عام 1835، بدأ الكيميائي السويدي الشهير جاكوب برزيليوس في رؤية تلك الأنماط. في التقرير السنوي للأكاديمية الملكية السويدية للعلوم الذي يصف أحدث تقدم في الفيزياء والكيمياء، نص على اكتشاف "قوة" جديدة يمكنها "توليد نشاط كيميائي"، وسرد التقرير العديد من الأمثلة التي أدى فيها وجود مادة ما إلى بدء تفاعل كيميائي معين، موضحاً كيف بدت هذه الظاهرة أكثر شيوعاً مما كان يعتقد سابقاً. كان يعتقد أن المادة لها قوة محفزة وأطلق على الظاهرة نفسها محفزاً.
سرعة المحفزات في إنتاج اللدائن والعطور والأطعة ذات النكهات حيث مرت كميات كبيرة من المواد عبر ماصات الكيميائيين منذ زمن برزيليوس. لقد اكتشفوا عدداً كبيراً من المحفزات القادرة على تكسير الجزيئات أو ضمها معاً. بفضل هذه المحفزات، تمكنا كبشر من استخراج آلاف المواد المختلفة التي نستخدمها في حياتنا اليومية، مثل الأدوية واللدائن والعطور والنكهات الغذائية.
بشكل مستقل، اكتشف بنيامين ليست وديڤد مامكيلان مفهوماً جديداً تماماً للتحفيز العضوي. ومنذ عام 2000، يمكن تشبيه التطورات التي حدثت في هذا المجال، تقريباً كحمى الهروع إلى الذهب. ولكن، احتفظ بنيامين وديڤد بمكانة رائدة. لقد صمما العديد من المحفزات العضوية الرخيصة والمستمرة، والتي يمكن استخدامها لتنحفيز مجموعة كبيرة من التفاعلات الكيميائية.
لا تتكون المحفزات العضوية غالباً من جزئيات بسيطة فحسب، بل يمكنها في بعض الحالات العمل كحزام ناقل تماماً مثل إنزيمات الطبيعة. في السابق، كان من الضروري في عمليات الإنتاج الكيميائي عزل كل منتج وسيط وتنقيته. وإلا فإن حجم المنتجات الثانوية سيكون كبيراً جداً. أدى هذا إلى فقدان بعض المادة في كل خطوة من البناء الكيميائي. تعتبر المحفزات العضوية أكثر مرونة. حيث يمكن في كثير من الأحيان إجراء عدة خطوات في عملية الإنتاج في تسلسل غير منقطع. يسمى هذا بالتفاعل التعاقبي. واستطاع ذلك التفاعل أن يقلل بشكل كبير من النفايات في التصنيع الكيميائي.
صياغة مصطلح التحفيز العضوي
عندما استعد ديڤد ماكميلان لنشر نتائجه، أدرك أن مفهوم التحفيز الكيميائي الذي اكتشفه يحتاج إلى اسم. نجح الباحثون سابقاً في تحفيز التفاعلات الكيميائية باستخدام جزيئات عضوية صغيرة، لكن تلك كانت أمثلة معزولة ولم يدرك أحد أن الطريقة يمكن تعميمها. أراد ماكميلان العثور على مصطلح لوصف الطريقة حتى يفهم الباحثون الآخرون أن هناك المزيد من المحفزات العضوية لاكتشافها. وقع اختياره على مصطلح التحفيز العضوي Organiccatalysis.
في يناير 2000، وقبل أن ينشر بنيامين ليست اكتشافه مباشرة، قدم ديڤد ماكميلان ورقته للنشر في مجلة علمية. تنص المقدمة على ما يلي: "" هيا بن نقدم استراتيجية جديدة للتحفيز العضوي نتوقع لها أن تكون قادرة على القيام بمجموعة من التحولات غير المماثلة".
أهمية المحفزات العضوية
على الجانب الآخر، تعمل المحفزات الحيوية بدقة مذهلة، تتكون المحفزات العضوية تلك من البروتينات، ويطلق عليها "الإنزيمات". تحتوي جميع الكائنات الحية على آلاف الإنزيمات المختلفة التي تحرك التفاعلات الكيميائية الضرورية للحياة داخل الجسم. العديد من الإنزيمات متخصصة في التحفيز غير المتماثل، وتشكل دائماً صورة مرآة واحدة من الصورتين الممكنتين للمركب. كما تعمل تلك المحفزات العضوية جنباً إلى جنب في تناغم رائع. فعندما ينتهي إنزيم من التفاعل، يتولى إنزيم آخر المهمة. وبهذه الطريقة، يمكن للمحفزات العضوية بناء جزيئات معقدة بدقة مذهلة، مثل الكوليسترول أو الكلوروفيل، أو سم الإستركنين، وهو أحد الجزئيات المعقدة للغاية.
نظراً لأن الإنزيمات عبارة عن محفزات فعالة، فقد حاول الباحثون في التسعينيات تطوير متغيرات إنزيمية جديدة لدفع التفاعلات الكيميائية التي تحتاجها البشرية. إحدى المجموعات البحثية التي تعمل على هذا كان مقرها معهد سكريپس للأبحاث في جنوب كاليفورنيا وكان بقيادة كارلوس يارباس الثالث. كان بنيامين ليست في منصب ما بعد الدكتوراه في مجموعة يارباس البحثية. ولدت عند بنيامين ليست حينها تلك الفكرة الرائعة التي أدت إلى الاكتشاف الذي حاز به جائزة نوبل للكيمياء 2021.
إذا قارنا قدرة الطبيعة على بناء إبداعات كيميائية مع قدرتنا الخاصة سنكتشف أننا علقنا لفترة طويلة في العصر الحجري. أنتج التطور عبر ملايين السنين أدوات دقيقة ومذهلة، هي الإنزيمات، تلك الإنزيمات قادرة على المساهمة في بناء المركبات الجزيئية التي تعطي الحياة أشكالها وألوانها ووظائفها. عندما بدأ الكيميائيون في ربط هذه التحف الكيميائية، نظروا إليها بإعجاب وذهول. كانت المطارق والأزاميل في صناديق أدواتهم للبناء الجزيئي بدائية وغير دقيقة، لذلك غالباً ما انتهت محاولاتهم في نسخ منتجات الطبيعة إلى الكثير من المنتجات الثانوية غير المرغوب فيها.
أدى الاكتشاف الذي حصل على جائزة نوبل في الكيمياء 2021 إلى الارتقاء بالبناء الجزيئي إلى مستوى جديد، فهو لم يجعل الكيمياء أكثر أمناً للبيئة فحسب، بل سهل أيضاً إنتاج جزيئات غير متماثلة عبر التحفيز العضوي غير المتماثل. ذلك المفهوم الذي طوره بنيامين ليست وديفيد ماكميلان بسيط بقدر ما هو رائع. الحقيقة هي أن الكثير من الناس تساءلوا لماذا لم نفكر في الأمر من قبل؟ ليس من السهل الإجابة عن هذا السؤال، ولكن قبل أن نحاول، نحتاج إلى إلقاء نظرة سريعة على التاريخ.
في التسعينيات، عمل بنيامين ليست على الأجسام المضادة التحفيزية. ترتبط تلك الأجسام المضادة بالفيروسات أو الجراثيم الغريبة في الجسم. عمل الباحثون في معهد سكيبس على إعادة تصميم تلك الأجسام حتى يتمكنون من إحداث تفاعلات كيميائية بدلاً من الارتباط بالأجسام الغريبة. أثناء عمل بنيامين مع الأجسام المضادة المحفزة، بدأ في التفكير في كيفية عمل الإنزيمات بالفعل. عادة ما تكون جزيئات ضخمة مبنية من مئات الأحماض الأمينية. بالإضافة إلى هذه الأحماض الأمينية، تحتوي نسبة كبيرة من الإنزيمات أيضاً على معادن تساعد في دفع العمليات الكيميائية. لكن- وهذه هي النقطة- تشارك العديد من الإنزيمات في تفاعلات كيميائية تحفيزية دون مساعدة المعان. إذ تتم التفاعلات عبر حمض أميني واحد أو عدد قليل من الأحماض الأمينية الفردية في الإنزيمات.
كان سؤال بنيامين العبقري هو هل يجب أن تكون الأحماض الأمينية جزءاً من الإنزيم لتحفيز تفاعل كيميائي ما؟ أو هل يمكن لحمض أميني واحد أو جزئيات بسيطة أخرى مماثلة القيام بنفس الوظيفة.
كان يعلم أن هناك بحثاً من أوائل التسعينيات استخدم حمض أميني يسمى البرولين كمحفز- لكن حدث هذا قبل أكثر من 25 عاماً من سؤاله. لكن إذا كان البرولين حافزاً فعالاً، فربما استمر شخص ما في العمل عليه؟ اعتقد بنيامين ليست أن السبب وراء عدم استمرار أي شخص في دراسة الظاهرة هو أنها لم تعمل بشكل جيد. دون أي توقعات حقيقية، اختبر بنيامين ما إذا كان البرولين يمكن أن يحفز تفاعل ألدول، حيث تربط ذرات الكربون جزيئين مختلفين معاً. لقد كانت محاولة بسيطة، ولكنها نجحت على الفور.
لم يكتشف ليست أن البرولين عامل محفز فعال فحسب كسابقه، بل أظهر أيضاً أن هذا الحمض الأميني يمكن أن يؤدي إلى تحفيز غير متماثل. من بين صورتي المرآة المحتملتين، كانت تتشكل إحداهما أكثر من الأخرى. وعلى عكس أولئك الذين اختبروا البرولين سابقاً كمحفز، أدرك بنيامين الإمكانات الهائلة التي يمكن أن تمتلكها تجربته. بالمقارنة مع كل من المعادن والإنزيمات، يعتبر البرولين أداة مثالية للكيميائيين. فالبرولين جزيء بسيط للغاية ورخيص وصديق للبيئة. عندما نشر بحثه في فبراير 2000، وصف بنيامين التحفيز غير المماثل مع الجزيئات العضوية كمفهوم جديد لديه العديد من الفرص المستقبلية، ولم يكن وحده في هذا الرأي. ففي مختبر بعيد في شمال كاليفورنيا، كان ديڤد ماكميلان يعمل أيضاً لتحقيق نفس الهدف.
قبل عامين، انتقل ديڤد ماكميلان من جامعة هارفرد إلى جامعة كاليفورنيا، بركلي. عمل ماكميلان في هارفرد على تحسين التحفيز غير المتماثل باستخدام المعادن. كان مجالاً جاذباً للكثير من الباحثين، لكن ديڤد ماكميلان لاحظ كيف أن المحفزات التي تم تطويرها نادراً ما تستخدم في الصناعة. بدأ ماكميلان يفكر في السبب، وافترض أن المعادن الحساسة كانت بكل بساطة صعبة للغاية ومكلفة للاستخدام.
كما فعل بنيامين، عرف ماكميلان أن تحقيق الظروف الخالية من الأكسجين والرطوبة التي تتطلبها بعض المحفزات المعدنية أمر بسيط في المختبر، ومعقد في الصناعة. فاستنتج أن تلك الأدوات الكيميائية التي يطورها تحتاج إلى إعادة تفكير كي تكون مفيدة صناعياً. لذلك، عندما انتقل إلى بركلي، ترك المعادن خلف ظهره، وبدأ في التفكير في تطوير شكل أبسط من المحفزات بدلاً من المعادن. بدأ ماكميلان في تصميم جزئيات عضوية بسيطة- تماماً مثل المعادن- قادرة على توفير الإلكترونيات أو استيعابها مؤقتاً. والجزئيات العضوية هي الجزئيات التي تبني كل الكائنات الحية. ولدى تلك الجزئيات هيكل ثابت من ذرات الكربون. ترتبط المجموعات الكيميائية بهيكل الكربون، وغالباً ما يحتوي على الأكسجين أو النيتروجين أو الكبريت أو الفسفور.
مضاعفة كفاءة التصنيع
أحد الأمثلة على الطريقة التي أدى بها التحفيز العضوي إلى مكونات جزيئية أكثر كفاءة هو أطروحة توليف جزيء الإستركنين الطبيعي والمعقد. قد يتعرف الكثير من محبي الروايات على الإستركنين من كتب الروائية أجاثا كريستي. ومع ذلك فبالنسبة للكيميائييين، يشبه الإستركنين مكعب الروبيك، فهو تحد ترغب في حله في أقل عدد ممكن من الخطوات. عندما تم تصنيع الإستركنين لأول مرة عام 1952، تطلب الأمر 29 تفاعلاً كيميائياً مختلفاً وشكلت 0.0009% فقط من المادة الأولية للإستركنين. وتم إهدار الباقي. وفي عام 2011، تمكن الباحثون من استخدام التحفيز العضوي ورد الفعل التعاقبي لبناء الإستركنين في 12 خطوة فقط. وكانت عملية الإنتاج أكثر كفاءة بمقدار 7000 مرة.
صناعة الأدوية
كان للتحفيز العضوي أثر كبير على البحوث الدوائية والتي تتطلب غالباً تحفيزاً غير متماثل. وإلى أن يتمكن الكيميائيون من إجراء تحفيز غير متماثل، احتوت العديد من المستحضرات الدوائية على صور معكوسة غير مرغوبة للجزيء. صورة الجزيء هي معكوسة في المرآة، يكون أحدهما نشطاً، بينما يكون للآخر تأثيرات غير مرغوب فيها. ومن الأمثلة الكارثية على ذلك فضيحة الثاليدومايد في الستينيات. حيث تسببت صورة دواء الثاليدومايد في حدوث تشوهات خطيرة في آلاف الأجنة البشرية. قيل عن الحدث أنه "أكبر كارثة طبية صنعها الإنسان على الإطلاق" ونتج عناه 10 آلاف طفل مشوه بمختلف الدرجات في 46 دولة ما بين 1950 و1960.
باستخدام التحفيز العضوي، تمكن الباحثون من إنتاج كميات كبيرة من الجزيئات غير المتماثلة المختلفة ببساطة. واستطاع الباحثون تصنيع مواد علاجية محتملة بكميات لم يمكن عزلها سهلاً إلا بكميات صغيرة من النباتات النادرة أو الكائنات الحية في أعماق البحار. استخدمت شركات الأدوية التقنية بالطبع لتسهيل إنتاج المستحضرات الدوائية المصنعة. ومن الأمثلة على ذلك إنتاج الباروكستين الذي يستخدم لعلاج القلق والاكتئاب، والأدوية المضادة للفيروسات مثل الأوسيلتاميفير الذي يستخدم لعلاج التهابات الجهاز التنفسي.
فئات المحفزات العضوية
يمكن تجميع المحفزات العضوية للتخليق غير المتماثل في عدة فئات:
- الجزيئات الحيوية: الپرولين، الفنايلألانين، الأمينات الثانوية بصفة عامة.[19] شبه قلويات الكينا، وخاصة قليلات الپپتيد.
- المحفزات التخليقية المشتقة من الجزيئات الحيوية.
- محفزات رابطة الهيدروجين، وتشمل TADDOLS المشتقة من البينول مثل النوبين، والمحفزات العضوية المعتمدة على الثوريات.
- أملاح التريازوليوم كمحفزات الجيل التالي في تفاعل ستيتر.
أمثلة على التفاعلات غير المتماثلة التي تنطوي على محفزات عضوية:
- تفاعل ديلز-ألدر الغير متماثلة
- تفاعلات مايكل الغير متماثلة
- تفاعلات مانيخ الغير متماثلة
- Shi epoxidation
- هدرجة ناقل المحفز العضوي
الپرولين
تم مراجعة الپرولين كمحفز عضوي.[20][21]
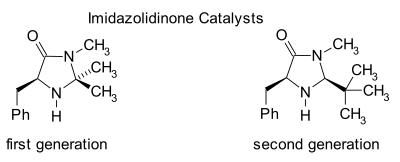
الإيميدازوليدينون كمحفز عضوي
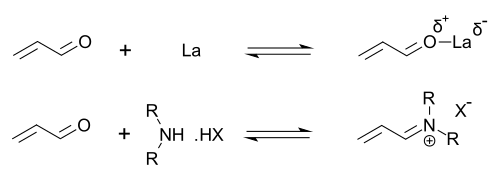
الإيميدازوليدينونات هي محفزات للعديد من التحولات مثل تفاعلات ديلز-ألدر غير المتماثلة وإضافات مايكل. تحفز المحفزات الكيرالية التفاعلات الغير متماثلة، غالبًا مع انتقائية تماثلية عالية. يعمل هذا المحفز عن طريق تكوين أيون إيمينيوم مع مجموعات كاربونيل من الألدهيدات غير المشبعة (الإنال) والإنون في توازن كيميائي سريع. يشبه "تنشيط الإيمينيوم" هذا تنشيط مجموعات الكربونيل بواسطة حمض لويس وكلا المحفزين يخفضان الركيزة LUMO:[22][23]
إن مادة الإيمينيوم الوسيطة العابرة هي حافز كيرالي يتم نقله إلى منتج التفاعل عن طريق الحث الكيرالي. ُأستخدمت المحفزات في تفاعل ديلز-ألدر، إضافات مايكل، عمليات ألكلة فريدل-كرافت، هدرجات النقل وepoxidations.
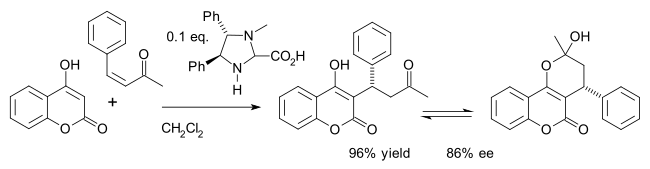
أحد الأمثلة على ذلك هو التخليق غير المتماثل للدواء، هو الوارافين (في حالة توازن مع الهميكتال) في إضافة مايكل لـ4-هيدروكسي كومارين والبنزيليدينياسيتون:[24]
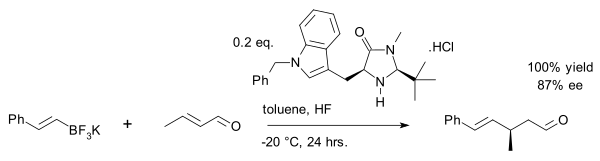
والاستخدام الحديث هو ألكلة الڤينيل للكروتونالدهيد مع ملح ثلاثي فلوريد البورات العضوية:[25]
لأمثلة أخرى لاستخدام الإيميدازوليدينون، انظر: هدرجة الناقل المحفز عضوياً وتفاعلات ديلز ألدر الغير متماثلة.
أيون الإيمينيون
تتكون الجزئيات العضوية من عناصر بسيطة ومشتركة، ولكن يعتمد اختلافها على كيفية تجميعها معاً. يترتب على ذلك الاختلاف الكبير في الخصائص المعقدة. وفق معرفة ماكميلان بالكيمياء، أدرك أنه لكي يحفز الجزيء العضوي التفاعل الذي يرغب فيه، يجب أن يصبح قادراً على تكوين "أيون إيمينيون" يحتوي أيون الإيمينيوم على ذرة نيتروجين وذرة النترجوين محبة للإلكترونات. اختار ماكميلان العديد من الجزئيات العضوية ذات الخصائص الصحيحة، ثم اختبر قدرتها على تحفيز تفاعل ديلز-أدلر. يستخدم الكيميائيون تفاعل دايلز-أدلر لبناء حلقات من ذرات الكربون.
وكما كان يأمل ماكميلان ويعتقد، عمل التفاعل بشكل رائع، عملت بعض الجزئيات العضوية بشكل ممتاز أيضاً في التحفيز غير المتماثل، فمن بين صورتين محتملتين، ظهرت إحداهما بأكثر من 90% من المنتج. وبذلك تمكن ماكميلان أيضاً من تحقيق التحفيز العضوي الغير متماثل. أدى اكتشاف ماكميلان مع اكتشاف ليست لفوزهما بجائزة نوبل في الكيمياء 2021.
الثيوروريا محفز عضوي
تشتمل مجموعة كبيرة من المحفزات العضوية على جزء اليوريا أو ثيوريا. توفر مشتقات اليوريا الفعالة تحفيزيًا (thio) والتي يطلق عليها (thio) محفزات اليوريا العضوية تفاعلات مزدوجة ذات رابطة هيدروجينية صريحة لتنسيق وتفعيل ركائز قبول رابطة-الهيدروجين.[26]
المصادر
- ^ Justus von Liebig, Justus (1860). "Ueber die Bildung des Oxamids aus Cyan". Annalen der Chemie und Pharmacie. 113 (2): 246–247. doi:10.1002/jlac.18601130213.
- ^ W. Langenbeck (1929). "Über organische Katalysatoren. III. Die Bildung von Oxamid aus Dicyan bei Gegenwart von Aldehyden". Liebigs Ann. 469: 16–25. doi:10.1002/jlac.19294690103.
- ^ Berkessel, A., Groeger, H. (2005). Asymmetric Organocatalysis. Weinheim: Wiley-VCH. ISBN 978-3-527-30517-9.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ^ Special Issue: List, Benjamin (2007). "Organocatalysis". Chem. Rev. 107 (12): 5413–5883. doi:10.1021/cr078412e.
- ^ Peter I. Dalko; Lionel Moisan (2004). "In the Golden Age of Organocatalysis". Angew. Chem. Int. Ed. 43 (39): 5138–5175. doi:10.1002/anie.200400650. PMID 15455437.
- ^ Matthew J. Gaunt; Carin C.C. Johansson; Andy McNally; Ngoc T. Vo (2007). "Enantioselective organocatalysis". Drug Discovery Today. 12 (1/2): 8–27. doi:10.1016/j.drudis.2006.11.004. PMID 17198969.
- ^ Dieter Enders; Christoph Grondal; Matthias R. M. Hüttl (2007). "Asymmetric Organocatalytic Domino Reactions". Angew. Chem. Int. Ed. 46 (10): 1570–1581. doi:10.1002/anie.200603129. PMID 17225236.
- ^ Peter I. Dalko; Lionel Moisan (2001). "Enantioselective Organocatalysis". Angew. Chem. Int. Ed. 40 (20): 3726–3748. doi:10.1002/1521-3773(20011015)40:20<3726::AID-ANIE3726>3.0.CO;2-D.
- ^ International Patent WO 2006068611 A1 20060629 " Direct Homogeneous and Heterogeneous Organic Acid and Amino Acid-Catalyzed Modification of Amines and Alcohols" Inventors: Armando Córdova, Stockholm, Sweden; Jonas Hafrén, Stockholm, Sweden.
- ^ Example 4 in U.S. Patent 3,975,440 August 17, 1976, Filed Dec. 9, 1970 Zoltan G. Hajos and David R. Parrish.
- ^ List, B. (2010). "Emil Knoevenagel and the Roots of Aminocatalysis". Angewandte Chemie International Edition in English. 49 (10): 1730–1734. doi:10.1002/anie.200906900. PMID 20175175.
- ^ Neises, Bernhard; Steglich, Wolfgang (July 1978). "Simple Method for the Esterification of Carboxylic Acids". Angewandte Chemie International Edition in English. 17 (7): 522–524. doi:10.1002/anie.197805221.
- ^ Basavaiah, Deevi; Rao, Anumolu Jaganmohan; Satyanarayana, Tummanapalli (March 2003). "Recent Advances in the Baylis−Hillman Reaction and Applications". Chemical Reviews. 103 (3): 811–892. doi:10.1021/cr010043d. PMID 12630854.
- ^ "The advent and development of organocatalysis" David C. MacMillan, NATUREVol 455|18 September 2008|doi:10.1038/nature07367
- ^ Z. G. Hajos, D. R. Parrish, German Patent DE 2102623 1971
- ^ Zoltan G. Hajos; David R. Parrish (1974). "Asymmetric synthesis of bicyclic intermediates of natural product chemistry". J. Org. Chem. 39 (12): 1615–1621. doi:10.1021/jo00925a003.
- ^ R. B. Woodward; E. Logusch; K. P. Nambiar; K. Sakan; D. E. Ward; B. W. Au-Yeung; P. Balaram; L. J. Browne; et al. (1981). "Asymmetric total synthesis of erythromcin. 1. Synthesis of an erythronolide A secoacid derivative via asymmetric induction". J. Am. Chem. Soc. 103 (11): 3210–3213. doi:10.1021/ja00401a049.
- ^ B. -F. Sun (2015). "Total synthesis of natural and pharmaceutical products powered by organocatalytic reactions". Tetrahedron Lett. 56 (17): 2133–2140. doi:10.1016/j.tetlet.2015.03.046.
- ^ Bertelsen, Søren (2009). "Organocatalysis—after the gold rush". Chemical Society Reviews. 38 (8): 2178–89. doi:10.1039/b903816g. PMID 19623342.
- ^ Gaunt, M. J.; Johansson, C. C. C.; McNally, A.; Vo, N. T. (2007). "Enantioselective organocatalysis". Drug Discovery Today. 12 (1–2): 8–27. doi:10.1016/j.drudis.2006.11.004. PMID 17198969.
- ^ Kucherenko, A. S.; Siyutkin, D. E.; Maltsev, O. V.; Kochetkov, S. V.; Zlotin, S. G. (2013). "Asymmetric organocatalysis: From proline to highly efficient immobilized organocatalysts". Russian Chemical Bulletin. 61 (7): 1313. doi:10.1007/s11172-012-0177-4. S2CID 93168492.
- ^ Gérald Lelais; David W. C. MacMillan (2006). "Modern Strategies in Organic Catalysis: The Advent and Development of Iminium Activation" (PDF). Aldrichimica Acta. 39 (3): 79.
- ^ Erkkilä, Anniinä; Majander, Inkeri; Pihko, Petri M. (2007). "Iminium Catalysis". Chem. Rev. 107 (12): 5416–5470. doi:10.1021/cr068388p. PMID 18072802.
- ^ Nis Halland; Tore Hansen; Karl Anker Jørgensen (2003). "Organocatalytic Asymmetric Michael Reaction of Cyclic 1,3-Dicarbonyl Compounds and α,β-Unsaturated Ketones - A Highly Atom-Economic Catalytic One-Step Formation of Optically Active Warfarin Anticoagulant". Angew. Chem. Int. Ed. 42 (40): 4955–4957. doi:10.1002/anie.200352136. PMID 14579449.
- ^ Sandra Lee; David W. C. MacMillan (2007). "Organocatalytic Vinyl and Friedel-Crafts Alkylations with Trifluoroborate Salts" (PDF). J. Am. Chem. Soc. 129 (50): 15438–15439. doi:10.1021/ja0767480. PMID 18031044.
- ^ Madarász, Ádám; Dósa, Zsolt; Varga, Szilárd; Soós, Tibor; Csámpai, Antal; Pápai, Imre (July 2016). "Thiourea Derivatives as Brønsted Acid Organocatalysts" (PDF). ACS Catalysis. 6 (7): 4379–4387. doi:10.1021/acscatal.6b00618.