ثالث أكسيد الحديد

| |
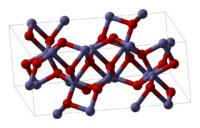
| |
| الأسماء | |
|---|---|
| أسماء أخرى
Ferric oxide, Hematite, ferric oxide, ferric iron, red iron oxide, synthetic maghemite, colcothar
| |
| المُعرِّفات | |
| رقم CAS | |
| ECHA InfoCard | 100.013.790 |
| E number | E172(ii) (colours) |
PubChem CID
|
|
| رقم RTECS |
|
CompTox Dashboard (EPA)
|
|
| الخصائص | |
| الصيغة الجزيئية | Fe2O3 |
| كتلة مولية | 159.69 g/mol |
| المظهر | red-brown solid |
| الرائحة | odorless |
| الكثافة | 5.242 g/cm3, solid |
| نقطة الانصهار | |
| قابلية الذوبان في الماء | insoluble |
| البنية | |
| البنية البلورية | rhombohedral |
| الكيمياء الحرارية | |
| الإنتالپية المعيارية للتشكل ΔfH |
−825.50 kJ/mol |
| المخاطر | |
تبويب الاتحاد الاوروپي (DSD)
|
not listed |
| نقطة الوميض | non-flammable |
| مركبات ذا علاقة | |
أنيونات أخرى
|
ثالث فلوريد الحديد |
كاتيونات أخرى
|
ثالث أكسيد المنغنيز, ثالث أكسيد الكوبالت |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
أكسيد الحديد الثلاثي أو القُلْقُطَار مركب كيميائي له الصيغة Fe2O3 ، ويكون على شكل مسحوق بلوري بني محمر .وهو المكون الأساسي للصدأ.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص
توجد منه عدة أنماط:
النمط ألفا
يمتلك ألفا أكسيد الحديد الثلاثي α-Fe2O3 بنية مشابهة للكوروندوم (α-Al2O3)، وهو النمط الأكثر شيوعاً. يوجد طبيعيا في معدن الهيماتيت والذي يمثل خامة الحديد الرئيسية. تتفاوت المغناطيسية الحديدية حسب درجة الحرارة. فعند درجات حرارة أقل من 260 كلفن يكون لا مغناطيسياً، في حين عند درجات حرارة بين 260 و950 كلفن تكون له خواص مغناطيسية.
النمط بيتا
له بنية مكعبة مركزية الوجه، شبه مستقر، ويتحول إلى النمط ألفا عند درجات حرارة تتجاوز 500°س. يحضر باختزال الهيمياتيت بالكربون، أو بالتحلل الحراري لمحلول كلوريد الحديد الثلاثي، أو التفكك الحراري لمركب كبريتات الحديد الثلاثي.
النمط غاما
وهو نمط مكعب، شبه مستقر، يتحول إلى النمط ألفا عند درجات الحرارة المرتفعة، ويوجد طبيعيا في معدن الميغاميت Maghemite.
التحضير
يحضر أكسيد الحديد الثلاثي بالتفكك الحراري لمركب أكسيد هيدروكسيد الحديد الثلاثي:
2FeO(OH)2 –Δ→ Fe2O3 + H2O
الاستخدامات
- يستخدم في تعدين الألومنيوم حيث يتفاعل الألومنيوم مع أكسيد الحديد ليتشكل الحديد الحر وأكسيد الألومنيوم في تفاعل ناشر للحرارة
2Al + Fe2O3 → 2Fe + Al2O3
- يستعمل كخضاب حيث يعطي اللون البني تحت الأسماء Pigment Brown 6و Pigment Brown 7وPigment Red 101[1]. .
انظر أيضا
المصادر
- ^ Paint and Surface Coatings: Theory and Practice William Andrew Inc. ISBN 1-884207-73-1