ستايرين
| |
| |
| الأسماء | |
|---|---|
| اسم أيوپاك المفضل
Ethenylbenzene[1] | |
| أسماء أخرى | |
| المُعرِّفات | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.002.592 |
| KEGG | |
PubChem CID
|
|
| رقم RTECS |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | C8H8 |
| كتلة مولية | 104.15 گ/مول |
| المظهر | سائل دهني عديم اللون. |
| الرائحة | sweet, floral[2] |
| الكثافة | 0.909 گ/سم3 |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | 0.03% (20°س)[2] |
| log P | 2.70 [3] |
| ضغط البخار | 5 mmHg (20°C)[2] |
| القابلية المغناطيسية | -68.2·10−6 cm3/مول |
| معامل الانكسار (nD) | 1.5469 |
| اللزوجة | 0.762 سپ عند 20 °گ |
| البنية | |
| Dipole moment | 0.13 د |
| المخاطر | |
| خطر رئيسي | flammable, toxic |
| صفحة بيانات السلامة | MSDS |
| توصيف المخاطر | R10 R36 |
| تحذيرات وقائية | S38 قالب:S20 S23 |
| NFPA 704 (معيـَّن النار) | |
| نقطة الوميض | 31 °C (88 °F; 304 K) |
| حدود الانفجار | 0.9%-6.8%[2] |
| الجرعة أو التركيز القاتل (LD, LC): | |
LC50 (التركيز الأوسط)
|
2194 ppm (mouse, 4 hr) 5543 ppm (rat, 4 hr)[4] |
LCLo (المنشورة الأقل)
|
10,000 ppm (البشر، 30 دقيقة) 2771 ppm (الفئران، 4 ساعات)[4] |
| حدود التعرض الصحية بالولايات المتحدة (NIOSH): | |
PEL (المسموح)
|
TWA 100 ppm C 200 ppm 600 ppm (5-minute maximum peak in any 3 hours)[2] |
REL (الموصى به)
|
TWA 50 ppm (215 mg/m3) ST 100 ppm (425 mg/m3)[2] |
IDLH (خطر عاجل)
|
700 ppm[2] |
| مركبات ذا علاقة | |
الستايرينات;
المتعلقة بالمركبات العطرية ذات العلاقة |
پوليستايرين، ستيلبين< بنزين إيثيلي |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
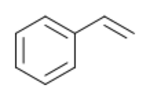
الستايرين، أو الستيرين، يُعرف أيضاً بنزين الإيثانول، نبزين الڤنيل، إيثان الفينيل، هو مركب عضوي صيغته الكيميائية C6H5CH=CH2. كأحد مشتقات البنزين، يتميز الستايرين بأنه سائل دهني عديم اللون يتبخر بسهولة وله رائحة حلوة، على الرغم من أن التركيزات العالية تكون رائحتها أقل قبولاً. الستايرين هو مركب باديء للپوليستايرين والكثير من الكو-پولميرات. في 2010 تم إنتاج حوالي 25 مليون طن من الستايرين.[5]
التواجد، التاريخ، والاستخدام
التواجد الطبيعي
التاريخ
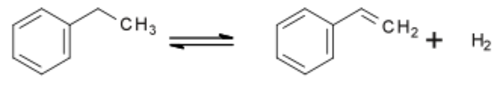
الإنتاج الصناعي من بنزين الإيثيل
مسارات صناعية أخرى
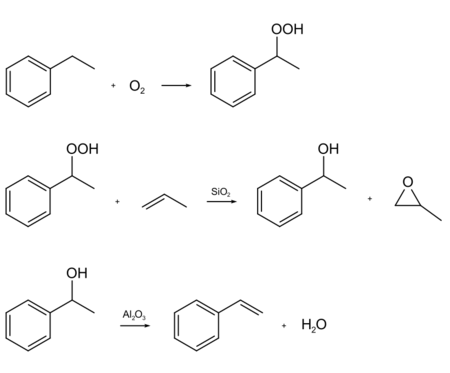
من بنزين الإيثيل والهيدروپروكسايد
من التولوين والميثانول
من البنزين والإيثان
التحضير المعملي
- C6H5CH=CHCO2H → :C6H5CH=CH2 + CO2
الپلمرة
الاستخدامات
الستايرين هو مركب متعدد الاستعمالات ويستخدم في صناعة الپوليستايرين المستخدم في كافة المواد المستعملة يومياً مثل مواد التغليف والعزل والمطاط الصناعي ومنتجات بلاستيكية أخري.
الآثار الصحية
إعادة المعالجة الحيوية
يمكن أن يستخدم الفطر الشبيه بالخميرة والمسمى المتفالية الجانسيلمية لمعالجة الهواء الملوث بالستايرين.[6]
المصادر
- ^ أ ب Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. pp. 4, 55, 379. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ أ ب ت ث ج ح خ NIOSH Pocket Guide to Chemical Hazards 0571
- ^ "Styrene_msds".
- ^ أ ب "Styrene". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ New Process for Producing Styrene Cuts Costs, Saves Energy, and Reduces Greenhouse Gas Emissions Archived 21 أبريل 2013 at the Wayback Machine, U.S. Department of Energy.
- ^ title=Isolation and characterisation of fungi growing on volatile aromatic hydrocarbons as their sole carbon and energy source|author1=Francesc X. PRENAFETA-BOLDU|author2=Andrea KUHN|author3=Dion M. A. M. LUYKX|author4=Heidrun ANKE|author5=Johan W. van GROENESTIJN|author6=Jan A. M. de BONT|volume=105|issue=4|pages=477-484|date=April 2001|
وصلات خارجية
- CDC - Styrene - NIOSH Workplace Safety and Health Topic
- Safety and Health Topics | Styrene (OSHA)
- OSHA-NIOSH 2018. Preventing Hearing Loss Caused by Chemical (Ototoxicity) and Noise Exposure Safety and Health Information Bulletin (SHIB), Occupational Safety and Health Administration and the National Institute for Occupational Safety and Health. SHIB 03-08-2018. DHHS (NIOSH) Publication No. 2018-124.
This article contains content from Wikimedia licensed under CC BY-SA 4.0. Please comply with the license terms.
تصنيفات:
- ECHA InfoCard ID from Wikidata
- Articles with changed KEGG identifier
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Short description is different from Wikidata
- ملوثات الهواء الخطرة
- مونمرات
- مسرطنات المجموعة 2B حسب تصنيف الوكالة الدولية لأبحاث السرطان
- مركبات الڤينيل
- مركبات الفينيل
- ألكينات
- الصحة والسلامة المهنية
- فينيلات
- كيماويات سلعية