يوديد الرصاص الثنائي
| |
| |
| الأسماء | |
|---|---|
| أسماء أخرى
Plumbous iodide
| |
| المُعرِّفات | |
| رقم CAS | |
| ECHA InfoCard | 100.030.220 |
CompTox Dashboard (EPA)
|
|
| الخصائص | |
| الصيغة الجزيئية | PbI2 |
| كتلة مولية | 461.01 g/mol |
| الكثافة | 6.16 g/cm3 |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | 0.044 g/100 mL (0 °C) 0.063 g/100 mL (20 °C) 0.41 g/100 mL (100 °C) [1] |
| نتاج قابلية الذوبان، Ksp | 8.49 x 10-9 |
| قابلية الذوبان | insoluble in ethanol soluble in alkalis |
| البنية | |
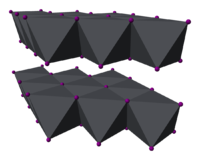
| البنية البلورية | Rhombohedral, hP3, SpaceGroup = P-3m1, No. 164 |
| هندسة إحداثية |
octahedral |
| المخاطر | |
تبويب الاتحاد الاوروپي (DSD)
|
Repr. Cat. 1/3 Harmful (Xn) Dangerous for the environment (N) |
| توصيف المخاطر | R61, R20/22, R33, R62, R50/53 |
| تحذيرات وقائية | S53, S45, S60, S61 |
| NFPA 704 (معيـَّن النار) | |
| نقطة الوميض | Non-flammable |
| مركبات ذا علاقة | |
أنيونات أخرى
|
ثاني فلوريد الرصاص ثاني كلوريد الرصاص ثاني بروميد الرصاص |
كاتيونات أخرى
|
ثاني يوديد القصدير |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
يوديد الرصاص الثنائي مركب كيميائي له الصيغة PbI2، ويكون على شكل بلورات صفراء .
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص
- ينحل مركب يوديد الرصاص في الماء بشكل ضعيف، فقط حوالي 0.1 غ/ 100 مل ماء عند 20°س . وحتى عند رفع درجة حرارة الماء إلى نقطة الغليان 100 °س فإن الانحلالية تزداد إلى 0.5 غ فقط. بالمقابل فإن يوديد الرصاص الثنائي ينحل بشكل جيد الأوساط القلوية بالإضافة إلى محلول يوديد البوتاسيوم.
- إن تسخين مركب يوديد الرصاص يؤدي إلى تغير لوني غير عكوس للبلورات من اللون الأصفر إلى اللون الأحمر القانئ ومن ثم إلى اللون الأحمر الداكن.
التحضير
- يحضر مركب يوديد الرصاص الثنائي من مزج محاليل مائية متساوية التركيز من نترات الرصاص الثنائي ويوديد البوتاسيوم حيث يترسب يوديد الرصاص الثنائي حسب المعادلة:
- Pb(NO3)2 (aq) + 2KI (aq) → PbI2 ↓ + 2KNO3
مع استمرار إضافة يوديد البوتاسيوم للمزيج ينحل الراسب المتشكل وذلك بسبب تشكل معقد لليود حسب المعادلة:
- PbI2 + KI → K[PbI3] aq
الاستخدامات
- يستخدم تفاعل ترسب يوديد الرصاص في الكيمياء التحليلية للكشف عن الرصاص وعن أنيون اليوديد.
المصادر
- Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4
- [1]
وصلات خارجية
- Case Studies in Environmental Medicine (CSEM): Lead Toxicity
- ToxFAQs: Lead
- National Pollutant Inventory - Lead and Lead Compounds Fact Sheet
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
الكلمات الدالة:

