نظرية العمليات المتالورجية
ساهم بشكل رئيسي في تحرير هذا المقال
|
نظرية العمليات المتالورجية Theory of Metallurgical Processes تصف العملية المتالورجية – بالإضافة إلى التصميم الهندسى والعوامل الإقتصادية – دراسة طاقات وسرعات التفاعلات المشمولة في العملية. فحساب حرارة التفاعلات، سواء أكانت طاردة أو ماصة للحرارة ، ضرورى لإنشاء الموازنة الحرارية للعملية وتحديد جدوى التفاعل. ويجب بعد ذلك حساب ثوابت الإتزان وحصيلة النواتج لإنشاء موازنة المواد. بالإضافة إلى ذلك، يشتمل عدد كبير من العمليات المتالورجية – سواء أكانت مائية أو حرارية أو كهربية – على عمليات أكسدة واختزال. وكل ما سبق هو مجال نظرية العمليات المتالورجية التى تشكل الأساس النظرى لعمليات الاستخلاص و المعالجات الأخرى التى تتم على الفلزات و السبائك. فمثلاً، استخلاص الذهب من خاماته بطريقة مائية هو عملية أكسدة، واستخلاص الحديد بطريقة حرارية في الفرن العالى هو عملية اختزال، واستخلاص الألومنيوم من Al2O3 بطريقة كهربية هو عملية اختزال، و كل هذه العمليات يمكن فهمها و دراستها من خلال موضوعات نظرية العمليات المتالورجية. وكما سيتضح لاحقاً، فإن عمليتى الأكسدة والاختزال – مع اسثناءات قليلة – هما عمليتان آنيتان أى تحدثان في نفس الوقت، ففهم هذه الأسس ضرورى لتطوير و رفع كفاءة العمليات المتالورجية.
الأكسدة والاختزال
يمكن تمييز أنواع مختلفة من عمليات الأكسدة كما يلى:
- تفاعلات الإضافة. وهى إضافة الأكسجين إلى ذرة أو أيون أو جزىء مثل:
C + O2 = CO2
- العمليات الكهركيميائية. وتشمل انتقال الإلكترونات من ذرة أو مجموعة ذرات. مثل
Cu + ½ O2 = CuO
تختلف هذه الحالة عن السابقةبسبب وجود انتقال للإلكترونات من النحاس إلى الأكسجين.
- الأكسدة مع الاختزال. (تفاعل عدم-التناسب) في هذه الحالة يقوم ذات الأيون بالأكسدة والاختزال في نفس الوقت، مثل:
ويتم هذا التفاعل كما يلى:
- التحويل. وهذا التفاعل خاص بالقليل من الكبريتيدات التى تنتج فلزاً و SO2 مثل PbS و Cu2S و Ni3S2 عندما تتفاعل مع الأكسجين في ظروف معينة، طبقاً للتفاعل الكلى الآتى:
MS + O2 = M + SO2
أما الاختزال فهو التفاعل العكسى للأكسدة. وقد يشمل نزع الأكسجين من أكسيد، مثل :
HgO = Hg + ½ O2
و تتم أيضاً تفاعلات مشابهة في المحاليل المائية مثل
و اختزال الأكسجين في المحلول له أهمية خاصة في المتالورجيا المائية لأنه يقوم بدور مُهَيمِن في العديد من التفاعلات، مثل إذابة الذهب في محلول السيانيد. أما العامل المختزل فهو ذلك الكاشف القادر على نزع الأكسجين أو إعطاء إلكترونات في التفاعل الكيميائى. والعوامل المختزلة الفعالة هى تلك القادرة على القيام بعدد كبير من تفاعلات الاختزال بسرعة. العوامل المختزلة الشائعة في درجات الحرارة العالية هى الكوك والفحم النباتى وأول أكسيد الكربون والهيدروجين. والعوامل المختزلة القوية في العمليات المتالورجية الحرارية هى الفلزات القلوية والفلزات الأرضية القلوية والألومنيوم.
باستثناء عمليات الأكسدة بالإضافة وأيون الكبريتيد إلى كبريتات والنيتريت إلى نيترات، يصاحب عمليات الأكسدة عمليات اختزال، أى أن تفاعلات الأكسدة والاختزال تحدث آنية (فى نفس الوقت). وقد تحدث عملية الأكسدة أو الاختزال بشكل متجانس أو بشكل متغاير
جهد الإلكترود
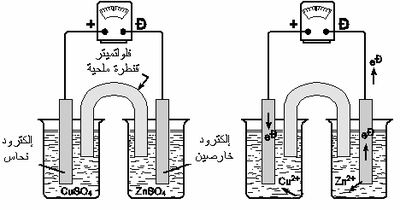
من الملائم في المتالورجيا المائية والكهربية أن تتم دراسة عمليات الأكسدة والاختزال عن طريق جهود الإلكترودات، أما في المتالورجيا الحرارية فالأنسب دراستهم عن طريق التغير في الطاقة الحرة. وكما سيتضح أدناه فإن كلا المصطلحين مرتبطان. يُقاس ميل المادة لأن تتأكسد أو تُخْتَزَل، أى أن تفقد أو تكتسب إلكترونات، يقاس ذلك بالفولت ويعرف بالجهد. فعند غمر شريحة من الخارصين في محلول واحد مول ZnSO4 وشريحة نحاس في محلول واحد مول CuSO4 وتوصيل الشريحتان بسلك، وتوصيل المحلولين بقنطرة ملحية لتفادى الاختلاط كما هو مبين في شكل 17-1، يُلاحظ أن الفلولتميتر يشير إلى 0,78 فولت، ويذوب الخارصين في كبريتات الخارصين ويترسب النحاس في كبريتات النحاس. وتنتقل الإلكترونات المتحررة في إلكترود الخارصين خلال السلك إلى إلكترود النحاس، وتنتشر أيونات الكبريتات ببطىء من محلول CuSO4 خلال القنطرة الملحية حتى تُكْمِل الدائرة الكهربية.
يُؤخذ جهد الإلكترود القياسى لتفاعل أيون الهيدروجين على أنه صفر. وأى تفاعل يشمل انتقال إلكترونات يمكن إجراؤه في خلية كهركيميائية ويمكن قياس جهده.
فى الأنظمة المائية يتغير جهد الإلكترود الخاص بفلز في المحلول مع تركيز الفلز. ويرتبط الجهد المَقِيس عند أى تركيز آخر مع الجهد القياسى بمعادلة نرنست:
حيث R هو ثابت الغازات = 8,314 جول/درجة حرارة، و T هى درجة الحرارة بالكلفن، و F هو الفارادى (1 فارادى = 96500 أمبير.ثانية أو 96500 كولوم) و Eo = جهد الإلكترود القياسى. وبالنسبة لإلكترود هيدروجين في درجة حرارة الغرفة فإن:
حيث pH هو الرقم الهيدروجينى = - لو[+H] ومن ثم بالنسبة للتفاعلات المشتملة على أيونات هيدروجين، فإن جهد الإلكترود سيكون معتمداً على الرقم الهيدروجينى pH.
التميه والحلمأة
تَتَمَيَّه الأيونات في المحاليل المائية، أى أنها تُحاط بجزيئات الماء بسبب قطبية الماء. والكاتيونات عادة أكثر تَمَيُّهاً من الأنيونات بسبب صغر أحجامها، ومن ثم فشحنتها أكثر تركيزاً، وتستطيع أن تجذب جزيئات ماء أكثر. والأيونات المُتَمَيِّهَة لديها ميل لفقد أيونات +H أو -OH، وتسمى هذه العملية بالحَلْمَأَة (أو الحلمهة أو التحليل المائى)، ويمكن تمثيلها بالمعادلة العامة الآتية:
أو بصورة أبسط كما يلى:
ويعتمد ميل الأيون إلى الحلمأة على:
• نسبة شحنة الأيون إلى نصف قطره، أى كثافة الشحنة. فكلما زادت كثافة الشحنة كلما زادت الحلمأة الحادثة والعكس بالعكس.
• البنية الإلكترونية. الأيونات التى لديها بنية غاز خامل أقل ميلاً للحلمأة.
الأحماض والقواعد
الأحماض والقواعد كواشف معتادة في المتالورجيا المائية. والحمض هو مادة تتحلل في الماء لإنتاج أيونات الهيدروجين. أما القاعدة فهى مادة تتحلل في المحاليل المائية لتكوين أيونات الهيدروكسيل. وحمضية أو قاعدية المحلول تعرف بمقياس الرقم الهيدروجينى، وهو مقياس يحظى بقبول كبير:
[+pH = - log[H
والرقم الهيدروجينى 7 يعنى أن تركيز أيونات الهيدروجين في المحلول = 10-7 جرام أيون/لتر. والرقم الهيدروجينى ل 0,1 مول HCl أى (3,75 جم/لتر أو 0,44%) يساوى 1، و ل 0,1 مول NaOH أى (4 جم/لتر أو 0,48%) يساوى 13.
المركبات التناسقية
تنتج المركبات التناسقية من آلية المانح والمُتَقَبِّل، فالمانح هو أى ذرة أو أيون لافلزى، سواء أكان حراً أو محتواً في جزىء متعادل أو في مركب أيونى قادر على منح زوج إلكترونات. والمُتَقَبِّل هو غالباً أيون فلزى يقبل المشاركة في زوج الإلكترونات. أما المركبات التناسقية التى تَهُم في المتالورجيا المائية فهى نوعان: المركبات المعقدة والمركبات المخلبية.
المركبات المعقدة
المركبات المعقدة هى مركبات تذوب في الماء أو أيونات ذات خواص كيميائية محددة مقارنة بالأيونات غير المعقدة. فعند إضافة النشادر إلى محلول كبريتات النحاس، وهو أزرق خفيف الزرقة، فإنه يتحول إلى أزرق قاتم بسبب تكون أمين النحاس المعقد:
بدلاً من تكوين هيدروكسيد نحاس غير ذائب. وهكذا يشترك أيون النحاس في زوج إلكترونات ذرة نيتروجين النشادر. والنشادر هى المانح و Cu2+ هو المُتَقَبِّل. وفى هذه الحالة، المانح هو مركب غير مشحون. والمركبات المانحة الحاملة لشحنة سالبة، أى أنيونات، هى مركبات شائعة، وتشمل -CN و F- و Cl- و -SO42 و NO3- و CO32- و OH- و PO43- و S2-.
المركبات المخلبية
المركبات المِخْلَبِيَّة هى مركبات معقدة ذات بنية حلقية، وتحتوى عادة على 5 أو 6 أعضاء، قد تكون ذوابة أو غير ذوابة في الماء. وتعتمد ذوبانية المركبات المخلبية على حجم تجمع الهيدروكربونات. كلما كبر كلما انخفضت الذوبانية في الماء، و وجود مجموعات عالية التميه، مثل المجموعات السلفونية والكربوكسيلية والأمينية والفينولية في النفايات العضوية. و تقوم المركبات المخلبية بدور هام في العديد من العمليات الحياتية، مثل الهيموجلوبين والكلوروفيل وفيتامين "ب12".
حرارة التفاعل
عندما يختلط حمض مثل حمص الكبريتيك مع قاعدة مثل هيدروكسيد الصوديوم، يُلاحظ أن الخليط يصبح ساخناً. فمن أين أتت هذه الحرارة؟ يمتلك أى نظام كمية معينة من الطاقة، تسمى الطاقة الداخلية أو محتوى الطاقة، ويرمز لها بالرمز E، وتتكون من طاقتى الحركة والوضع لكل ذرات النظام. وعند التأثير بكمية حرارة q على نظام طاقته الداخلية E1، فإن الطاقة الداخلية للنظام تزداد إلى E2. عند ضغط ثابت، حرارة التفاعل تساوى مجموع الزيادة في الطاقة الداخلية وشغل التمدد. ويظهر مجموع ΔE + P ΔV كثيراً في حسابات الطاقة ويرمز له بالرمز ΔH، وهو المحتوى الحرارى أو الإنثالبى (أو السَخَانَة)
حرارة التفاعل ΔH تساوى الفرق بين المحتوى الحرارى للنواتج والمتفاعلات في درجة الحرارة المعنية، أى:
ويجب الانتباه لعدد الجزيئات الداخلة في التفاعل. وكما هو متفق عليه، فحرارة التكوين تكون سالبة عند نشوء حرارة أى للتفاعل الطارد للحرارة، وموجبة عند امتصاص الحرارة أى للتفاعل الماص للحرارة.
حرارة التكوين
يُعْرَف التغير في المحتوى الحرارى الذى يحدث عند تكون 1 مول من مركب من عناصره بحرارة التكوين لهذا المركب. وبما أن هذه الكمية تعتمد على الحالة الفزيائية للمواد المشتركة في التفاعل، فإنه يفترض عامة أن العناصر والمركبات تكون في حالاتها القياسية. والحالات القياسية تؤخذ على أنها الصورة المستقرة للمواد عند 25 ْم وواحد ضغط جوى. وعندما تكون كل المواد في حالاتها القياسية،فإن التغير في المحتوى الحرارى يُعْرَف بحرارة التكوين القياسية، ويرمز لها بΔH298. وﻷن قيم المحتوى الحرارى نسبية، فإن قيمة المحتوى الحرارى للعناصر في حالاتها القياسية قد اعتبرت صفراً. ومحصلة التغير الحرارى في تفاعل كيميائى هى نفس القيمة سواء أتم التفاعل في مرحلة واحدة أو عدة مراحل. وهذا القانون هو تطبيق مباشر لمبدأ بقاء الطاقة، ويعرف بقانون هِسْ (1840م). تتغير حرارات التفاعل مع درجة الحرارة لأن المتفاعلات والنواتج لديها سعات مختلفة لامتصاص الحرارة. وبمعرفة قيمة ΔH عند درجة حرارة معينة يُمكن حساب قيمتها عند أى درجة حرارة أخرى باستخدام القاعدة الآتية:
الحسابات النظرية
من التطبيقات المباشرة لقانون هِسْ دورة هابِر-بورن (1919م) لحساب حرارات التكوين نظرياً. فمثلاً حرارة تكوين (جامد)NaCl يمكن حسابها بمعرفة الطاقات الآتية:
• كمية الحرارة اللازمة لتحويل الصوديوم الفلزى إلى بخار (حرارة التسامى، S).
• الطاقة اللازمة لتحويل بخار الصوديوم إلى أيونات غازية موجبة الشحنة (جهد التأين، I).
• الحرارة اللازمة لتحويل الكلور الغازى ثنائى الذرة إلى غاز أحادى الذرة (طاقة الانحلال، D).
• الطاقة اللازمة لتحويل الكلور الغازى أحادى الذرة إلى أيونات غازية سالبة الشحنة (الأُلفة الإلكترونية، e).
• الطاقة اللازمة لإحضار أيون الصوديوم الغازى موجب الشحنة وأيون غازالكلور سالب الشحنة معاً من اللانهاية إلى داخل شبكة بلورية جامدة لتكوين NaCl (طاقة الشبكة البلورية، U).
وبصيغة أخرى:
هذه القيمة المحسوبة نظرياً تنطبق على القيمة التجريبية التى وُجدت للتفاعل. من العواقب الهامة لدورة هابر-بورن إمكانية التنبأ باستقرار مركب كيميائى من خواص العناصر المكونة له.
انظر أيضا
- استخلاص الفلزات
- متالورجيا حرارية
- متالورجيا مائية
- متالورجيا كهربية
- علم الفلزات
- تركيز الخامات
- تحرير المعادن
المراجع
- F. Habashi (2003). Metals from Ores. An Introduction to Extractive Metallurgy,. Québec, Québec City, Canada: Métallurgie Extractive.