أبحاث على الإنفلونزا الإسپانية
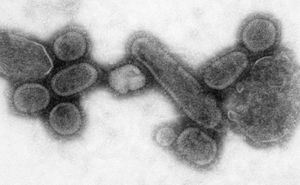
الأبحاث عن إنفلونزا 1918، هي مجموعة أبحاث علمية عن أسباب وخصائص الإنفلونزا الإسپانية التي تفشت في عام 1918، والتي اعتبرت من أشد الأمراض الوبائية فتكا في التاريخ الحديث.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
خلفية
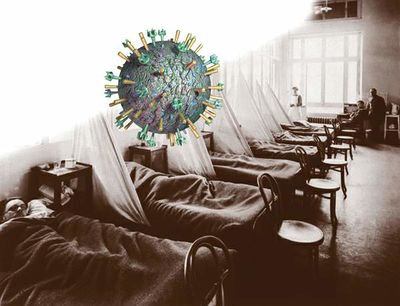
في7/9/1918 وفي ذروة الحرب العالمية الأولى، مرض بالحمى الشديدة أحد الجنود في معسكر تدريب خارج بوسطن. شخَّص الأطباء حالته على أنها التهاب سحايا، إلا أنهم في اليوم التالي غيروا رأيهم في التشخيص بعد أن دخل المشفى 12 جنديا آخر بسبب أعراض تنفسية. وفي السادس عشر من الشهر ذاته ظهرت 36 حالة جديدة من هذا المرض الغامض. ومما لا يصدق أنه بحلول ال23 من الشهر كان قد بلغ عدد الحالات المرضية 604 12 في المعسكر الذي كان يضم 000 45 جندي. وبحلول نهاية الفاشية outbreak كان قد أصيب ثلث عدد قاطني المعسكر بهذا المرض الحاد، وقد مات منهم نحو 800 جندي. غالبا ما كان يظهر لدى الجنود المصابين ازرقاق في الجلد وكانوا يعانون بشدة قبل أن يستسلموا للموت نتيجة للاختناق. مات الكثيرون منهم بعد مرور أقل من 48 ساعة على ظهور الأعراض المرضية، وقد وجد عند تشريح جثثهم أن رئاتهم كانت ممتلئة بسائل أو بدم.
إن هذه المجموعة الغريبة من الأعراض لم تكن تطابق أيا من الأمراض المعروفة. لذا فقد تكهن الخبير الذائع الصيت في علم الأمراضpathologistا <W .H. ويلش> بأنه لا بد أن يكون ما نراه نوعا جديدا من العدوى (الخمج) أو الطاعون. إلا أن هذا المرض لم يكن في الحقيقة طاعونا ولا حتى مرضا جديدا. لم يكن سوى الإنفلونزا. ومع ذلك يُعتقد أن هذه السلالة المُعدية والمُفَوَّعة virulent من ڤيروس الإنفلونزا قد قتلت نحو 40 مليون شخص حول العالم في ما بين عامي 1918 و1919.
| "
نظرة إجمالية/ لغز عام 1918(**) ▪ كانت جائحة الإنفلونزا التي اكتسحت العالم في عاميْ 1918 ـ 1919 استثنائية، وذلك بسبب العدد الكبير الذي تسببت بقتله، وبخاصة عدد اليافعين الذين توفوا بسبب الفوعة غير العادية لڤيروس الإنفلونزا. ▪ كانت الأسباب التي جعلت تلك السلالة فتاكة بذاك الشكل، من الألغاز الطبية المحيرة لمدة طويلة إلى أن تمكن مؤلفو المقالة من ابتداع تقنيات مكنتهم من استرجاع جينات ڤيروس 1918 بدءًا من الأنسجة المحفوظة للضحايا. ▪ كشف تحليل تلك الجينات والپروتينات التي تكودها عن خصائص ڤيروسية ربما مكنتها بنفس الوقت من أن تكبت الاستجابة المناعية لدى الضحايا وأن تحرض تفاعلات مناعية حادة مما أسهم في حدوث النسبة العالية من الوفيات. ▪ من غير المرجح أن تكون العوائل المعروفة لإنفلونزا الطيور والثدييات هي مصدر الڤيروس الجائحي، لذا يبقى منشؤه مجهولا. " |
لقد اختفى تفشي الإنفلونزا الأكثر فتكا في التاريخ الحديث بالسرعة نفسها التي ظهر بها تقريبا، وظن الكثيرون أن مسببها قد ضاع مع الزمن. لم يقم أحد بحفظ عينات من العامل الممرض من أجل دراسات لاحقة، ذلك أنه لم يكن من المعروف آنذاك أن مسبب الإنفلونزا قد شُخِّص كڤيروس حتى عام 1930. إلا أنه بفضل نفاذ البصيرة الهائل لرجال المتحف الطبي التابع للجيش الأمريكي، والمثابرة الحثيثة لمتخصص في علم الأمراض يدعى <J. هالتن>، والتقدم الحاصل في التحليل الجيني لعينات النسج القديمة، استطعنا استعادة أجزاء من ڤيروس 1918 ودراسة خصائصه. والآن بعد مرور أكثر من 80 عاما على تلك الكارثة الطبيعية المروعة عاميْ 1918-1919، تقوم النسج المستعادة من بعض الضحايا بالإجابة عن التساؤلات الأساسية المتعلقة بطبيعة تلك السلالة الجائحية pandemic وبطريقة عمل ڤيروسات الإنفلونزا بشكل عام.
لم يكن الفضول التاريخي هو الدافع الوحيد للجهود المبذولة. ولما كانت ڤيروسات الإنفلونزا تتطور باستمرار، فإن سلالات جديدة منها تواصل تهديدها للمجتمعات البشرية. لقد ظهرت جائحاتُ ڤيروسات الإنفلونزا البشرية مرتين منذ عام 1918 وذلك في عامي 1957 و 1968. كما أن سلالات الإنفلونزا التي كانت في العادة تصيب الحيوانات فقط، أصبحت تصيب البشر أيضا على غرار ما شوهد أخيرا عندما انتشرت سلالة إنفلونزا الطيور في آسيا. كان الهدفان الأساسيان لنا هما تحديد السبب الذي جعل إنفلونزا 1918 شديدة الفوعة بهدف تطوير العلاجات المتعلقة بها والمعايير اللازمة للوقاية منها، ومعرفة منشأ الڤيروس الجائحي بحيث يمكن استهداف المصادر المحتملة للسلالات التي قد تسبب جائحات في المستقبل.
البحث عن ڤيروس 1918
كانت جائحة الإنفلونزا عام 1918 مماثلة في الكثير من النواحي لغيرها من الجائحات السابقة واللاحقة لها. وفي كل مرة تظهر سلالة لإنفلونزا جديدة تمتلك خصائص جديدة لم يسبق للجهاز المناعي لمعظم البشر تعرُّفها، يكون من المرجح عندئذ حدوث تفشٍّ واسع للإنفلونزا. إلا أن هناك خصائص تنفرد بها جائحة عام 1918 بقيت لغزًا محيرًا حتى الآن.
كانت تلك الجائحة، على سبيل المثال، استثنائية من حيث الاتساع والعمق، فقد اجتاح الوباء أوروبا وأمريكا الشمالية ووصل إلى قفار ألاسكا وإلى الجزر السحيقة في المحيط الهادئ. وفي نهاية الأمر ربما أصيب ثلث عدد سكان العالم بالمرض. كما أن المرض كان شديدا بصورة غير عادية، حيث كان معدل الوفيات يراوح ما بين 2.5 و 5%، وهي نسبة تزيد 50 ضعفا على المعدلات المشاهدة في فاشيات الإنفلونزا الأخرى.
بحلول خريف 1918 كان الجميع في أوروبا يدعون المرض باسم الإنفلونزا الإسبانية، ومن المحتمل أن ذلك يعود إلى أن إسبانيا المحايدة لم تفرض الرقابة التي فرضت أيام الحرب على الأخبار المتعلقة بالجائحة في البلاد المتقاتلة. وقد بقيت تلك التسمية دارجة على الرغم من أن الانتشار الأول ـ أو الموجة الربيعية ـ للجائحة نشأ بدايةً حول معسكرات الجيش الأمريكي في الشهر3/1918. وامتدت الموجة الرئيسية الثانية للجائحة العالمية من الشهر 9 إلى الشهر11/1918، كما حدثت في مطلع عام 1919 موجة أخرى حادة من الإنفلونزا في أمكنة كثيرة.
لم تكن المضادات الحيوية قد اكتشفت بعد، وكان معظم الذين ماتوا أثناء الجائحة قد سقطوا صرعى ذات الرئة (الالتهاب الرئوي) pnemonia نتجت من بكتيرات انتهازية أصابتهم بعد أن أضعفتهم الإنفلونزا. إلا أن مجموعة من ضحايا الإنفلونزا ماتوا بعد أيام قليلة من ظهور الأعراض لديهم، وذلك بسبب حدوث التهاب رئوي ڤيروسي أكثر حدة ـ نتج من الإنفلونزا ذاتها ـ جعل الرئة لديهم إما نازفة بشدة أو ممتلئة بالسوائل. إضافة إلى ذلك فقد حدثت معظم الوفيات لدى البالغين الفتيّين الذين تراوح أعمارهم بين 15 و 35 سنة، وهي مجموعة نادرا ما تموت بسبب الإنفلونزا. كان من المذهل أن يشكل الأفراد الذين تقل أعمارهم عن 65 عاما أكثر من 99% من وفيات الإنفلونزا «الإضافية» excess (أي هؤلاء الذين يتجاوزون معدل الوفيات السنوية الطبيعية) في عامي 1918 و 1919.
بدأت الجهود الحثيثة لمحاولة فهم سبب جائحة 1918 وخصائصها الغريبة بمجرد انتهائها، ومع ذلك بقي الڤيروس المتهم دفينا نحو ثمانية عقود. وفي عام 1951 قام علماء من جامعة أيوا، كان منهم طالب دراسات عليا جاء مؤخرا من السويد ويدعى <J. هالتن>، بالوصول حتى شبه جزيرة سيوارد الواقعة في ألاسكا وذلك بحثا عن سلالة 1918 [انظر الإطار في الصفحة 22]. في الشهر11/1918 انتشرت الإنفلونزا في قرية لصيد الأسماك يقطنها الإسكيمو، وتدعى الآن بريڤگ ميشن Brevig Mission، وذلك خلال خمسة أيام مما أدى إلى قتل 72 شخصا، أي نحو 85 في المئة من تعداد البالغين فيها. لقد دفنت جثثهم منذ آنذاك في الجليد السرمدي permafrost، وقد أمّل أفراد بعثة 1951 أن يجدوا ڤيروس 1918 محفوظا في رئات هؤلاء الضحايا. إلا أنه لسوء الحظ باءت بالفشل جميع الجهود المبذولة لعزل واستزراع ڤيروس الإنفلونزا الحي المأخوذ من تلك العينات.
وفي عام 1995 قامت مجموعتنا بمحاولة للعثور على ڤيروس 1918 باستخدام مصدر مختلف للأنسجة، هي عينات من الخزعات المؤرشفة والمحفوظة في مركز الباثولوجيا (الأمراض) التابع للقوات المسلحة Armed Forces Institute of Pathology (AFIP )ـ وقد كنا لعدة سنوات نطور خبرتنا فيما يتعلق باستخلاص عناصر جينية ڤيروسية هشة من أنسجة تالفة أو متحللة وذلك لأهداف تشخيصية. استطعنا عام 1994 على سبيل المثال استخدام طرق حديثة لمساعدة أحد خبراء أمراض الثدييات البحرية من المركز AFIP في تقصي موت عدد كبير من الدلافين حيث كان يلقى باللوم في ذلك على المد الأحمر red tide. وعلى الرغم من أن العينات النسيجية المتوافرة للدلافين كانت تالفة بشدة فقد تمكّنّا من استخلاص قطع كافية من الرنا RNA منها قادتنا إلى تعرّف ڤيروس جديد مشابه للڤيروس المسبب لمرض حمى الكلاب(1)، الذي كان السبب الحقيقي وراء موت الدلافين. وفي الحال بدأنا بالتساؤل: أباستطاعتنا ـ اعتمادا على قدرات معهدنا العلمي وإمكاناته ـ حل ألغاز أخرى في أمور طبية غامضة تنتمي إلى الماضي؟
لقد تطور المركز AFIP ـ الذي هو سليف المتحف الطبي التابع للجيش الأمريكي الذي أنشئ عام 1862، مع تطور اختصاص علم الأمراض(الپاثولوجيا)، وفي المركز حاليا مجموعة تضم أكثر من 3 ملايين عينة. وعندما عرفنا أن هذه العينات تتضمن عينات مأخوذة من خزعات لضحايا إنفلونزا 1918، قررنا فورا ملاحقة ڤيروس الجائحة. شملت دراستنا البدئية فحص 78 عينة نسيجية مأخوذة من ضحايا الموجة الخريفية القاتلة عام 1918، مع التركيز على تلك التي تمثل تخربا رئويا حادا والتي كانت من خصائص المرضى الذين ماتوا بسرعة. ولما كان ڤيروس الإنفلونزا عادة ما يغادر الرئة بعد الإصابة بأيام قليلة فقط، لذا كانت فرصتنا الكبرى تكمن في العثور على بقايا الڤيروس في هؤلاء الضحايا.
كانت الممارسة الاعتيادية القائمة في تلك الحقبة تعتمد على حفظ عينات الخزعات في الفورمالدهيد ثم طمرها في البارافين، لذا فقد اقتضى اصطياد الأجزاء الجينية الصغيرة جدا للڤيروس من تلك العينات «المثبتة» fixed التي حفظت نحو 80 عاما، تطبيقَ أقصى حدود للتقنيات التي كنا قد طورناها. وبعد عام كامل من النضال والحصول على نتائج سلبية حصلنا عام 1996 على أول عينة إيجابية للإنفلونزا، وذلك من خزعة رئوية لجندي مات في الشهر 9/1918 في فورت جاكسون بولاية كارولينا الجنوبية. وقد استطعنا تحديد تسلسل النيوكليوتيدات في شدف صغيرة من خَمس من جينات الإنفلونزا التي عزلت من تلك العينة.
لكننا استمررنا بالبحث عن حالات إيجابية أخرى بغية إثبات أن تلك التسلسلات تنتمي إلى الڤيروس القاتل عام 1918. وقد عثرنا على حالة إيجابية أخرى عام 1997. وقد مات ذلك الجندي أيضا في الشهر9/ 1918 في كامپ آمْپتُن بولاية نيويورك. لقد سمح لنا الحصول على عينة أخرى بتأكيد التسلسلات الجينية لدينا، إلا أن الكميةالصغيرة جدا المتبقية من النسج جعلتنا قلقين من حيث إمكانية إتمام تسلسل الحمض النووي الڤيروسي بكامله.
في عام 1997 جاء الحل لمشكلتنا من مصدر غير متوقع وذلك من قبل <J. هالتن> أخصائي علم الباثولوجيا المتقاعد والبالغ من العمر آنذاك 73 عاما. كان قد قرأ عن نتائجنا المبدئية وعرض أن يعود إلى بريڤگ ميشن في محاولة جديدة لإخراج جثث ضحايا إنفلونزا 1918 المدفونة في الجليد السرمدي هناك. وبعد مرور 46 عاما على محاولته الأولى وبعد الحصول على الموافقة من مجلس قرية بريڤگ ميشن، استطاع الحصول على خزعات رئوية مجمدة لأربع من ضحايا الإنفلونزا. وقد حصلنا من واحدة من تلك العينات، تعود إلى امرأة مجهولة السن، على رنا ڤيروس الإنفلونزا، وكان ذلك مفتاحا لسَلْسَلة الجينوم (المجين) الكامل لڤيروس 1918. وبعد عام كامل مُضْنٍ من الحصول على النتائج السلبية،
تم العثور الحالة الأولى في عام 1996
حديثا قامت مجموعتنا، بالتعاون مع زملاء من بريطانيا، بمسح عينات نسيجية مأخوذة من ضحايا إنفلونزا 1918 وذلك في مستشفى لندن الملكي Royal London Hospital. وتمكنا من تحليل جينات ڤيروس الإنفلونزا المعزول من حالتين من تلك الحالات ووجدناها مطابقة تقريبا للعينات التي أُخذت من أمريكا الشمالية، مما يؤكد الانتشار الواسع والسريع على مستوى العالم لڤيروس متماثل. ولكن ما الذي تستطيع أن تقدمه لنا هذه التسلسلات النووية من معرفة حول فوعة سلالة ڤيروس عام 1918 أو منشأ تلك السلالة؟ تتطلب الإجابة عن تلك الأسئلة بعض المعلومات الأساسية حول طريقة عمل ڤيروسات الإنفلونزا وكيف تسببت بالمرض لدى العوائل المختلفة للڤيروس.
الإنفلونزا تغير وجهها
إن سلالات الإنفلونزا الثلاث الحديثة التي سببت جائحات خلال المئة عام الماضية تنتمي إلى ڤيروسات الإنفلونزا من النمط A. فالإنفلونزا تصنف في ثلاثة أنماط رئيسية A، B، C. يصيب الشكلان الأخيران منها( B و C )الإنسان فقط ولم يُحدِثا أي جائحة قط، في حين يصيب ڤيروس الإنفلونزا من النمط A مجموعة كبيرة من الحيوانات بما فيها الدجاج والخنازير والجياد والبشر والثدييات الأخرى. وتمثل الطيور المائية، مثل البط، المستودع الطبيعي natural reservoir لجميع الأنماط الفرعية المعروفة للإنفلونزا من النمط A. وهذا يعني أن الڤيروس يصيب أحشاء الطير دون أن يتسبب بحدوث أية أعراض. لكن يمكن لهذه السلالات التي تتطفل على الطيور أن تَطْفُر مع مرور الزمن، أو يمكن لها أن تتبادل بعض المواد الجينية مع سلالات أخرى للإنفلونزا، مؤدية إلى إنتاج ڤيروسات جديدة قادرة على الانتشار بين الثدييات والطيور الداجنة.
إن دورة حياة ڤيروس الإنفلونزا A وكذلك بنية جينومه (مجينه) تسمحان له بالتطور وبتبادل الجينات بسهولة. وتتألف المادة الجينية للڤيروس من ثماني قطع منفصلة من الرنا معبأة داخل غشاء دهني مرصع بالپروتينات [انظر الشكل العلوي في الصفحة 18]. ولكي يتكاثر الڤيروس، يجب عليه الارتباط أولا بسطح خلية حية ومن ثم دخوله إليها، حيث يقوم بالسيطرة على آليات خلوية محرضا إياها على إنتاج پروتينات ڤيروسية جديدة ونسخ إضافية من الرنا الڤيروسي. تجتمع تلك القطع معا لتشكل ڤيروسات جديدة تغادر خلية العائل لتعدي خلايا أخرى. لا توجد آلية مدققة تضمن أن نُسخَ الرنا الڤيروسي الجديدة دقيقة وصحيحة، لذا تشيع الأخطاء التي تؤدي إلى حدوث طفرات جديدة. إضافة إلى ذلك، فإنه إن حدث وأصابت سلالتان مختلفتان من الإنفلونزا الخلية ذاتها يمكن عندئذ لقطع الرنا أن تمتزج بحرية هناك منتجة ذرية من الڤيروسات تحتوي على مجموعة من الجينات من كلتا السلالتين من الڤيروسات الأصلية. تعتبر هذه العملية من إعادة التنسيق reassortment للجينات الڤيروسية آلية مهمة لتوليد سلالات جديدة ومتنوعة.
يتم تعريف الأنواع المختلفة لڤيروسات الإنفلونزا من النمط A المنتشرة بالرجوع إلى پروتينين واسمين على سطوحها. أحدهما هو الهيماگلوتينين Hemagglutinin HA الذي يمتلك أكثر من 15 ضربا مغايرا variant معروفا (أي نمطا فرعيا). أما الآخر فهو النيورامينيداز neuraminidase NA ، الذي يمتلك تسعة أنماط فرعية. ينتج العائل الذي يتعرض إلى هذه الپروتينات أضدادا مميزة. لذا كانت سلالة 1918 هي الأولى التي سميت H1N1 نظرا للأضداد التي وجدت في دماء أولئك الذين نجوا من الجائحة. وبالطبع كانت الأنسال المنحدرة من السلالة H1N1 والأقل فوعة هي سلالات الإنفلونزا السائدة حتى عام 1957، حينما ظهر ڤيروس H2N2 بصورة جائحية. ومنذ عام 1968 كان النمط الفرعي H3N2 الذي سبب حدوث الجائحة في ذلك العام هو السائد حتى الآن.
إن النمطين الفرعيين HA وNA الموجودين على سطح ڤيروس إنفلونزا من النمط A لا يستخدمان فقط في تعرف هذا الڤيروس، بل هما ضروريان جدا لتكاثر الڤيروس؛ كما أنهما يعتبران الأهداف الابتدائية لاستثارة الجهاز المناعي الخاص بالعائل المصاب بهذا الڤيروس، حيث يبدأ جزيء الپروتين HA بإحداث العدوى بارتباطه بمستقبلات على السطح الخارجي لخلايا معينة من خلايا العائل المصاب، وهذه غالبا ما تكون الخلايا المبطنة للجهاز التنفسي في الثدييات، وكذلك الخلايا المبطنة للأمعاء في الطيور. ويمكِّن الپروتين NA النسخ الجديدة للڤيروس من مغادرة خلية العائل لتسبب الإصابة في خلايا أخرى مجاورة.
بعد تعرض العائل للمرة الأولى لنمط فرعي من الپروتين HA، تقوم الأضداد بحجب ارتباطه بالمستقبلات الخلوية أثناء التعرض التالي، وهي من ثمّ تكون فعّالة جدا في منع تكرار الإصابة بالسلالة نفسها. لكن، تظهر من حين إلى آخر ڤيروسات إنفلونزا ذات أنماط فرعية HA جديدة بالنسبة إلى البشر، وغالبا ما يعود ذلك إلى إعادة تنسيقها ضمن الجميعة الواسعة extensive pool لڤيروسات الإنفلونزا التي تصيب الطيور البرية. وفي العادة ترتبط ڤيروسات HA المهيأة لإصابة الطيور ارتباطا ضعيفا بالمستقبلات الخلوية المنتشرة على المجرى التنفسي في البشر. لذا لا بد للڤيروس أن يعدل بدرجة ما من نزعته إلى الارتباط بهذه المستقبلات في الطيور قبل أن يتمكن من التضاعف والانتشار بشكل فعال في البشر. وإلى عهد قريب، كانت الدلائل المتوافرة تشير إلى أن ڤيروسا يسبب الإنفلونزا حصريا في الطيور ربما لا يمكنه إعداء (خمج) الإنسان بشكل مباشر. ومع ذلك فقد أصيب 18 شخصا بڤيروس إنفلونزا الطيور H5N1 في هونغ كونغ عام 1997 ومات ستة منهم.
حدث تفشٍّ لشكل أشد إمراضا من السلالة H5N1 وانتشر بشكل واسع في الدواجن الآسيوية في عامي 2003 و 2004، وقد مات أكثر من 30 شخصا ممن أصيبوا بهذا الڤيروس في ڤيتنام وتايلاند.
حينما يصيب ڤيروس الإنفلونزا عائله، فإن فوعته تعتمد على مجموعة معقدة من العوامل، التي تتضمن مدى سهولة دخول الڤيروس إلى النسج المختلفة، ومدى سرعة تضاعفه وعنف استجابة العائل المناعية للعامل الدخيل. لذا فإن الفهم الدقيق للأسباب التي جعلت سلالة الإنفلونزا الجائحية في عام 1918 بتلك الشدة من الفوعة والقدرة على العدوى (الإخماج) يمكن أن يقود إلى بصيرة أعمق حول الأسباب التي تجعل أي سلالة من سلالات الإنفلونزا عاملا أكثر أو أقل تهديدا.
تسيطر الإنفلونزا على العائل لتتضاعف وتتطور
الإنفلونزا ڤيروس صغير وبسيط ـ مجرد كرة شحمية مجوفة مرصعة ببعض الپروتينات وتحمل ثمانية أجزاء جينية فقط (الشكل أدناه). إلا أن ذلك يمثل كل ما يحتاج إليه الڤيروس من أجل تحريض خلايا العائل الحي على عمل ڤيروسات جديدة (في الأسفل). يتمتع أحد الپروتينات الموجودة على سطح الإنفلونزا بأهمية خاصة وهو الهيماگلوتينين HA، إذ يسمح للڤيروس بدخول الخلايا. ويحدد شكل هذا الپروتين العائلَ النوعي الذي يمكن إصابته من قبل سلالة الڤيروس. ويقوم پروتين آخر هو النورامينيداز NA بقص الڤيروسات الجديدة المتشكلة محررا إياها من الخلية المصابة، مؤثرا بذلك في مدى كفاءة انتشار الڤيروس. إن حدوث تبدلات وإن كانت طفيفة في هذه الپروتينات وغيرها من پروتينات الإنفلونزا يمكن أن يساعد الڤيروس على إصابة أنواع جديدة من العوائل والتملص من الهجوم المناعي. ويمكن للتبدلات أن تنشأ نتيجة لحدوث أخطاء أثناء نسخ الجينات الڤيروسية، أو يمكن أن تكتسب بالمقايضة عندما تختلط الجينات الخاصة بنوعين مختلفين من ڤيروسات الإنفلونزا يكونان قد أصابا الخلية نفسها (في اليسار).
يبرز الپروتينان السطحيان الأساسيان HA وNA من طبقة شحمية مزدوجة. ويوجد بالداخل ثمانية أجزاء منفصلة من الرنا الڤيروسي تقوم بتكويد الپروتينات الأخرى التي تحدد جميع الخصائص المتعلقة بوظيفة الڤيروس.
الإصابة والتضاعف
يرتبط پروتين HA الخاص بڤيروس الإنفلونزا بحمض السياليك الموجود على سطح خلية العائل (a) مما يسمح للڤيروس بالانزلاق إلى الداخل (b) حيث يحرر الرنا الخاص به (c) والذي يدخل إلى نواة الخلية (d) وهناك يتم نسخ الرنا الڤيروسي و«قراءة» تعليماته الوراثية، مما يحث الآلية الخلوية على إنتاج پروتينات ڤيروسية جديدة (e). بعد ذلك يتجمع الرنا والپروتينات الڤيروسية الجديدة لتشكيل ڤيروسات تتبرعم خارجة من الغلاف الخلوي (f). يكون سطح الڤيروسات مغطى بالبداية بحمض السياليك. ولمنع الڤيروسات من الارتباط بعضها ببعض عبر پروتينات الهيماگلوتينين أو بسطح خلايا العائل، يقوم النورامينيداز بقص حمض السياليك (g)، مما يحرر الڤيروسات لتصيب خلايا أخرى.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
إعادة التنسيق
يمكن أن تنشأ سلالات جديدة من الإنفلونزا عندما تصاب الخلية نفسها بنوعين مختلفين من الڤيروسات (في الأعلى)، فيمكن لنسخ الرنا الخاص بكل منهما أن تختلط مؤدية إلى إنتاج أنسال تمتلك مجموعة من الجينات تعود لكلا الأبوين. بهذه الطريقة يمكن لسلالة إنفلونزا خاصة بالطيور أو الحيوان أن تكتسب جينات تعطيها القدرة على الانتشار بسهولة أكبر بين البشر.
وجه قاتل
بفضل استعادتنا رنا ڤيروس عام 1918 تمكنا من استخدام جينات الڤيروس ذاتها لتصنيع الأجزاء المكونة له ـ أي إعادة تخليق أجزاء ذلك الڤيروس القاتل. كان پروتين الهيماگلوتينين هو أول المكونات التي كنا نتلهف على دراستها، وذلك بحثا عن خصائص محددة يمكنها أن تفسر الفوعة الاستثنائية لسلالة عام 1918
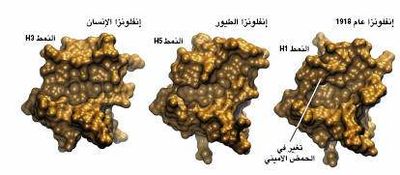
بارتباط الهيماگلوتينين الطيري بمستقبلات خلايا الثدييات
وقد رأينا على سبيل المثال أن جزء الپروتين HA من ڤيروس عام 1918 الذي يرتبط بخلايا العائل المصاب، يماثل تقريبا موضع الارتباط الخاص بالپروتين HA الذي يعود لڤيروس يصيب الطيور حصريا [انظر الشكل في أسفل هذه الصفحة]. كان موقع ارتباط المستقبلات الخلوية يختلف في اثنتين من عزلات(1) عام 1918 عن ما هي الحال في الشكل الطيري بحمض أميني واحد فقط كوحدة بنائية لپروتين الڤيروس. وفي العزلات الثلاث الأخرى حدث تبدل في حمض أميني آخر. قد تمثل هذه الطفرات التي تبدو طفيفة، الحد الأدنى من التبدل اللازم للسماح للپروتين HA من النمط الطيري بالارتباط بالمستقبلات الخاصة في الثدييات
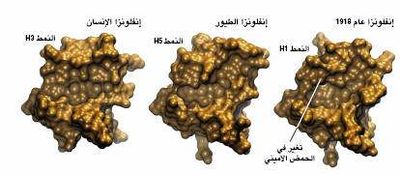
لكن في حين أن اكتساب قدرة ارتباط جديدة هو خطوة حاسمة وأساسية للسماح للڤيروس بأن يصيب نمطا جديدا من العوائل، إلا أنه لا يفسر بالضرورة لماذا كانت سلالة عام 1918 مميتة بهذا الشكل. وجَّهنا اهتمامنا إلى تسلسلات الجينات بالذات باحثين عن خصائص قد تكون مرتبطة بشكل مباشر بحدة المرض، منها طفرتان كانتا معروفتين في ڤيروسات إنفلونزا أخرى، تكمن إحداهما في الجينة الخاصة بالپروتين HA. فلكي يكون الپروتين HA فعالا في الخلية يجب أن يُشْطر إلى قطعتين بوساطة إنزيم نوعي قاطع للپروتين (پروتياز) يوجد في أمعاء العائل. إن بعض الأنماط الفرعية H4 و H7 من ڤيروسات الطيور تكتسب طفرة جينية تتمثل بإضافة حمض أميني أساسي واحد أو أكثر في موضع الشطر مما يسمح بتفعيل الپروتين HA عن طريق إنزيمات الپروتياز الموجودة بكثرة. تؤدي إصابة الدجاج وغيرها منالطيور بمثل ذلك الڤيروس إلى حدوث المرض في أعضاء متعددة فيها، بل إنها تصيب الجهاز العصبي المركزي، وتؤدي إلى حدوث معدل مرتفع جدا من الوفيات. لقد شوهدت هذه الطفرات في ڤيروسات H5N1المنتشرة حاليا في آسيا. لكننا مع ذلك لم نجدها في ڤيروس عام 1918.
شوهدت الطفرة الأخرى ذات التأثير المهم في الفوعة في جينة NA لسلالتين من ڤيروسات الإنفلونزا التي تصيب الفئران. مرة أخرى، فإن حدوث الطفرات في حمض أميني واحد، يسمح للڤيروس بالتضاعف في العديد من نسج الجسم المختلفة، وكانت هذه السلالات عادة مميتة لفئران التجربة. إلا أننا، هنا أيضا، لم نجد هذه الطفرة في جينة NA من ڤيروس عام 1918.
بما أن تحليل جينات ڤيروس 1918 لم تكشف عن خصائص تفسر فوعته الشديدة، لذا بدأنا، بالتعاون مع العديد من المراكز الأخرى، جهودا متضافرة بغية إعادة تخليق أجزاء من ڤيروس 1918 ذاته بهدف دراسة تأثيره في النسج الحية.
هندسة عكسية لڤيروس الإنفلونزا
عندما لم تكشف تحليلات جينات ڤيروس 1918 عن أسباب محددة لفوعة سلالة تلك الجائحة، اتجهت مجموعتنا إلى اتباع أساليب الوراثيات العكسية reverse genetics وهي طريقة تهدف إلى فهم وظيفة الجينات عن طريق دراسة الپروتينات المكودة من قبلها. وقد قمنا بالتعاون مع كل من كلية الطب في ماونت سيناي، ومراكز ضبط الأوبئة والوقاية منها، ووزارة الزراعة الأمريكية، وجامعة واشنطن، ومركز الأبحاث سكريپس Scripps، ب«بناء» ڤيروسات إنفلونزا تحتوي على واحد أو أكثر من جينات ڤيروس 1918 بغية متابعة كيفية عمل هذه الڤيروسات المأشوبة في الحيوانات والمزارع الخلوية للبشر.
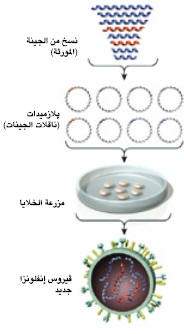
لإنشاء مثل تلك الڤيروسات طبقنا تقنية جديدة تدعى الوراثيات العكسية المعتمدة على الپلازميدات plasmid-based reverse genetics، وهي تتطلب بدايًة عمل نسخ دَنَوِيّة من جينات الإنفلونزا التي توجد عادة في صورة رنا؛ ثم تقحم كل نسخة دَنَوِيّة ضمن حلقة صغيرة من الدنا تدعى الپلازميد. تُحقن الپلازميدات في الخلايا الحية، حيث تقوم الآلية الخلوية بتنفيذ التعليمات الجينية التي تحملها وتصنع بذلك ڤيروسات إنفلونزا تحمل فقط المجموعة المطلوبة من الجينات.
إن الوراثيات العكسية لن تسمح لنا بدراسة ڤيروس 1918 وحسب، بل إنها ستسمح أيضا للعلماء في الولايات المتحدة وأوروبا بتقصي مدى التهديد الذي يشكله ڤيروس إنفلونزا الطيور H5N1 للبشر. فمنذ الشهر1/2004 أصابت تلك السلالة ـ التي توجد حاليا في 10 بلاد آسيوية ـ أكثر من 40 شخصا مؤدية إلى موت 30 منهم. كانت إحدى الضحايا أُمًّا يعتقد أنها تلقت الڤيروس من ابنتها وليس بشكل مباشر من الطيور. إن هذا النوع من الانتقال من شخص إلى آخر يوحي بأنه في تلك الحالة قد حدث تكيف في الڤيروس الطيري بحيث أصبح أسهل انتشارا بين البشر وذلك إما بالتطفر أو باكتساب جينات جديدة عن طريق إعادة ترتيب جيناته مع جينات سلالة ڤيروس إنفلونزا بشري منتشر. إن حدوث مثل ذلك التطور المخيف سوف يزيد من إمكانية حدوث جائحة بشرية. ويقوم العلماء في المراكز CDC وجامعة إيرازموس في هولندا، بغية التنبؤ بمثل تلك الكارثة ومنع حدوثها، بالتخطيط لدراسة مجموعة من التوافيق combinations تضم الڤيروس الطيري H5N1 مع سلالات إنفلونزا بشرية حالية، بهدف تقييم إمكانية وجودها بشكل طبيعي في البشر، إضافة إلى شدة فوعتها.
إن ما ستكشفه هذه التجارب، كما هي الحال في عمل مجموعتنا المتعلق بجينات ڤيروس 1918، سوف يكون أساسيا لفهم كيفية تشكل جائحات الإنفلونزا وأسباب إحداثها للمرض. ويتساءل بعض المراقبين عن مدى أمان إجراء التجارب بسلالات الإنفلونزا القاتلة، إلا أن جميع هذه الأبحاث تجرى في مختبرات مؤمَّنة صممت خصيصا للتعامل مع ڤيروسات الإنفلونزا الممرضة والشديدة الخطورة.
إضافة إلى ذلك، إن إعادة خلق پروتينات سلالة 1918 قد مكنتنا من التحقق من أن الأدوية المضادة للڤيروسات والمتوافرة حاليا مثل أمانتادين amantadine، وكذلك الأحدث منها مثل مثبطات النورامينيداز مثل أوسيلتاميڤير (Tamiflu) oseltamivir سوف تكون فعالة ضد سلالة 1918 في حال حدوث إصابة عرضية. إن ڤيروسات H5N1 هي أيضا حساسة لمثبطات النورامينيداز.
قام العلماء في أمريكا والمملكة المتحدة مؤخرا بتطبيق تقنية الوراثيات العكسية المعتمدة على الپلازميدات لخلق بذور سلالة جديدة بهدف تحضير لقاح بشري ضد H5N1. لقد صنعوا شبيها لڤيروس H5N1 يختلف عنه في أنه يفتقر إلى الخصائص الفتاكة للسلالة بحيث يستطيع المصنعون استخدامه بشكل آمن لإنتاج اللقاح(2). وقد برمجت التجارب السريرية على لقاح H5N1 لتبدأ في نهاية عام 2004.
يمكننا باستخدام تقنية جديدة تدعى الوراثيات العكسية باستخدام الپلازميدات plasmid-based reverse genetics، تسمح لنا بنسخ جينات ڤيروس 1918 ومن ثم ضمها إلى جينات ڤيروسية لسلالة إنفلونزا معروفة لدينا لنحصل على ڤيروس هجين. وهكذا نستطيع أن نستخدم سلالة إنفلونزا مهيأة لإصابة الفئران على سبيل المثال، ثم نضمها إلى جينات ڤيروسية مختلفة لسلالة 1918، وبعد ذلك نعرّض حيوانًا حيًا أو مزرعة نسج بشرية للعدوى بهذا الڤيروس المهندس وراثيا حتى يمكننا معرفة أي المكونات الڤيروسية من السلالة الجائحية هي المسؤولة عن إحداث العدوى.
إن قدرة ڤيروس 1918 المميزة على إحداث تخريب سريع وشامل لكل من النسج التنفسية العلوية والسفلية، على سبيل المثال، تشير إلى أن الڤيروس تضاعف بأعداد كبيرة وانتشر بسرعة من خلية إلى أخرى. من المعروف أن الپروتين الڤيروسي NS1 يمنع إنتاج الإنترفيرون من النمط الأول (IFN) الذي هو نظام إنذار مبكر تستخدمه الخلايا لاستثارة رد الفعل المناعي لديها في مواجهة إصابة ڤيروسية. ولدى اختبارنا للڤيروسات المأشوبة recombinant viruses في مزرعة نسيجية للخلايا الرئوية البشرية وجدنا أن الڤيروس الذي كان يمتلك الجينة NS1 1918 كان حقا أكثر فاعلية في إحصار منظومة إنتاج الإنترفيرون من النمط الأول لدى العائل المصاب.
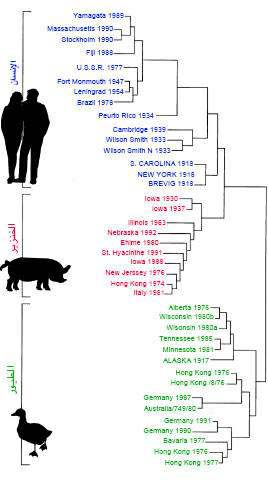
شجرة عائلة الإنفلونزا
بحثًا عن أدلة حول منشأ الهيماگلوتينين HA لڤيروس 1918، قام المؤلفون بتحليل تسلسلات جينية من النمط الفرعي H1 ضمن مجموعة متنوعة من سلالات الإنفلونزا التطورية. وقاموا بإنشاء خريطة نشوء السلالة phylogeny التي تبين علاقاتها. وقعت عينات سلالة 1918 (S. Carolina, New York, Brevig) ضمن عائلة ڤيروسات الإنفلونزا الخاصة بالبشر. إن ابتعاد جينة H1 لسلالة 1918 عن عائلة السلالة الطيرية (الخاصة بالطيور) المعروفة، يمكن أن يشير إلى أنها ربما نشأت في سلالة إنفلونزا طيرية، ثم أمضت بعض الوقت من التطور في عائل مجهول إلى أن ظهرت عام 1918. ومما يدعم هذا الاستنتاج، أنه وُجِدت سلالة طيرية معاصرة في أوزة برانت محفوظة (ألاسكا 1917) وكانت هذه السلالة متباعدة من حيث النشوء عن سلالة 1918 وأكثر تشابها مع الإنفلونزا الطيرية الحديثة.
وإلى الآن، تمكَّنا من إنتاج ڤيروسات إنفلونزا مأشوبة تضمنت واحدةً إلى خمس من جينات 1918، ومن المثير أننا وجدنا أن أيا من الڤيروسات المأشوبة التي كانت تحتوي على جينات HA و NA لڤيروس 1918 قتلت الفئران وسببت تلفا رئويا شديدا مشابها لما شوهد في بعض ضحايا الجائحة. ولدى تحليلنا هذه الأنسجة الرئوية وجدنا بصمات للتفعيل الجيني المشاهد في الاستجابات الاعتيادية لمواجهة الالتهاب. إلا أننا وجدنا أيضا تفعيلا أعلى من الطبيعي للجينات الخاصة بالعناصر الدفاعية للمنظومة المناعية، أي الخلايا التائية T cells والبالعات macrophages وكذلك للجينات التي لها علاقة بالأذيات النسيجية والتخرب التأكسدي والتموُّت الخلوي المبرمج أو الانتحار الخلوي.
قام <Y. كاواوكا> [من جامعة ويسكونسن ـ ماديسون] حديثا بتجارب مماثلة على جينات الإنفلونزا 1918 في الفئران وحصل على نتائج مماثلة. لكنه عندما اختبر جينات HA و NA كلا على حدة وجد أن جينات HA 1918 وحدها كانت قادرة على إحداث الاستجابة المناعية الحادة، مما يشير إلى أن هذا الپروتين، ولأسباب غير واضحة حتى الآن، ربما أسهم بدور أساسي في فوعة السلالة 1918.
إن هذه التجارب التي تجرى حاليا هي بمثابة نافذة على الماضي، تساعد العلماء على فهم الخصائص غير العادية لجائحة 1918. وبالمثل، ستستعمل هذه التقنيات لدراسة أنماط التغيرات التي يمكن أن تطرأ على سلالة إنفلونزا الطيور الحالية H5N1 والتي قد تعطي هذا الڤيروس الفتاك القدرة على إحداث الجائحات في البشر [انظر الإطار في الصفحة المقابلة]. أما السؤال الآخر الذي يطرح نفسه بذات القوة فهو كيفية نشوء مثل تلك السلالات الشديدة الفوعة أصلا. لذا تقوم مجموعتنا أيضا بتحليل جينات ڤيروس 1918 من أجل حل لغز نشأتها ومصدرها.
البحث عن المصدر
يعتبر علم تطور السلالات phylogenetics السبيل الأفضل لتحليل العلاقات ما بين ڤيروسات الإنفلونزا، حيث يتم إنشاء شجرات عائلات افتراضية باستخدام تسلسلات الجينات الڤيروسية مع معرفة مدى التواتر النموذجي لحدوث الطفرات. وحيث إن جينوم (مجين) ڤيروس الإنفلونزا يتألف من ثمانية أجزاء مستقلة من الرنا يمكنها أن تتحرك بشكل مستقل مغيرة تراتيبها، لذا يجب أن تُجرى تجارب النشوء هذه بشكل مستقل لكل جزء جيني.
لقد اكتمل لدينا تحليل خمسة من أجزاءالرنا الثمانية الخاصة بڤيروس 1918. لقد أدت مقارنتنا حتى الآن لجينات الإنفلونزا 1918 بالعديد من ڤيروسات الإنفلونزا الأخرى مثل تلك الخاصة بالبشر والخنازير والطيور، إلى وضع ڤيروس 1918 في مصاف ڤيروسات البشر والخنازير وخارج مجموعة ڤيروسات الطيور [انظر الإطار في الصفحة 21]. مع ذلك فقد كان لجينات ڤيروس 1918 بعض خصائص جينات إنفلونزا الطيور. لذا فمن الممكن أن يكون الڤيروس قد نشأ أصلا من مستودع reservoir طيري في وقت ما قبل عام 1918. ومن الواضح أنه بحلول عام 1918 كان الڤيروس قد اكتسب تكيفا كافيا مع الثدييات ليقوم بدور ڤيروس يحدث جائحة في البشر. والسؤال هو أين حدث ذلك؟
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
ثمرة المثابرة
أثناء زيارته ألاسكا في صيف 1949، قابل طالب الطب السويدي <J. هالتن> المبشرين اللوثريين Lutheran missionaries في فيربانكس الذين حدثوه عن حصيلة جائحة 1918 في قرى الإسكيمو. كانت إحداها وهي مستوطنة صغيرة واقعة في شبه جزيرة سيوارد Seward Peninsula تدعى تيلّر ميشن قد محيت تقريبا في الشهر11/1918. اضطر المبشرون الذين أصيبوا بالهلع حينئذ إلى استدعاء الجيش الأمريكي ليساعد على دفن جثث 72 من الضحايا في قبر جماعي، قاموا بوضع صليبين عليه. اتجه <هالتن> (منتصف اليسار وفي الأسفل) مدفوعا بتلك القصة إلى جامعة أيوا Iowa ليبدأ بدراسة الدكتوراه في الميكروپيولوجيا (علم الأحياء الميكروية). وهناك كان دائم التفكير في جائحة 1918 والتساؤل عن إمكانية استرجاع الڤيروس الفتاك الذي سببها، من جثث الضحايا التي ربما تكون محفوظة في الجليد السرمدي permafrost وذلك بغية دراسته. في صيف 1951 تمكن <هالتن> من إقناع اثنين من أعضاء هيئة التدريس في جامعة أيوا، هما عالم ڤيروسات وعالم پاثولوجيا (أمراض)، بزيارة القرية التي كانت تدعى عندئذ بريڤگ ميشن Brevig Mission. قام العلماء بعد حصولهم على موافقة كبار رجال القبيلة بفتح القبر وتمكنوا من الحصول على عينات من نسج خلوية من الأجزاء المتبقية من رئات بعض الضحايا
لدى قيامنا بتحليل جينة الهيماگلوتينين لڤيروس 1918 وجدنا أن تسلسلها يختلف عن تسلسلات الڤيروسات الطيرية اختلافا أكبر بكثير من اختلاف الأنماط الفرعية 1957 H2 و 1968 H3. استنتجنا بالتالي أن جينة 1918 H1 إما أن تكون قد بقيت لبعض الزمن في عائل وسيط، حيث تجمعت فيها الكثير من التبدلات عما كان عليه التسلسل الطيري الأصلي، أو أن تكون الجينة قد جاءت مباشرة من ڤيروس طيري لكنه كان مختلفا بشكل واضح عن تسلسلات H1 الطيرية المعروفة.
بغية التحقق من الاحتمال الثاني حول ما إذا كانت جينات H1 الطيرية قد تبدلت تبدلا أساسيا خلال العقود الثمانية التي تلت جائحة 1918، فقد تعاونّا مع علماء متحف التاريخ الطبيعي التابع للمعهد السميثسوني Smithsonian ومع جامعة ولاية أوهايو. وبعد فحص الكثير من الطيور المحفوظة منذ ذاك العهد تمكنت مجموعتنا من عزل سلالة إنفلونزا طيرية من النمط الفرعي H1 من إوزة من نوع برانت Brant كانت قد جمعت عام 1917 وحفظت في الإيثانول، وذلك ضمن مجموعة الطيور الخاصة بالمعهد السميثسوني. وقد ظهر أن تسلسل H1 الطيري عام 1917 كان وثيق القرابة بسلالات H1 الطيرية الحديثة العائدة لأمريكا الشمالية، وهذا يشير إلى أن التسلسلات الطيرية H1 لم تتبدل إلا قليلا عبر الثمانين عاما الماضية. إن السَّلسلة الواسعة لسلالات H1 طيرية إضافية قد تكشف عن سلالة أكثر تشابها مع 1918 HA، ولكن قد لا نجد أي H1 طيري مشابه لسلالة 1918، لأن الپروتين HA لم يتشكل reassort في الواقع بدءا من سلالة طيرية.
في هذه الحالة، لا بد أنها امتلكت عائلا وسيطا. والخنازير هي من الاحتمالات الواردة حيث إنه من المعروف أنها قابلة للإصابة بالڤيروسات من النوعين البشري والطيري. وقد شوهد بالفعل، تفشٍ متزامن للإنفلونزا في البشر والخنازير أثناء جائحة 1918، إلا أننا نعتقد أن اتجاه الانتقال كان على الغالب من البشر إلى الخنازير. وهناك العديد من الأمثلة عن سلالات ڤيروس إنفلونزا A البشرية أصابت الخنازير منذ عام 1918، في حين أن سلالات إنفلونزا الخنازير لم تعزل من البشرإلا في حالات فردية. ومع ذلك، ولتقصي إمكانية أن يكون الپروتين 1918 HA قد بدأ كشكل طيري ثم تكيف بشكل تدريجي ليتلاءم والثدييات كعائل وذلك في الخنزير، بحثنا في مثال حالي عن نشوء الڤيروسات الطيرية في الخنازير ـ هو ذرية إنفلونزا HIN1 طيرية توطدت في الخنازير الأوروبية عبر ال25 سنة الماضية. وجدنا أنه حتى بعد مرور 20 سنة من التطور في الخنازير فإن عدد التبدلات الحادثة في التسلسلات الطيرية لم يكن معادلا للتبدلات الحادثة في سلالة جائحة 1918.
لدى تطبيقنا مثل هذه التحليلات على أربع جينات أخرى لڤيروس 1918، وصلنا إلى النتيجة نفسها: إنه من الممكن جدا أن يكون الڤيروس الذي أشعل جائحة 1918 هو سلالة طيرية، انعزلت لبعض الوقت خلال نشوئها، عن جميعة pool جينات الإنفلونزا النموذجية الخاصة بالدجاج المائي، أي إنها ـ شأنها شأن سلالة ڤيروس السارس التاجي SARS corona virus ـ ظهرت بين البشر من مصدر حيواني مازال مجهولا.

الاستقصاءات المستقبلية
إن تحليلنا لخمسة أجزاء من رنا ڤيروس 1918 قد ألقى بعض الضوء على منشئه، وهو يشير بقوة إلى أن الڤيروس الجائحي كان السلف المشترك لذراري H1N1 البشرية والخنزيرية اللاحقة، وأنها لم تنشأ من الخنازير. إن تحليل الجينات الڤيروسية لم يعط حتى اليوم أي دليل محدد حول الفوعة الاستثنائية لسلالة ڤيروس 1918. إلا أن التجارب التي أجريت على ڤيروسات مهندسة وراثيا تحتوي على جينات 1918 تشير إلى أن پروتينات معينة من پروتينات ڤيروس 1918 يمكنها أن تحفز تضاعفا سريعا للڤيروس وأن تستثير رد فعل مناعيا شديد التخريب لدى العائل المصاب.
نأمل مستقبلا أن نتمكن من تصنيف سلالة الڤيروس الجائحي 1918 في المكان الصحيح مع ڤيروسات الإنفلونزا السابقة واللاحقة له مباشرة. لم يكن السلف المباشر للڤيروس الجائحي، أي سلالة ڤيروس الموجة الأولى أو السلالة الربيعية، يتمتع بالفوعة الاستثنائية التي ميزت بالموجة الخريفية، كما كان انتشاره أقل سهولة. ونقوم حاليا بالبحث عن عينات رنا الإنفلونزا من ضحايا الموجة الربيعية بغية تعرف اختلافات جينية ما بين السلالتين يمكنها أن توضح سبب كون الموجة الخريفية أكثر حدة من الموجة الربيعية. وبشكل مشابه فإن العثور على عينات رنا لڤيروس إنفلونزا بشرية لما قبل عام 1918 سوف يوضح تلك الأجزاء الجينية من ڤيروس 1918 التي كانت حديثة (مستجدة) تماما في البشر. ويمكن تفسير نسبة الوفيات المرتفعة بين اليافعين خلال جائحة 1918 بأن الڤيروس قد اكتسب بعض الخصائص من سلالات كانت منتشرة من قبل، وكان الأناس الأكبر سنا قد اكتسبوا بعض المناعة ضدها. كما أن العثور على عينات H1N1 من عام 1920 وما بعد ذلك سوف يساعدنا على فهم التطور اللاحق لڤيروس 1918 إلى أشكال أقل فوعة.
يجب أن نتذكر أن آليات نشوء سلالات الإنفلونزا الجائحية مازالت حتى الآن غير مفهومة تماما. وبما أن السلالات الجائحية عامي 1957 و 1968 كانت تمتلك پروتينات HA شبيهة بپروتينات إنفلونزا الطيور، لذا يبدو مرجحا أنها نشأت عن إعادة الترتيب المباشر لسلالات ڤيروسية بشرية وطيرية. ومع ذلك، لم يتم بتاتا تعرف الظروف الحقيقية لأحداث إعادة الترتيب الحاصلة، لذا فإننا لا نعرف الزمن الذي استغرقته السلالات الجديدة لتتطور إلى جائحة بشرية.
إن السلالة الجائحية عام 1918 هي أكثر مدعاة للحيرة، ذلك أن تسلسل جيناتها لا يتوافق مع إعادة الترتيب المباشر من سلالة طيرية معروفة ولا مع تكيف سلالة طيرية في الخنزير. وفي حال ثبت أن ڤيروس 1918 اكتسب جينات جديدة بآلية تختلف عما يحدث في السلالات الجائحية اللاحقة فإنه سيكون لذلك مدلولات مهمة فيما يتعلق بالصحة العامة. ومن الممكن أن يكون مصدر مختلف قد أسهم في الفوعة الاستثنائية لسلالة 1918. إن سَلْسَلة عدد أكبر بكثير من ڤيروسات إنفلونزا الطيور، والبحث حول عوائل متوسطة بديلة خلاف الخنازير، مثل: الدواجن والطيور البرية والجياد، قد تعطي دلائل أكبر حول مصدر جائحة 1918، وإلى أن يتوفر لدينا فهم أفضل لمنشأ مثل تلك السلالات، فإن الجهود المبذولة للكشف والوقاية قد تغفل عن ملاحظة بداية الجائحة التالية.
المراجع
Devil's Flu: The World's Deadliest Influenza Epidemic and the Scientific Hunt for the Virus That Caused It. Pete Davies. Henry Holt and Co., 2000.
America's Forgotten Pandemic: The Influenza of 1918. Second edition. Alfred W. Crosby. Cambridge University Press, 2003.
The Origin of the 1918 Pandemic Influenza Virus: A Continuing Enigma. Ann H. Reid and Jeffery K. Taubenberger in Journal of General Virology, Vol. 84, Part 9, pages 2285-2292; September 2003. Global Host Immune Response: Pathogenesis and Transcriptional Profiling of Type A Influenza Viruses Expressing the Hemagglutinin and Neuraminidase Genes from the 1918 Pandemic Virus. J. C. Kash, C. F. Basler, A. Garcia-Sastre, V. Carter, R. Billharz, D. E. Swayne, R. M. Przygodzki, J. K. Taubenberger, M. G. Katze and T. M. Tumpey in Journal of Virology, Vol. 78, No. 17, pages 9499-9511; September 2004.
Scientific American, January 2005 المؤلفان <K .J. تاوبِنْبِرگر> ـ <H .A. ريد> ـ <G .Th. فانينگ>