دورة كريبس
دورة حمض الستريك المعروفة بدورة كريبس Krebs Cycle أو حلقة حمض الليمون تعرف أيضاً بدورة الأحماض ثلاثية الكربوكسيل TCA هي سلسلة من التفاعلات الكيميائية محفزة بالانزيمات لها دور مركزي هام في جميع الخلايا الحية التي تستخدم الأكسجين في التنفس الخلوي. وتمثل دورة حمض السيتريك في الكائنات الحيوائية جزء من المسلك الاستقلابي المكتنف في التحويل الكيميائي للكاربوهيدرات والدهون و البروتين الى ثاني أكسيد الكربون و الماء ليولد الطاقة الممكن للجسم استخدامها, و تلك الدورة هي المسلك الثالث من أربعة مسالك مكتنفة في تقويض الكربوهيدرات و تصنيع الأدينوزين ثلاثي الفوسفات , والمسالك الثلاثة الأخريات هن: تحلل السكر و تأكسد البيروفات و السلسلة التنفسية , ولهذه الدورة أهمية شديدة حتى في الخلايا التي تقوم بعملية التخمر حيث أنها تعطي طلائع لعدة مركبات مثل الأحماض الأمينية.
التعريف
دورة كريبس وتعرف أيضاً بدورة كريز سلسلة تفاعلات كيميائيّة تحدث في جميع الخلايا التي تحتاج إلى الأكسجين لتحيا. ويطلق عليها أيضا دورة حمض السيتريك أو دورة حمض ثلاثي الكربوكسيليك. حصل هانز أدولف كريز، الكيميائي الحيوي الألماني المولد، عام 1953م على جائزة نوبل للفسيولوجيا (علم وظائف الأعضاء) أو الطب لاكتشافه منهج المعالجة. والدورة جزء مهم في الأيض، حيث تقوم الخلايا فيها بتغيير الغذاء إلى طاقة.
وتغير التفاعلات الكيميائية في الدورة أستيل الأنزيم التميمي أ، وهو أحد أشكال حمض الخليك، إلى ثاني أكسيد الكربون وماء. ويتكون أستيل الإنزيم التميمي أ في الجسم من تحلل الدهون والبروتينات والكربوهيدرات.
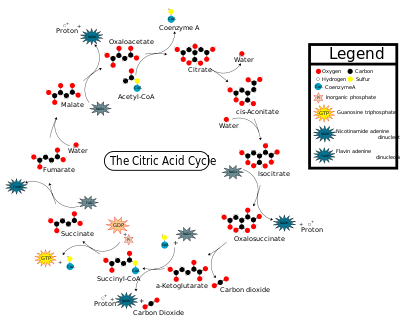
وتبدأ دورة كريبس باتحاد أستيل الإنزيم التميمي أ مع حمض الأوكسالوأستيك، وهو منتج نهائي للدورة نفسها، ويتشكل عن توافق هذه الحموض حمض السيتريك. ويَنْتُج عن إعادة تنظيم جزيئات حمض السيتريك حمض الأيسوستريك الذي يمر عبر سلسلة من المراحل ليشكل خلالها ستة حموض وسيطة، وهي ألفا ـ كيتوجلوتاريك، والسكسينيك، سكسنيل الإنزيم التميمي أ، والفيوماريك، والماليك وأخيرًا الأوكسالوأستيك، ومن ثَمَّ يُصبح حمض الأوكسالوأستيك جاهزاً للاتحاد مع أستيل الإنزيم التميمي أ لبدء دورة أخرى
استعراض عام
يتم أكسدة جزيئان من الكربون الى ثاني أكسيد الكربون و تخزن الطاقة الناتجة من هذا التفاعل على شكل GTP (جوانوزين ثلاثي الفسفات) و NADH (نيكوتين أميد ثنائي النيوكليوتيد مختزل من NAD) و FADH2 (فلافين أدينين ثنائي النيوكليوتيد), و يتم التخزين عن طريق NAD , FADH2 وهما تميما الانزيمات Coenzymes مستخدما في الفسفتة التأكسدية.
| الخطوة | Substrate | الإنزيم | نوع التفاعل | المتفاعلون Reactant/ Coenzymes |
نواتج التفاعل Product/ تميم الإنزيم Coenzymes |
التعليق | ||
|---|---|---|---|---|---|---|---|---|
| 1 | Oxaloacetate | Citrate synthase | تكثيف | Acetyl CoA + H2O |
CoA-SH | |||
| 2 | Citrate | Aconitase | تجفاف | H2O | ||||
| 3 | cis-Aconitate | Aconitase | تميه Hydration | H2O | ||||
| 4 | Isocitrate | Isocitrate dehydrogenase | أكسدة | NAD+ | NADH + H+ |
|||
| 5 | Oxalosuccinate | Isocitrate dehydrogenase | نزع الكربوكسيل Decarboxylation | H+ | CO2 | |||
| 6 | α-Ketoglutarate | α-Ketoglutarate dehydrogenase | Oxidative decarboxylation |
NAD+ + CoA-SH |
NADH + H+ + CO2 |
|||
| 7 | Succinyl-CoA | Succinyl-CoA synthetase | substrate level phosphorylation | GDP + Pi | GTP + CoA-SH |
or ADP->ATP | ||
| 8 | Succinate | Succinate dehydrogenase | أكسدة | FAD | FADH2 | |||
| 9 | Fumarate | Fumarase | Addition (H2O) | H2O | ||||
| 10 | L-Malate | Malate dehydrogenase | أكسدة | NAD+ | NADH + H+ | |||
المنتجات
نتائج الدور الأول من الدورة هم: جُزَيئة GTP, ثلاثة جزيئات NADH, جزيئة FADH2 و جزيئتان CO2, و لأن كل دورة تؤدي الى انتاج جزيئتان من أسيتيل التميم الانزيمي أ المعروف ب acetyl CoA من كل جزيئة كلوكوز فان كل جزيئة گلوكوز تتطلب دورتان كريبس فتكون النتيجة : جزيئتان GTP, ستة جزيئات NADH , جزيئتان FADH2 و أربعة جزيئات CO2.
| الوصف | المتفاعلون | المنتجات |
| اجماعي التفاعلات في دورة حمض السيتريك: | أسيتيل التميم الانزيمي أ + 3 NAD+ + FAD + GDP + Pi + 2 H2O | → CoA-SH + 3 NADH + 3 H+ + FADH2 + GTP + 2 CO2 |
| تجميع التفاعلاتالتي تحدث خلال أكسدة البيروفات و دورة حمض السيتريك يعطي تفاعل أكسدة البيروفات قبل السلسلة التنفسية: | حمض بيروفيك + 4 NAD+ + FAD + GDP + Pi + 2 H2O | → 4 NADH + 4 H+ + FADH2 + GTP + 3 CO2 |
| تجميع التفاعلات السابقة مع التفاعلات التي تحدث خلال تحلل السكر يعطي تفاعل أكسدة الكلوكوز قبل السلسلة التنفسية: | كلوكوز + 10 NAD+ + 2 FAD + 2 ADP + 2 GDP + 4 Pi + 2 H2O | → 10 NADH + 10 H+ + 2 FADH2 + 2 ATP + 2 GTP + 6 CO2 |
(the above reactions are equilibrated if Pi represents the H2PO4- ion, ADP and GDP the ADP2- and GDP2- ions respectively, ATP and GTP the ATP3- and GTP3- ions respectively).
Considering the future conversion of GTP to ATP and the maximum 32 ATP produced by the 10 NADH and the 2 FADH2 (see the theoretical yields for cellular respiration), we see that each glucose molecule is able to produce a maximum of 36 ATP.
انظر أيضاً
- نزع كربوكسيل التأكسدي
- حمض السيتريك
- تحلل السكر Glycolysis
- نزع كربوكسيل البيروفات
- الفسفتة التأكسدية
- دورة كريبس (الاختزالية) العكسية
- هانز أدولف كريبس
المراجع
- Neil A. Campbell (2005). Biology (7th ed. ed.). Benjamin Cummings. ISBN 978-0805371468.
{{cite book}}:|edition=has extra text (help); Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - Solomon, E.P. (2005). Biology. Brooks Cole. ISBN 978-0534495480.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|editions=ignored (help); Unknown parameter|month=ignored (help)
المصادر
وصلات خارجية
- An animation of the citric acid cycle at Smith College
- A video of members of The Ohio State Marching Band enacting the Krebs cycle at YouTube
- Notes on citric acid cycle at rahulgladwin.com
- A more detailed tutorial animation at johnkyrk.com
- A citric-acid cycle self quiz flash applet at University of Pittsburgh
- The chemical logic behind the citric acid cycle at ufp.pt
دورة حمض الستريك السبيل الأيضي
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||