بنية الحراريات
ساهم بشكل رئيسي في تحرير هذا المقال
|
بنية الحراريات structure of refractories
مقدمة
الحراريات هى مواد إنشائية قادرة على تحمل درجات الحرارة العالية مع احتفاظها بخصائصها الفيزيائية في جو الفرن عند ملامستها للأخباث والفلزات المنصهرة والغازات الأَكَّالَة. وتستخدم الحراريات على نطاق واسع في معظم عمليات التصنيع عالية درجة الحرارة، مثل صهارة النحاس والألومنيوم وصناعة الزجاج والخزفيات والأسمنت وتجهيز الخامات وتنقية البترول وصناعة البتروكيماويات. إلا أن صناعة الحديد والصلب تستهلك وحدها نحو ثلثى إجمالى الحراريات المستخدمة، وقد تم في هذه الصناعة تطوير العديد من الحراريات. والأدوار الأساسية للحراريات هى المحافظة على استمرار العمليات التى تتم في درجات حرارة عالية، مع أقل تكلفة تشغيل ممكنة، والتحكم في استهلاك الطاقة كما هو مطلوب.
أشكال الحراريات
نحو 70% من كل الحراريات المستخدمة في الصناعة تصنع في هيئة طوب أو أشكال، مثل طوب العَقْد والطُوَيْبَات (الشَقْفَات) والطوب العِدِل والصابونى والإسفينى والتاجى والمقوس الظهر والمستدق والعَضُدِى، وغير ذلك من الأشكال الخاصة والمسجلة. وقد يكون الطوب المشكل مترابط كيميائيا باستخدام إضافات تمنح الطوب مقاومة (ميكانيكية) في درجة حرارة الغرفة، وقد يحرق أو تشعل فيه النار في درجات حرارة عالية، للحصول على الخصائص الفيزيائية المرغوبة. والثلاثين في المائة المتبقية من الحراريات المستخدمة تُنتَج في هيئة حراريات سائبة غير مشكلة، تسمى عادة الحراريات اللاوصلية، وتضم هذه المجموعة عدة أصناف، هى حراريات تُصب (قابلة للصب) وخلائط القذف والحراريات اللدنة وخلائط الدَكّ. وعند الإنشاء توضع هذه المواد مباشرة في الفرن لتكوين البطانة الحرارية ثم تحرق في مكانها. والملاطات تعتبر أيضاً حراريات لاوصلية؛ وتتكون من حبيبات ومُلَدِّنَات، وتستخدم في رَصّ (صَفّ) وتثبيت الطوب الحرارى. وتصنف الملاطات إلى ملاطات هوائية الشَكّ (هوائية التجمد) وأخرى حرارية الشك. الأنواع الهوائية الشك تحتوى على كيمياويات مثل سليكات الصوديوم أو البوتاسيوم أو روابط (مواد رابطة) فوسفاتية تمدها بالمقاومة (الميكانيكية) المناسبة في درجة حرارة الغرفة. وتحتوى الملاطات حرارية الشَكّ على حبيبات حرارية بدون إضافات كيميائية، وتكتسب مقاومتها فقط بعد التسخين لدرجات حرارة عالية حيث تتكون رابطة خزفية بين الحبيبات. وغالباً ما تستخدم المواد الحرارية العازلة في التطبيقات المرتفعة درجة الحرارة للتقليل من فقدان الحرارة وتوفير الوقود. ويمكن أن توجد هذه الحراريات في هيئة طوب عازل أو لوح أو بطانية من ألياف حرارية، أو أشكال خاصة مصبوبة تحت تفريغ. ونادراً ما تستخدم طلاءات خزفية تتحمل درجات الحرارة العالية في التطبيقات الحرارية، لأنها تُستهلك عادة بسرعة أو تَبْلَى وتهترئ عن مواضعها أثناء الخدمة. إلا أنه في تطبيقات معينة يمكن إطالة عمر الأجزاء المصنوعة من فلزات حرارية أو من الحراريات الخزفية العادية بوضع طبقة عالية الكثافة من مادة حرارية على سطحها بالرش باللهب أو البلازما. وهذه الطلاءات محدودة الاستخدام في بعض التطبيقات الخاصة ولا تستخدم في الأفران المعتادة.
التركيبات الكيميائية
chemical compositions
تتكون معظم الحراريات الصناعية من أكاسيد فلزات أو من الكربون أو الجرافيت أو من كربيد السليكون. أما المواد الحرارية الأجدد مثل الكربيدات والنيتريدات والبوريدات والسليسيدات فتستخدم عامة في تطبيقات خاصة لإعتبارات اقتصادية. والأكاسيد الحرارية الأكثر استخداماً هى SiO2 وAl2O3 وMgO وCaO وCr2O3 وZrO2. والحراريات المحتوية على SiO2 وZrO2 يشار إليها بالحراريات الحمضية، وتلك المحتوية على MgO وCaO بالحراريات القاعدية، وتلك المصنوعة من Al2O3 وCr2O3 بالحراريات المتعادلة. وهذا ترميز قديم، وبالرغم من أنه ليس حقيقياً جداً من الناحية الكيميائية، إلا أنه جد مفيد في مناقشة تفاعلات الأخباث عالية درجة الحرارة الملامسة للحراريات. فعلى سبيل المثال تتفاعل المغنسيا أو الجير مع السليكا في درجة حرارة أدنى بكثير من نقطة انصهار أى منهما. وبناءاً على ذلك يجب الانتباه والحذر للتأكد من أن التركيبات الكيميائية للمواد الحرارية المستخدمة في تلامس مع بعضها البعض لا تتفاعل في درجة حرارة أدنى من تلك المتوقعة أثناء الخدمة (جدول 1).
تصنع الحراريات الشائعة عادة من المواد الموجودة في الطبيعة، ولكن مع الاتجاه إلى استخدام درجات حرارة أعلى في العديد من التطبيقات زادت الحاجة لاستخدام الأكاسيد المجهزة كيميائياً والأكاسيد عالية النقاوة. ومن الأمثلة على ذلك الألومينا عالية النقاوة، المنتجة بطريقة "باير"، والمغنسيا عالية النقاوة المُحَضَّرَة بترسيب هيدروكسيد المغنسيوم أو بتكليس كلوريد الكالسيوم، والزركونيا المجهزة كيميائياً. الأنواع والمواد الخام
طوب السليكا
يصنع طوب السليكا silica brick من المعادن الموجودة طبيعياً مثل المرويت (الكوارتزيت) وتجمعات حصى السليكا والنوفاكوليت. وهذه المواد الخام المستخدمة في صناعة حراريات السليكا المعتادة، كما هو مبين في جدول 2، يجب أن تحتوى على مستويات سليكا عالية (99% أو أكثر) وشوائب منخفضة وخاصة الألومينا والقلويات، لأنها يمكن أن تقوم بدور الصهور أثناء حرق المادة الحرارية فتقلل من مقاومة المنتج النهائى الكلية للحرارة. ويترابط هذا الطوب عادة بإضافة 3-3,5% CaO. وتتكون كمية قليلة من الزجاج عند الحرق، وتتحول البقية المتبقية من مادة المرويت الخام إلى تريدميت وكريستوبليت.
يتصف هذا الطوب بمعامل تمدد عالٍ جداً بين درجة حرارة الغرفة و500 ْم، ومن ثم يجب أن يسخن ويبرد ببطئ شديد في هذا المدى من درجات الحرارة. ولطوب السليكا قدرة كبيرة على تحمل الأحمال في درجات الحرارة العالية. وتوجد منه ثلاثة أنواع: طوب فائق الأداء، ومحتواه من الألومينا والقلويات منخفض جداً؛ وطوب معتاد أو عادى الأداء؛ وطوب أفران الكوك.
السليكا المصهورة fused silica. تنتج السليكا المصهورة بالصهر الفعلى لأنواع مخصوصة من رمال السليكا عالية الرتبة منتقاة خصيصاً لهذا الغرض في فرن قوس كهربائية أو مقاومة كهربائية أو أى فرن آخر مناسب. فيتم تحويل المادة الخام المتبلورة إلى زجاج غير متبلور يسمى السليكا المصهورة. تختلف خصائص هذه المادة الخام المصهورة جدياً عن خصائص رمل المرو الأصلى، وخاصة تميز السليكا المصهورة بمعامل تمدد حرارى منخفض جداً. وتتصف كذلك منتجات السليكا المصهورة بموصلية حرارية منخفضة ومقاومة ممتازة للصدمات الحرارية. وقد وجدت تركيبات السليكا المصنوعة من السليكا المصهورة تطبيقات مناسبة في الترقيع الساخن للبطانات الحرارية، وتطبيقات أخرى مثل الأحجبة الحرارية حيث تتفاقم الصدمات الحرارية.
طوب نصف سليكى
يصنع هذا الطوب من الطين (الطَفْل) السليكى ويحتوى في أكثره على كريستوبليت مترابط بطور زجاجى. ويحتوى هذا الطوب في المعتاد على 18-25% ألومينا و72-80% سليكا. ولهذا الطوب مقدرة ممتازة على تحمل الأحمال حتى 1300 ْم، ولكنه مثل طوب السليكا العادى ذو تمدد حرارى عالٍ نسبياً بين درجة حرارة الغرفة و500 ْم. كربيد السليكون
يُصنع كربيد السليكون المستخدم كمادة حرارية خام بواسطة مصانع إنتاج الحبيبات الحاكة (الكاشطة)، ويتم ذلك في أفران كهربائية من خليط من الكوك ورمل السليكا. المادة النهائية صلدة للغاية (9,1 على مقياس "موز") وذات موصلية حرارية عالية ومقاومة جيدة في درجات الحرارة المرتفعة، بالإضافة إلى معامل تمدد منخفض ومقاومة جيدة جداً للصدمات الحرارية. هذه الخصائص بالإضافة إلى استقرار كيميائى وفيزيائى كبير، فهو ينحل في درجة حرارة 2185 ْم، ويتأكسد ببطء في الهواء، ولكنه مستقر نسبياً في الظروف المُخْتَزِلة، هذه الخصائص جعلته مادة قيمة للاستخدامات الحرارية. تستخدم هذه المادة في درجات حرارة 1535-1650 ْم في العديد من التطبيقات، مثل الأشكال الحرارية لجدران أفران الغلايات، وطوب البناء الشبكى للمسترجعات الحرارية، واللِفاعات (وهى حواجز تفصل بين اللهب وبين الشحنة في الفرن ومفردها لِفَاع)، وقضبان مَزَالِق الأفران، وملحقات القمائن وأحواض وحدات تنقية الخارصين. يوضح جدول 3 تحليل لبعض رتب كربيدات السليكون الحرارية.
يصنع هذا الطوب من الطين الحرارى (أو يقال له الطين النارى) الموجود في الطبيعة، والذى يحتوى في المعتاد على ألومينا تترواح بين 25 و45%. وتزداد مقاومته للحرارة مع زيادة محتواه من الألومينا ونقص محتوى الشوائب مثل القلويات وأكسيد الحديد. وتقاس مقاومة الحرارة لهذه النوعية من الطوب في الغالب بالمخروط البيرومترى المكافئ، الذى يبين تأثير درجة الحرارة والزمن على المادة الحرارية. تتكون معظم الأطيان الحرارية من معدن الكاولينيت (Al2O3•2SiO2•2H2O)، مع كميات صغيرة من معادن طينية أخرى ومرويت (كوراتزيت) و أكسيد حديد وتيتانيا وشوائب قلوية. وتستخدم الأطيان كما تستخرج (تُعدَّن) أو بعد التكليس، الذى تتكسر خلاله الأطيان إلى موليت (3Al2O3•2SiO2) وزجاج سِليكى. وتتوزع مكامن الطين الحرارى توزيعاً كبيراً في أنحاء العالم.
وبالرغم من أن الأطيان كانت من بين أول المواد الخام المستخدمة في عمل الحراريات، إلا أن استخدامها تناقص لأن الاحتياجات المطلوبة من الحراريات الحديثة قد استدعت استبدالها بمواد أفضل أداءاً. ومع ذلك فالأطيان ما زالت مادة هامة في الصناعة. فقد تستخدم كمواد رابطة أو ملدنات أو كرُكَام لإنتاج الحراريات، يوضح جدول 4 بعض خصائص الأطيان.
طوب الألومينا العالية
يحتوى الطوب في هذا التصنيف على ألومينا في المدى من 45 – 100%، ويصنع عامة بدمج الطين مع البوكسيت و/أو الألومينا الاصطناعية. والبوكسيت هو مادة خام موجودة في الطبيعة، تتكون في أكثرها من معدن الجبسيت (Al(OH)3)، مع كميات متفاوتة من الكاولينيت، وكميات قليلة من شوائب أكسيد الحديد والتيتانيا، ولأن الفقد عند الاشتعال كبير في البوكسيت، فإنه يُكَلَّس أولاً في درجات حرارة عالية لتحويله إلى حبيبات كثيفة، متكونة في الأساس من الكوراندم (Al2O3) والموليت.
الكاولين البوكسيتى أو البوكسيت السليكى وهى مواد خام ضمن هذه العائلة تستخدم في تصنيع الحراريات، وتحتوى على 50-70% ألومينا. تُعدَّن هذه المواد وتخلط وتحرق في قمائن دوارة لإنتاج بطانة متعددة الاستعمالات من سليكات الألومنيوم المُكلَّسة، تترواح في محتواها من الألومينا ما بين 50 إلى أكثر من 70 %. يبين جدول 5 أمثلة على الكاولينات البوكيستية.
السلِّيمانيت. وهى مجموعة معادن خالية من الماء وصيغتها Al2O3•SiO2، وهى السليمانيت والأندلوسيت والكِيانيت. والأخيران هما الأكثر شيوعاً تجارياً. تحتوى هذه المعادن على نحو 60% ألومينا، والباقى يتكون من السليكا وقليل من شوائب الحديد والتيتانيا، انظر جدول 6. تتحول هذه المعادن عند التسخين إلى خليط من الموليت وزجاج سليكى، ويتكون موليت كامل في درجة حرارة 1300-1400 ْم. ويصحب تحول الكيانيت عند التسخين تمدد بين 16 – 18% في الحجم، في حين يتمدد السليمانيت والأندلوسيت فقط بنسب مئوية قليلة. ولهذا يستخدم الكيانيت غالباً كأحد المكونات في الملاطات لمنع الانكماش.
البوكسيت. البوكسيت bauxite في حالته الخام هو مجموعة من المعادن الموجودة طبيعياً، تتكون أساساً من الجبسيت (Al2O3•3H2O) أو الدياسپور أو البيوميت (AlO(OH)) بالإضافة إلى أطيان متنوعة. البوكيستات الحرارية المتكلسة موجودة في صور محددة كما في جدول 7، وتُنْتَج من خامات منخفضة الحديد ومنخفضة السليكا خلال عمليات تكليس، تتم في قمائن دوارة أو قمائن بتيار سحب سفلى. يتم التكليس في مدى درجات حرارة من 1400-1800 ْم، ويتم فيه تحويل البوكسيت الخام إلى معادن الكورندم والموليت، وكلاهما مكونان شديدا المقاومة للحرارة. ومن الخصائص الهامة للبوكسيتات احتواؤها على أقصى نسب للألومينا (85% أو أكثر)، وأقصى كثافة حجمية، وأدنى شوائب مثل أكسيد الحديد والتيتانيا والقلويات (Na2O وK2O وLiO2)، والعناصر الأرضية القلوية (الأتربة القلوية) (CaO وMgO).
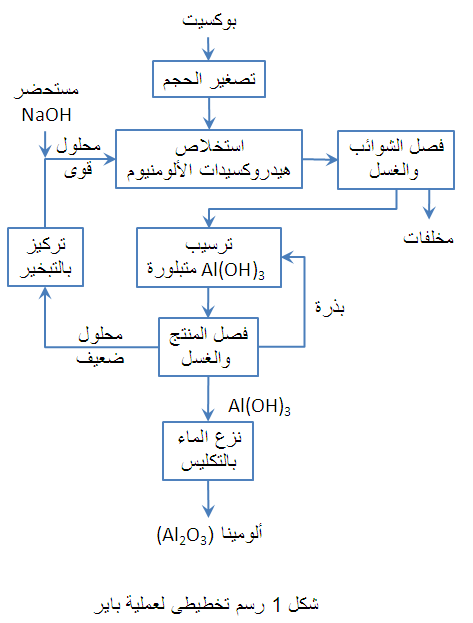
الألومينا. alumina والألومينا عالية النقاوة المنتجة بعملية "باير" متاحة في صورة متفاعلة أو متكلسة، وتباع الأخيرة تحت الاسم التجارى "ألومينا صفيحية". والألومينا المصهورة متاحة أيضاً كمنتج مصنوع من البوكسيت، الذى رُكِّز أثناء الصهر بإزالة الحديد والسليكا في صورة حديد سليكونى (فروسليكون). وقد تصنع رُتَب خاصة من الألومينا من منتجات عملية باير. يوضح شكل 1 رسم تخطيطى لعملية "باير"، ويوضح شكل 2 منتجاتها واستخداماتها المختلفة. وفى العموم تستخدم الألومينات المتكلسة لتعزيز ترابط الحراريات أثناء التصنيع أو الاستخدام، بينما تشكل المنتجات الصفيحية والمصهورة ركامات شديدة الاستقرار. وتتكون الألومينا الصفيحية بالتكليس في 1925 ْم، بينما تتكون الألومينا المصهورة الأكثر كثافة بالصهر الكلى ثم التجميد السريع. وبالإضافة إلى ذلك فحبيبات الموليت المصهورة عالية النقاوة المصنوعة من خلائط الألومينا عالية الجودة والسليكا متاحة أيضاً. يوضح جدول 8 خصائص الألومينات المختلفة.
مجموعة المغنسيا أو المغنسيا-الجير
وتشمل هذه المجموعة جميع الحراريات المصنوعة من المغنسيات والدولوميت الاصطناعية، وهى تشكل أهم مجموعة من الحراريات المستخدمة لعمليات صناعة الصلب القاعدية. وتستخدم كل هذه المواد في المقام الأول كمصدر للمغنسيا (MgO).
المغنسيا
يتم إنتاج المغنسيات magnesia الحديثة عالية النقاء في عمليات محكومة جيداً. المصادر الرئيسية للمغنسيات هى المحاليل الملحية (الآبار العميقة في الغالب) ومياه البحر. يُرسب هيدروكسيد المغنسيوم، Mg(OH)2، من هذه المصادر عن طريق التفاعل مع الدولوميت المكلس أو الحجر الجيرى؛ و أحد المصادر يستخدم عملية مفاعل حديثة. وتتم تصفية (ترشيح) هيدروكسيد المغنسيوم الناتج لزيادة محتواه من المواد الصلبة. ثم يمكن إدخال عجينة الترشيح مباشرة إلى قمينة دوارة لانتاج مغنسيا حرارية الرتبة، ولكن الأكثر شيوعا الآن هو تكليس عجينة الترشيح في نحو 900-1000 ْم (1650 -1830 ْف)، عادة في أفران متعددة المواقد/المجامر، لتحويل هيدروكسيد المغنسيوم إلى مغنسيا نشطة. ثم تُقولب هذه المغنسيا المكلسة أو تُكوَّر لحرقها إلى مغنسيا حرارية الرتبة كثيفة، عادة في قمائن قائمة تصل إلى درجات حرارة حوالى 2000 ْم (3630 ْف). المنتج النهائى هو مغنسيا متكلسة. وتنتج المغنسيا المصهورة بصهر مغنسيا حرارية الرتبة أو بادئة من مغنسيا أخرى في فرن قوس كهربائية. ثم تُزال الكتلة المنصهرة من الفرن ويتم تبريدها وتكسيرها حتى تبدأ مسيرتها من أجل استخدامها في الحراريات.
الشوائب في المغنسيا محكومة بتركيب المصدر الأصلى للمغنسيا (المياه المالحة أو مياه البحر)، وتركيب الدولوميت المكلس أو الحجر الجيري، وتقنيات التجهيز. ولا سيما كميات ونسبة CaO وSiO2 فهى تخضع لرقابة صارمة، ويُحافظ على B2O3 في مستويات متدنية للغاية. النتائج النهائية هى مغنسيات حرارية عالية الدرجة جاهزة لتصنيع المنتجات الحرارية. يبين جدول 9 وجدول 10 تركيب الرتب المختلفة من المغنسيا.
النقاوة العالية هامة للغاية لأن MgO لديها مقامة عالية للحرارة ومقاومة جيدة للأخباث القاعدية. فالتقليل من المحتوى الكلى للشوائب في المغنسيا مهم جداً، لأن الشوائب تؤثر على مقاومة الحرارة والأداء. والنسبة العالية لـ CaO/SiO2، ويفضل أن تكون 2:1 أو أعلى بقليل، هى الأمثل للحفاظ على مقاومة عالية للحرارة في المغنسيا. وبانخفاض إجمالى الشوائب إلى نحو 1 ٪ أو أقل يقل تأثير وأهمية نسبة CaO/SiO2 شيئاً فشيئاً. الكثافة العالية تقلل من الترشُّح وانحلال حبيبات المغنسيا عن طريق الخبث. ويوفر الحجم الكبير للبلورات (محقق كأفضل ما يمكن المغنسيا المنصهرة) مساحة سطح أقل لهجوم الخبث. انخفاض محتوى B2O3 يضمن مقاومة عالية في درجات الحرارة المرتفعة للطوب المحروق. وانخفاض نسب الجير إلى SiO2 مطلوبة في بعض المنتجات، حيث تستخدم MgO مع مواد خام أخرى (مثل Cr2O3) أو لمقاومة التميه إلى الحد الأقصى. وطوب المغنسيا الحرارى متاح في عدة صور: مترابط كيميائياً، ومترابط بالزفت، ومحروق، ومحروق ثم مشرب في الزفت.
الدولوميت
الدولوميت dolomite الطبيعى المزدوج الكربونات (CaCO3•MgCO3) يمكن تحويله إلى دولوميت حرارى (CaO MgO) بالحرق في درجة حرارة عالية. وهناك عدد محدود من رواسب الدولوميت موجود في العالم ذو انتظام ونقاوة وسلوك تحميص مرضٍ يمكن تجهيزها إلى دولوميت حرارى بتكلفة معقولة. الدولوميت عالى النقاوة هو ما يحتوى على أكبر من 97٪ CaO + MgO وشوائب من 0,5إلى 3٪. معظم رواسب الدولوميت عالى النقاوة يصعب تكليسها وتلبيدها إلى كثافة عالية، وعادة ما تتطلب طرق خاصة للحصول على دولوميت حرارى مقبول. السليكا وأكسيد الحديد والألومينا هى أكثر الشوائب شيوعا في الدولوميت عالى النقاوة. انظر جدول 11.
يمتاز الدولوميت بمقاومة ممتازة للحرارة ومستقر جداً استقراراً ديناميكياً حرارياً في تلامسه مع الصُلب (الفولاذ) أو خبث صناعة الصلب. لاحظ في جدول 12 أن CaO هو الاكثر استقراراً من بين الأكاسيد الحرارية الشائعة في درجات حرارة صناعة الصلب.
جزء الجير lime الحر من الدولوميت المحروق تمام الحرق يمكن أن يتفاعل مع رطوبة الغلاف الجوى، فيسبب ذلك تحول المادة إلى مسحوق وتنهار. درجة التَمَيُّه تحت ظروف معينة من الزمن ودرجة الحرارة والرطوبة النسبية يعتمد على نسبة الجير والشوائب الموجودة في المادة، وعلى كثافة الحبيبات التى تحققت أثناء عملية حرق التام. وفى الممارسة العملية مع مواد التعبئة والتغليف والتقنيات الحديثة جنبا إلى جنب مع غيرها من وسائل حماية المنتجات، يمكن إطالة عمر تخزين منتجات الدولوميت. ومنها أن طوب الدولوميت غير المحروق غالباً ما يكون مترابطاً بالقطران (القار) أو الزفت، والطوب المحروق غالباً ما يُشَرَّب في القطران أو الزفت لإطالة عمر الخدمة.
مجموعة المغنسيا-كروم
خامات الكروم chrome ores أو الكروميت chromite وغالباً ما تسمى الاسبنيلات الغنية (المثراة) بالكروم، هى أعضاء من مجموعة معادن الاسبنيل موجودة بشكل طبيعي. هذه المواد تتميز كلها بنقط انصهار عالية نسبيا، والاستقرار في درجة الحرارة جيدة (ولا سيما في الاتحاد الحرارى مع المغنسيت)، وخصائص تمدد حرارى معتدلة.
خامات الكروم مشمولة في صيغة (Mg•Fe+2) (Cr,Al,Fe+3)2O4 حيث يمكن أن يحل المغنسيوم بديلا عن الحديد والألومنيوم عن الكروم. والمعادن الزائدة التى يقال لها عادة الشوائب المعدنية غالبا ما ترتبط بهذه الخامات. وتسهم الشوائب المعدنية بالسليكا المتبقية والجير والمغنسيا الإضافية إلى خام الكروم. التحكم والوضع وكمية الشوائب المعدنية لا تقل أهمية للخصائص النهائية للحراريات عن التركيبة الكيميائية الأساسية للخام. غالبا ما تتم ترقية الخامات بواسطة تقنيات الفصل الميكانيكى للتقليل من الشوائب. ومن ثم فمركزات الكروم ذات الشوائب المنخفضة، كما هو مبين في جدول 13، هى غالباً المادة التجارية المستخدمة في الحراريات. وCr2O3 النقى المفصول كيميائيا من الكروميت يمكن أن يستخدم في تركيبة مع أكاسيد أقل تكلفة لانتاج خصائص حرارية محددة.
بالإضافة إلى المواد الخام الحرارية القاعدية المكونة من المغنسيا تامة الحرق وخام الكروم كمواد أولية، هناك تركيبات أخرى من المغنسيت-كروم ضمن هذه السلسلة، فمجموعة مواد المغنسيت-كروم الخام موجودة أيضاً وتشمل المغنسيت-كروم المتكلسين معاً، والمغنسيت-كروم المصهور، والبيكروكروميت الاصطناعية وهى مزيج من المغنسيت وأكسيد الكروم. تظهر في جدول 14 تركيبات نموذجية للمغنسيت-كروم.
الزركون / الزركونيا
الزركون zircon أو سليكات الزركونيوم (ZrO2•SiO2)، هو مادة خام موجودة بشكل طبيعى لها مقاومة ممتازة للحرارة، ثقلها النوعى (4,5 - 4,6 جم/سم3) عالى بصورة غير عادية بالمقارنة مع معظم المواد الحرارية. وتشمل المصادر الزركون الرئيسية رمال غرب أستراليا الطبيعية، شرق ولاية فلوريدا، ساحل ناتال الشرقى في شمال جنوب أفريقيا، وبلدان المجموعة الاقتصادية الأوروبية وجمهورية الصين الشعبية. عادة ما يتم العثور على الزركون مع رمال معادن ثقيلة أخرى، وعلى الأخص معادن التيتانيا. ويبين جدول 15 خصائص الزركون.
يُنتج أكسيد الزركونيوم (ZrO2) أو يسمى الزركونيا zirconia تجاريا مثل معدن الباديليت الموجود بشكل طبيعي. وقد مثلت صناعة الحراريات أحد مجالات النمو الرئيسية للزركونيوم. الارتفاع النسبى في درجة إنصهار باديليت، جنبا إلى جنب مع المقاومة الفائقة للتآكل والتحات، تجعل الزركونيا مكوناً مثالياً للعديد من نظم الحراريات. الزركونيا في الحالة طبيعية توجد في طور ذو بلورة أحادية الميل. وعند تسخينها، تخضع الزركونيا لتحول طورى (للنظام الرباعي) وانكماش للحجم يبلغ نحو 5 ٪، ومع زيادات إضافية في درجة الحرارة يستقر الشكل (البلورى) المكعبى عند 2350 ْم. ولمواجهة هذه التحولات الطورية الضارة، يمكن استقرار الزركونيا على الطور المكعبى بإضافة كميات صغيرة من الكالسيا والمغنسيا، أو الإيتريا، ونتيجة لذلك الاستقرار تتحسن مقاومة الصدمات الحرارية وخصائص التحميل الساخن في المنتج النهائي. الزركونيا متوفرة في الصورة الطبيعية أو المستقرة أو المصهورة، وهذه الأخيرة غالبا ما تكون خليطاً مع الألومينا والسليكا أو غيرها من الأكاسيد المتوافقة. ويبين جدول 16 الخصائص النموذجية للزركونيا.
مجموعة الكربون
تستخدم صور مختلفة من الكربون carbon بشكل متزايد في الحراريات. فعلى سبيل المثال، الحراريات الحديثة تَستخدِم صور جرافيت مختلفة في توليفة مع أكاسيد أخرى لمنح الحراريات خصائص خاصة. وقد يكون الجرافيت ذو طبيعة اصطناعية حيث يُنتج بتسخين كوك البترول المكلس إلى 3000 ْم أو قد يكون طبيعياً حيث يستخرج من الصين والمكسيك وكندا، إلخ. ويمكن أن تُنْتَج بعض الحراريات من الكربون الخالص أو الجرافيت الخالص للاستخدام في تطبيقات الأجواء شديدة الاختزال.
وعموما، يستخدم الجرافيت graphite في الحراريات من أجل الحد من الخصائص التَبَلْلُّيَّة للمواد الحرارية التى تؤثر بشكل مباشر في التآكل الناتج عن الخبث، ولرفع الموصلية الحرارية التى ستؤدى إلى تحسين مقاومة الصدمات الحرارية. في الحراريات المبنية على أكسيد-كربون، قد يتغير محتوى الكربون من محتوى منخفض مثل 4-5 ٪ وقد يصل إلى 30-35 ٪. كما نلاحظ أنه بزيادة المحتوى الجرافيتى تزداد الموصلية الحرارية للحراريات، ولكن تقل كثافتها في الوقت ذاته. هذه النتيجة ترجع أساساً إلى حقيقة أن كثافة الجرافيت أقل بكثير من كثافة المواد الحرارية الأخرى المستخدمة. وهناك اختلافات أخرى واضحة في شكل (مورفولوجية) الجرافيت بالمقارنة مع غيره من المواد الحرارية، فمواد الجرافيت التى تستخدم في الحراريات عادة ما تكون ذات بنية قُشَارِيَّة flaky (أى تتكون من قُشيرات)، ومن ثم فإن هذه القشيرات لا تستسلم لظواهر تعبئة الجسيمات كما تفعل الجسيمات الحبيبية.
يبين جدول 17 خصائص عدة أنواع من الجرافيت. يُنَقَّى الجرافيت القُشيرى عادة إلى محتويات عالية للغاية من الكربون: 99 ٪ بالوزن كربون أو أعلى، وتستعمل هذه التنقية عملية كيميائية وأخرى حرارية؛ ولهذه الخطوات تأثير كبير على سعر المواد.
الحراريات الخاصة
Cordierite
المقالة مازالت قيد الإنشاء
المصادر الرئيسية
(1) E. Ruh, "Refractories for the Iron and Steel Industries" (الحراريات المستخدمة في صناعات الحديد والصلب), Encyclopedia of Materails Sceince and Engineering, Pergamon Press, 1986, pp. 4140-45. (2) E. Ruh, "Refractories for the Nonferrous Metallurgical Industries" (الحراريات المستخدمة في الصناعات الفلزية غير الحديدية), Encyclopedia of Materails Sceince and Engineering, Pergamon Press, 1986, pp. 4145-50. (3) D. H. Hubble, R. O. Russell, H. L. Vernon and R. J. Marr, "Chapter 4: Steelmaking Refractories" (حراريات صناعة الصلب), in "Steel Making and Refining Volume", Making, Shaping and of steel AISE Steel Foundation, Pittsburgh, PA, USA, 1998, pp. 227-90. (4) معجم الحراريات والأفران الصناعية، حمدى يس دسوقى، أمين أحمد قاسم، أنور محمود عبد الواحد، المؤسسة الشعبية للتأليف في لايبزغ ومؤسسة الأهرام، 1981. (5) معجم مصطلحات الحديد والصلب، محمد عبد العزيز خطاب، أنور محمود عبد الواحد، حسن مرعى، المؤسسة الشعبية للتأليف في لايبزغ ومؤسسة الأهرام، 1974.