بروميد الحديد الثنائي
| |
| الأسماء | |
|---|---|
| اسم أيوپاك
بروميد حديد ثنائي
| |
| أسماء أخرى
بروميد الحديدوز
بروم الحديديك ثنائي بروميد الحديد | |
| المُعرِّفات | |
| رقم CAS | |
| ECHA InfoCard | 100.029.244 |
CompTox Dashboard (EPA)
|
|
| الخصائص | |
| الصيغة الجزيئية | FeBr2 |
| كتلة مولية | 215.65 غ/مول |
| المظهر | بلورات صفراء بنية |
| الكثافة | 4.63 غ/سم3 |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | منحل في الماء |
| قابلية الذوبان | إيثانول ميثانول |
| المخاطر | |
تبويب الاتحاد الاوروپي (DSD)
|
قالب:مؤذ |
| توصيف المخاطر | R20-R36/37/38 |
| تحذيرات وقائية | S26-S36 |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
بروميد الحديد الثنائي مركب كيميائي له الصيغة FeBr2، ويكون على شكل بلورات صفراء بنية.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص
- ينحل بروميد الحديد الثنائي في الماء بشكل جيد، كما ينحل في كل من الميثانول والإيثانول ورباعي هيدرو الفوران.
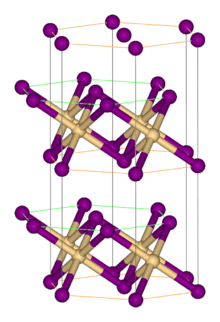
- بلورات بوميد الحديد الثنائي تتبع نظام بلوري مشابه لنمط يوديد الكادميوم، وتكون المجموعة الفراغية له P3m1، وثوابت الشبكة البلورية كالتالي [1]
- a = 377,6 pm und c = 622,7 pm. في هذه البنية البلورية تتراصف طبقات من أيونات البروميد، تتوضع أيونات الحديد الثنائي فيما بينها ضمن الفجوات ثمانية الوجوه. [2]
التحضير
يحضر بروميد الحديد الثنائي من التفكك الحراري لمركب بروميد الحديد الثلاثي عند درجات حرارة تفوق 200°س.
- 2FeBr3 –Δ→ 2FeBr2 + Br2
كما يمكن أن يحصل على بروميد الحديد الثنائي من تفاعل فلز الحديد مع بروميد الأمونيوم:
- 2NH4Br + Fe → FeBr2 + NH3 + H2
التفاعلات
- يتفاعل بروميد الحديد الثنائي مع (C2H5)4NBr ليعطي [(C2H5)4N] 2FeBr4. وهو معقد معقد عضوي فلزي.[3]
- يتفاعل بروميد الحديد الثنائي مع البروم وأيون البروميد ليشكل معقد ملون له الصيغة [FeBr3Br9]-. تتداخل المدارات في هذا المعقد. [4]
المراجع
- ^ Einkristall-Strukturbestimmung bon Eisen(II)-bromid (Kapitel in Dissertation).
- ^ Haberecht, J.; Borrmann, H.; Kniep, R. "Refinement of the Crystal Structure of Iron Dibromide, FeBr2 Zeitschrift für Kristallographie - New Crystal Structures (2001), volume 216, page 510.
- ^ N. S. Gill, F.. B. Taylor Inorganic Syntheses 1967, volume 9, page 136-142.
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5