مركب كيميائي
المركب الكيميائي هو مادة كيميائية تكونت من عنصرين أو أكثر,بنسبة ثابتة تحدد تركيبه. فمثلا الماء (H2O) مركب يتكون من ذرتين هيدروجين لكل ذرة أكسجين.
وبصفة عامة فإن هذه النسبة يجب أن تكون ثابتة لبعض الإعتبارات الفيزيائية, وليس طبقا للإختيارات البشرية. ولهذا السبب فإن المواد مثل النحاس الأصفر, الموصل الفائق تعتبر خليط أو سبيكة وليست مركب.
ومن الخواص المميزة للمركب أن له معادلة كيميائية (معادلة جزيئية). وتصف هذه المعادلات نسبة الذرات الموجودة به, وعدد الذرات الموجودة في جزيء واحد من المادة, وعلى هذا فيكون شكل الإيثان C2H4 وليس CH2). ولا تحدد المعادلة إذا كان المركب يتكون من جزيئات. فمثلا كلوريد الصوديوم (ملح الطعام NaCl) هو مركب أيوني.
ويمكن للمركبات أن يكون لها حالات عديدة. معظم المركبات توجد في هيئة صلبة. كما أن المركبات الجزيئية يمكن أن توجد أيضا في حالة سائلة أو غازية. ويمكن لكل المركبات أن تتفكك إلى مركبات أصغر أو إلى ذرات لو تم تعريضها للحرارة لدرجة معينة (تسمة درجة حرارة التفكك. وكل مركب له رقم CAS (رقم لتعريف كل المركبات).
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
أنواع المركبات
أمثلة على المركبات الكيميائية
الماء
أشهر وأهم مادة على الأرض بعد الهواء . الماء مركب يتكون من عنصرين هما الهيدروجين والأوكسيجين ، وصيغته التي نأخذ فيها النسبة الأبسط لعدد الذرات المتحدة مع بعضها فهي H2O ، أما النسبة الوزنية ( الكتلية ) (غم : غم أو كغم : كغم ... الخ ) بين الهيدروجين والأوكسيجين
= 1 : 8
O : H
ملح الطعام
مادة شائعة وهامة في التغذية البشرية ، ملح الطعام مركب يتكون من عنصرين هما : الصوديوم والكلور وصيغته هي NaCl .
النسبة الوزنية ( الكتلية ) بين الصوديوم والكلور في الملح ( اسمه العلمي كلوريد الصوديوم ) .
= 46 : 71 تقريباً .
Cl : Na
= 2 : 3 تقريباً .
تبين لك من التمهيد السابق أن العدد الكبير من المركبات ناتج عن اتحاد عدد محدود من العناصر . إذ يبلغ عدد العناصر النشطة والفعالة والتي لها مركبات في الطبيعة حوالي ثمانين عنصراً فقط . وقد لا تستغرب إذا عرفت أن عنصراً واحداً فقط هو الكربون يكون باتحاده مع ذرات كربونية أخرى ومع عدد محدود من العناصر ملايين المركبات ، وأنه يشتق من هذه الملايين ملايين أخرى وهي المعروفة باسم المركبات العضوية ، فكل البروتينات والأنزيمات والسكاكر والدهون والفيتامينات وغيرها هي أمثلة لهذا النوع من المركبات العضوية ذات الأهمية للحياة
ما التغيرات التي تطرأ على العناصر عندما تكون المركبات ؟
ما الذي يحدث بين عنصر وآخر حينما يتكون المركب ؟ دعنا نجيب على هذا السؤال بمصطلح غير علمي وغير دقيق في البداية فنقول تتكون جسور بين الذرة والأخرى ، هذه الجسور تغير من خواص وطبيعة العناصر وتعطي خواص جديدة هي خواص المركب الكيميائي . إن الجسور التي تربط بين الهيدروجين والأوكسجين في الماء تكسب الماء خواص جديدة مختلفة عن خواص كل من الهيدروجين والأوكسيجين .
ينطبق الأمر نفسه على كل المركبات الأخرى المعروفة
ما الذي يكون هذه الجسور بين ذرات العناصر ؟
الجواب بكل بساطة إنها الإلكترونات ، أهي كل الكترونات الذرة ؟ لا ، بل إنها جزء بسيط من الكترونات الذرة ، تلك هي الإلكترونات الأبعد عن النواة والمعروفة باسم إلكترونات التكافؤ أو إلكترونات الربط ، بل إن البعض من إلكترونات التكافؤ هذه قد لا تشارك في مد هذه الجسور كما سنشاهد في الأمثلة بعد قليل . إذن الجسور الرابطة هي جسور إلكترونية .
نعلم من دراستنا لموضوع المادة أن الجزيئات هي الوحدات الأساسية التي تتكون منها المواد مهما كان نوعها ، وأن الجزيئات بدورها تتكون من وحدات أصغر هي الذرات ، فالجزيء عادة يتكون من ذرتين أو أكثر ولكن الجزيء في الغازات النبيلة مثل الهيليوم وبقية أفراد مجموعته فيتكون من ذرة واحدة فقط .
وفي حالة الفلزات يتكون الجزيء الواحد من عدد كبير من الذرات قد تبلغ 36 ذرة أو أكثر ، ونظراً لذلك رأى العلماء أن نكتب الصيغة الجزيئية للفلزات بأبسط صورة وهي ذرة واحدة ، فنعتبر جزيء الفلز في التفاعلات الكيميائية مكوناً من ذرة واحدة فقط .
ونعلم من دراستنا لموضوع الذرات والتعادل أن ذرات العناصر تتكون من دقائق مادية صغيرة وعديدة ولكن أشهرها وأهمها ثلاثة أنواع هي :
دقائق خفيفة وسالبة الشحنة يتكون منها الغلاف الخارجي للذرات .
1. الإلكترونات (ـ) :
دقائق ثقيلة ( إذا ما قورنتت بالإلكترونات ) ، موجبة الشحنة وتوجد في حيز صغير في قلب الذرة نطلق عليه اسم النواة .
2. البروتونات (+) :
دقائق ثقيلة ، تعادل البروتونات في كتلتها تقريباً ( وهي في الواقع أثقل بمقدار ضئيل) وهي لا تحمل شحنة ، لذلك غير
3. النيوترونات ( ï ) :
مسؤولة عن شحن الذرات،وهي بذلك تختلف عن الإلكترونات ( السالبة) والبروتونات ( الموجبة ) في أنها دقائق متعادلة .
يكون عدد البروتونات (+) = عدد الإلكترونات(ـ) في النوع ذاته من الذرات لذلك تكون ذرات العنصر الواحد متعادلة في الوضع الطبيعي . تتميز الكترونات الذرات بأنها خفيفة وحرة الحركة خاصة كلما ابتعدت عن النواة الموجبة ( لوجود البروتونات فيها ) التي تجذبها حسب قانون الجذب العام المعروف " الشحنات المختلفة تتجاذب والشحنات المتشابهة تتنافر ) . وهكذا فبسبب خفة الإلكترونات وحركتها الدائمة وبسبب كون الخارجية منها بعيدة عن النواة فإن لدى بعضها القدرة على التحرر والإنفلات ليكون روابط مع ذرات أخرى من نفس نوعه أو مع أنواع ( عناصر ) مغايرة ، بينما تبقى البروتونات محتجزة في نواة الذرة ولا يسمح لها بالمغادرة. إذن يمكن للذرة أن ينقص فيها عدد الإلكترونات حينما تبتعد عنها بعض إلكتروناتها فتصبح موجبة (لماذا )؟؟؟
أو أن يزيد فيها عدد الإلكترونات حينما تقترب منها إلكترنات من ذرة ( أو ذرات ) أخرى أي أنها تكسب الإلكترونات فتصبح سالبة ( لماذا ) ؟؟؟
إذا خسرت الذرة إلكتروناً أو إلكترونات أصبحت أيوناً موجباً ، وإذا كسبت إلكتروناً أو إلكترونات أصبحت أيوناً سالباً .
أمثلة على مركبات كيميائية وطريقة الربط فيها
1. الماء:
يتكون من الهيدروجين وعدد الإلكترونات الخارجية فيه = 1 ( وفي الواقع في حالة الهيدروجين لا يوجد غيره ) ، ومن الأوكسيجين وعدد الإلكترونات الخارجية فيه = 6 ( يوجد إلكترونان داخليان لا يتدخلان في الربط ) ، فإذا مثلنا الإلكترونات الخارجية بنقاط حول رمز الذرة ( حسب طريقة لويس ) يكون :
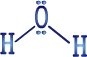
وعند تكون الماء تنتج رابطتان بسبب ازدواج الإلكترونات المنفردة بين الهيدروجين والأوكسيجين وينتج جزيء الماء الذي يمكن أن نمثله كما يلي حسب تراكيب لويس
لاحظ أن ذرة الهيدروجين الواحدة عملت رابطة واحدة بينما ذرة الأوكسيجين الواحدة عملت رابطتين . إذن في الماء يعمل الأوكسيجين جسرين رابطين مع ذرتي الهيدروجين . يسمى هذا الربط باسم الربط التساهمي أو المشترك ويمكنك مقارنته بشركة تجارية بين شخصين يقدم كل واحد منهما حصة في الشركة تساوي حصة الآخر . لاحظ أن هنالك زوجين من إلكترونات التكافؤ للأوكسيجين لم يشتركا في الربط لاحظ أيضاً أن الإلكترونات جميعها قد أصبحت مزدوجة وأن ذرة الأوكسيجين قد انطبقت عليها قاعدة الثمانية ، بينما انطبقت على ذرة الهيدروجين قاعدة أخرى هي قاعدة الثنائي ( راجع رموز لويس والأيونات ) وهي من القواعد التي توصل إليها العالم لويس بعد قاعدة الثمانية وتنص على ما يلي : ازدواج الإلكترونات يؤدي إلى استقرار الذرات أو بطريقة أخرى " تستقر الذرات إذا ازدوجت الإلكترونات " .
2. غاز الميثان.
يتكون من الهيدروجين والكربون ، حيث ترتبط أربع ذرات هيدروجين مع ذرة كربون .
إذن الربط هنا تساهمي أو مشترك كما هو الحال مع الماء وقد أسهمت كل ذرة هيدروجين بالكترون واحد لتعمل أربعة جسور رابطة بينها وبين ذرة الكربون وكل جسر منها يتكون من إلكترونين . انطبقت قاعدة الثمانية على الكربون وقاعدة الثنائي على الهيدروجين .تكتب صيغة الميثان البسيطة على شكل CH4.
4. من الأمثلة الأخرى على مركبات تساهمية :
ثاني أوكسيد الكربون CO2 ، ثاني كبريتيد الكربون CS2 ، ورابع كلوريد الكربون CCl4 ، الكحول ، النشادر ( الأمونيا ) ... وغيرها .
اكتب صيغ لويس للمركبات التالية :
أ. NH3 ب.CS2 ج.CO2 د.CCl4
لكتابة الصيغ الكيميائية للمركبات يجب ملاحظة التالي:
- عدد إلكترونات تكافؤ العنصر الأول ؟ اكتب رمز لويس للعنصر .
- عدد الروابط التي تستطيع أن تعملها ذرة العنصرالأول.
- عدد إلكترونات تكافؤ العنصر الثاني ؟ اكتب رمز لويس للعنصر.
- عدد الروابط التي تستطيع أن تعملها ذرة العنصر الثاني.
- صيغة لويس للمركب.