خلية حامضية
| Eosinophil | |
|---|---|
 3D rendering of eosinophil | |
 Eosinophil under the microscope (400x) from a peripheral blood smear. Red blood cells surround the eosinophil, two platelets at the top left corner. | |
| Details | |
| النطق | /ˌiːoʊˈsɪnəfɪl/)[1] |
| الجهاز | Immune system |
| Identifiers | |
| MeSH | D004804 |
| TH | TH {{{2}}}.html HH2.00.04.1.02017 .{{{2}}}.{{{3}}} |
| FMA | 62861 |
| المصطلحات التشريحية | |
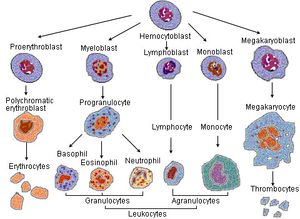
الخلية الحامضية أو كريات الدم البيضاء الحامضية إنگليزية: Eosinophil أحد أنواع الخلايا البيض. يبرز دورها الدفاعي عند الإصابات بالطفيليات. وهي أحد مكونات جهاز المناعة تشكل نسبة 2-4 % من كريات الدم البيضاء و تكون نواتها على شكل فصين صغيرين وتحتوي على حبيبات لذلك فهي تصنف من ضمن خلايا الدم البيضاء ذات الحبيبات (المحببة) و يبرز دورها الدفاعي عند الإصابة بالطفيليات. تسيطر مع الخلايا البدينة والخلايا القاعدية على الآليات المرتبطة بالحساسية والربو فلها دور في إحداث تفاعلات الحساسية. وهي حببيبات تتطور خلال تكوُّن الدم في نخاع العظام قبل الهجرة إلى الدم.
هذه الخلايا حمضية أو "محبة للحمض" كما يتضح من تقاربها الكيميائي مع صبغات قطران الفحم: تكون عادةً شفافة وتظهر باللون الأحمر الطوبي عند صبغها باليوزين. يتركز التصبغ في حبيبات صغيرة داخل السيتوبلازم الخلوي، تحتوي على العديد من الوسائط الكيميائية مثل الهستامين والبروتينات مثل بيروكسيداز الحمضات وريبونوكلياز (RNase) وديوكسي ريبونيوكلياز (DNase) وليباز وبلازمينوجين والبروتين الأساسي الرئيسي. تتحرر هذه الوسائط من خلال عملية تسمى زوال الحبيبات بعد تفعيل الحمضات، وهي سامة لكل من الطفيلي والأنسجة المضيفة.
في الأصِحَّاء، تشكل الحمضات حوالي 1-6٪ من خلايا الدم البيضاء، وحجمها حوالي 12-17 ميكرومتر.[2] تتواجد في النخاع والتقاء قشرة ونخاع الغدة الصعترية، وفي الجهاز الهضمي السفلي والمبيض والرحم والطحال والعقد اللمفاوية، ولكن لا توجد في الرئة والجلد والمريء في الظروف العادية. ويرتبط وجود الحمضات في هذه الأعضاء بالمرض. تستمر الحمضات في الدورة الدموية لمدة 8-12 ساعة، ويمكنها البقاء على قيد الحياة في الأنسجة لمدة 8-12 أيام إضافية في غياب التحفيز.[3] أوضح العمل الرائد في الثمانينات أن الحمضات هي حبيبات فريدة من نوعها، لديها القدرة على البقاء على قيد الحياة لفترات طويلة من الزمن بعد نضوجها في الجسم الحي.
التطور
تتطور الحمضات وتنمو في نخاع العظام. وتتميز عن الخلايا الأم النخاعية باستجابتها للسيتوكينات؛ إنترلوكين 3 (IL-3) وإنترلوكين 5 (IL-5) والعامل المحفز لمستعمرات البلاعم والحبيبات (GM-CSF).[4][5][6]
تُنتِج الحمضات وتُخزِّن العديد من البروتينات الحبيبية الثانوية قبل خروجها من نخاع العظام. بعد النضج، تنتشر الحمضات في الدم وتهاجر إلى المواقع الالتهابية في الأنسجة، أو إلى مواقع العدوى بالديدان الطفيلية استجابةً للكيموكينات وبعض الليوكوترين. في هذه المواقع المعدية، يتم تنشيط الحمضات بواسطة السيتوكينات من النوع 2 المُنتَجَة من مجموعة فرعية معينة من الخلايا التائية المساعدة (TH2).[7]
الوظيفة
بعد التنشيط، تشمل وظائف الحمضات المؤثرة إنتاج كلٍ من:
- البروتينات الحبيبية الموجبة وإطلاقها عن طريق عملية زوال الحبيبات[8][9][10]
- أنواع الأكسجين التفاعلية مثل هيبروبروميت والفائق والبيروكسيد[11]
- وسطاء الدهن مثل إيكوزانوات من الليوكوترين (على سبيل المثال، LTC4، LTD4، LTE4) وعائلات البروستاغلاندين (على سبيل المثال، PGE2)[12]
- الإنزيمات، مثل الإيلاستاز.
- عوامل النمو مثل عامل نمو الأنسجة بيتا وعامل النمو المشتق من الصفيحات[13][14]
- السيتوكينات مثل إنترلوكين1 وإنترلوكين2 وعامل نخر الورم ألفا
وبالإضافة إلى ذلك،[15] هناك أيضًا الحمضات التي تلعب دورًا في مكافحة الالتهابات الفيروسية وهو واضح من وفرة RNases داخل حبيباتها، وفي إزالة الفيبرين أثناء الالتهاب. تكافح الحمضات استعمار الديدان وقد تكون مرتفعة قليلا في وجود بعض الطفيليات. وتشارك أيضًا في العديد من العمليات البيولوجية الأخرى مثل تطوير الغدة الثديية في مرحلة ما بعد البلوغ ودورة الوَدَق ورفض الطعم الخيفي والأورام. كما أنها تساعد في عرض المستضد للخلايا التائية.[16]
ويعتبر تراكم الحمضات في الغشاء المخاطي للأنف سمة رئيسية لتشخيص التهاب الأنف التحسسي (الحساسية الأنفية).
بروتينات الحبيبات
بعد التنشيط بواسطة التحفيز المناعي، تفرغ الحمضات لتحرير مجموعة من البروتينات الموجبة الحبيبية السامة لكثير من الأنسجة والقادرة على إحداث تلف الأنسجة.[17] وتشمل:
- البروتين الأساسي الرئيسي
- بروتين حمضي موجب
- بيروكسيداز الحمضات
- سموم عصبية يوزينية[18]
كثرة الحمضات

كثرة اليوزينيات أو الحمضات هي وجود أكثر من 500 حمضة / ميكروليتر من الدم، ويحدث في الأشخاص الذين يعانون من إصابة طفيلية في الأمعاء وفي أمراض الأوعية الدموية المناعية (مثل التهاب المفاصل الروماتويدي) والذئبة الحمامية الجهازية والأمراض الخبيثة مثل سرطان الدم اليوزيني وفرط اليوزينيات النسيلي ومرض هودجكين (فرط اليوزينيات اللمفية) والتهابات الجلد الخطيرة (مثل التهاب الجلد التقشري). أيضًا في مرض أديسون وغيرها من أسباب انخفاض إنتاج الكورتيكوستيرويد (يثبط الكورتيزون مستويات الحمضات في الدم) وحالات ارتجاع المريء (اتتواجد الحمضات فيها في الظهارة الحرشفية للمريء) والتهاب المريء اليوزيني. ومع استخدام بعض الأدوية مثل البنسلين. ولكن ربما السبب الأكثر شيوعًا لفرط الحمضات هو حالات الحساسية مثل الربو. في عام 1989، تسببت إمدادات L-تريبتوفان الملوثة في شكل قاتل من فرط الحمضات معروف باسم متلازمة الألم العضلي من فرط اليوزينيات.
العلاج
من العلاجات المستخدمة لمكافحة أمراض المناعة الذاتية الناجمة عن الحمضات:
- الكورتيكوستيرويدات - تعزز موت الخلايا المبرمج. فيتم تقليل أعداد الحمضات في الدم بسرعة
- العلاج بالأجسام المضادة وحيدة النسيلة - على سبيل المثال، ميبوليزوماب أو ريسليزوماب ضد إنترلوكين-5، ويمنع تكون اليوزينيات
- مضادات تخليق ليكوترين أو مستقبلاته
- إماتينيب (STI571) - يثبط عامل النمو المشتق من الصفيحات لفرط اليوزينيات في سرطان الدم
دراسات الحيوان
داخل الأنسجة الدهنية من الفئران المفتقدة لـ CCR2، هناك عدد متزايد من الحمضات وتنشيط أكبر للبلاعم والنزعة نحو التعبير عن سايتوكين من النوع 2. وعلاوة على ذلك، تمت مبالغة هذا التأثير عندما أصبحت الفئران تعاني من السمنة المفرطة من اتباع نظام غذائي عالي الدهون.[19]
انظر أيضاً
- Eosinopenia, decrease in eosinophil blood count
- Eosinophilia, increase (>500 cells per microliter) in eosinophil blood count
- Hypereosinophilia, extreme increase (>1,500 cells per microliter) in eosinophil blood count
- Clonal hypereosinophilia, presence of a premalignant or malignant clone of eosinophils in bone marrow and blood
- Chronic eosinophilic leukemia
الهامش
- ^ "eosinophil - Definition of eosinophil in English by Oxford Dictionaries". Oxford Dictionaries - English. Retrieved 27 March 2018.
- ^ Young, Barbara; Lowe, joseph o'connell; Stevens, Alan; Heath, John W. (2006). Wheater's Functional Histology (5th ed.). Elsevier Limited. ISBN 0-443-06850-X.
- ^ Young, Barbara; Lowe, James S.; Stevens, Alan; Heath, John W. (2006). Wheater's Functional Histology (5th ed.). Elsevier Limited. ISBN 0-443-06850-X.
- ^ Metcalf D, Begley C, Nicola N, Johnson G (1987). "Quantitative responsiveness of murine hemopoietic populations in vitro and in vivo to recombinant multi-CSF (IL-3)". Exp Hematol. 15 (3): 288–95. PMID 3493174.
- ^ Metcalf D, Burgess A, Johnson G, Nicola N, Nice E, DeLamarter J, Thatcher D, Mermod J (1986). "In vitro actions on hemopoietic cells of recombinant murine GM-CSF purified after production in Escherichia coli: comparison with purified native GM-CSF". J Cell Physiol. 128 (3): 421–31. doi:10.1002/jcp.1041280311. PMID 3528176.
- ^ Yamaguchi Y, Suda T, Suda J, Eguchi M, Miura Y, Harada N, Tominaga A, Takatsu K (1988). "Purified interleukin 5 supports the terminal differentiation and proliferation of murine eosinophilic precursors". J Exp Med. 167 (1): 43–56. doi:10.1084/jem.167.1.43. PMC 2188821. PMID 3257253.
- ^ Wagner LA, Christensen CJ, Dunn DM, et al. (June 2007). "EGO, a novel, noncoding RNA gene, regulates eosinophil granule protein transcript expression". Blood. 109 (12): 5191–8. doi:10.1182/blood-2006-06-027987. PMC 1890841. PMID 17351112.
- ^ Trulson A, Byström J, Engström A, Larsson R, Venge P (2007). "The functional heterogeneity of eosinophil cationic protein is determined by a gene polymorphism and post-translational modifications". Clin Exp Allergy. 37 (2): 208–18. doi:10.1111/j.1365-2222.2007.02644.x. PMID 17250693.
- ^ Hogan S, Rosenberg H, Moqbel R, Phipps S, Foster PS, Lacy P, Kay AB, Rothenberg ME (2008). "Eosinophils: Biological Properties and Role in Health and Disease". Clin Exp Allergy. 38 (5): 709–50. doi:10.1111/j.1365-2222.2008.02958.x. PMID 18384431.
- ^ Lacy P (2005). "The role of Rho GTPases and SNAREs in mediator release from granulocytes". Pharmacol Ther. 107 (3): 358–76. doi:10.1016/j.pharmthera.2005.03.008. PMID 15951020.
- ^ Saito K, Nagata M, Kikuchi I, Sakamoto Y (2004). "Leukotriene D4 and eosinophil transendothelial migration, superoxide generation, and degranulation via beta2 integrin". Ann Allergy Asthma Immunol. 93 (6): 594–600. doi:10.1016/S1081-1206(10)61269-0. PMID 15609771.
- ^ Bandeira-Melo C, Bozza P, Weller P (2002). "The cellular biology of eosinophil eicosanoid formation and function". J Allergy Clin Immunol. 109 (3): 393–400. doi:10.1067/mai.2002.121529. PMID 11897981.
- ^ Kato Y, Fujisawa T, Nishimori H, Katsumata H, Atsuta J, Iguchi K, Kamiya H (2005). "Leukotriene D4 induces production of transforming growth factor-beta1 by eosinophils". Int Arch Allergy Immunol. 137. Suppl 1 (1): 17–20. doi:10.1159/000085427. PMID 15947480.
- ^ Horiuchi T, Weller P (1997). "Expression of vascular endothelial growth factor by human eosinophils: upregulation by granulocyte macrophage colony-stimulating factor and interleukin-5". Am J Respir Cell Mol Biol. 17 (1): 70–7. doi:10.1165/ajrcmb.17.1.2796. PMID 9224211.
- ^ Rothenberg M, Hogan S (2006). "The eosinophil". Annu Rev Immunol. 24 (1): 147–74. doi:10.1146/annurev.immunol.24.021605.090720. PMID 16551246.
- ^ Shi H (2004). "Eosinophils function as antigen-presenting cells". J Leukoc Biol. 76 (3): 520–7. doi:10.1189/jlb.0404228. PMID 15218055.
- ^ Gleich G, Adolphson C (1986). "The eosinophilic leukocyte: structure and function". Adv Immunol. Advances in Immunology. 39: 177–253. doi:10.1016/S0065-2776(08)60351-X. ISBN 9780120224395. PMID 3538819.
- ^ Slifman N, Loegering D, McKean D, Gleich G (1986). "Ribonuclease activity associated with human eosinophil-derived neurotoxin and eosinophil cationic protein". J Immunol. 137 (9): 2913–7. PMID 3760576.
- ^ Bolus, WR; Gutierrez, DA; Kennedy, AJ; Anderson-Baucum, EK; Hasty, AH (October 2015). "CCR2 deficiency leads to increased eosinophils, alternative macrophage activation, and type 2 cytokine expression in adipose tissue". Journal of leukocyte biology. 98 (4): 467–77. doi:10.1189/jlb.3HI0115-018R. PMC 4763864. PMID 25934927.