أستال
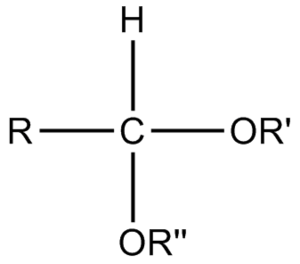
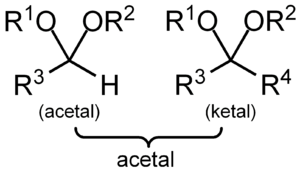
الأستالات acetals هي إترات تحتوي على زمرتي ألكوكسيل RO- مرتبطتين بذرة من الكربون حيث R مجموعة ألكيل كالمتيل CH3- والإتيل C2H5 -- وغيرهما، صيغتها العامة
عادة ما يُميَّز بين الكيتال وبين الأستال حيث يمتلك الكيتال ذرتي كربون مرتبطتين بمجموعة R، في حين يمتلك الأسيتال ذرة واحدة أو اثنتين من الكربون مرتبطة بمجموعة R مثل H-. أما الاصطلاحات الحديثة فتعتبر الكيتال مجموعة جزئية من الأسيتال.
البلاستيك المعروف ببولي أوكسيمثيلين هو متعدد الأسيتال.
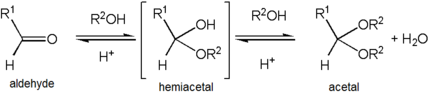
يتكون الأستال عن طريق برتنة مجموعة الهيدروكسيل في الأسيتال الجزئي وفقدانها على شكل جزيئة ماء، يتبعها هجوم سريع من قبل جزيئة كحول نحو الكاربوكتيون المتكون، وبفقدان بروتون من الكحول المرتبط يتكون الأسيتال. يتمتع الأستال باستقرارية إذا ما قورن بالأسيتال الجزئي، ولكن تكونه عكوسي كما هو الحال في الإسترات. فعند إجراء تفاعل تكوين الأسيتال يجب سحب الماء باستمرار من إناء التفاعل وإلا فإن الناتج سيعاني من الحلمهة.
يؤدي تكون الأستال إلى تقليل العدد الكلي للجزيئات الموجودة، لذلك فإنه ليس محبذاً من ناحية الإنتروبية. ولتحسين التفاعل يفضل استخدام أورثواستر كمصدر للكحول. تخضع الألدهيدات والكيتونات إلى عملية تسمى تبادل الأسيتال مع أورثواستر لتعطي الأسيتال، ويستخدم الماء الناتج من تكون الأسيتال في تحلل الأورثواستر مائياً لتكوين كميات إضافية من الكحول يعاد استخدامها في التفاعل مرة أخرى.
خواصها
 |
 |
الأستالات سوائل رجراجة طيارة ذات رائحة إترية، حداها الأولان وهما المتيلال CH2(OCH3)2، وثنائي متيل الأستال CH3CH(OCH3)2 يمتزجان بالماء، وكذلك حال الديوكسولان. وتنقص نسبة انحلالها بازدياد التبادل على الكربون. وتعد الحدود الأولى مذيبات فهي تحل كميات كبيرة نسبياً من الأستيلين في الدرجة الصفر.
ليس للأستالات أهمية تذكر في الاصطناع إلا من حيث كونها مذيبات أحياناً، لكونها مركبات شديدة الثبات لايخربها سوى خماسي كلور الفوسفور أو التحلل بالماءhydrolysis بحضور الحموض القوية. وهي لا تتحلل بالماء في الأوساط المعتدلة أو القلوية لذلك يعد تحويل الألدهيد إلى أستال طريقة لحماية الوظيفة الألدهيدية من فعل الأسس، ويلجأ إليها عندما يراد تحويل وظيفة أخرى في الجزيء. وما تكوّن الأستالات المختلطة الحلقية إلا إحصاراً block للوظيفة الغولية الأولية. وما تكوين الأوكسولان إلا حماية في آن واحد للوظيفة الكربونيلية والوظيفة الگليكولية، كما في الانتقال من الطحول CH2OH-C≡CH إلى قرينه CH2OH-C≡C-R، والذي لا يتم بالمعالجة بالصوديوم، ثم الألكلة، وذلك لتكوّن الإتر R-O-CH2-C≡C-H بل بإحصار الوظيفة الغولية بالانضمام إلى ثنائي هدرو بيران، ثم ألكلة الناتج، وأخيراً تحليل الأستال المختلط تحليلاً مائياً في وسط حمضي للحصول على الغول المطلوب واستعادة ثنائي هدرو بيران:
وجود الأستالات واستعمالاتها
لا يصادف أي أستال ذي وظيفة بسيطة في الحالة الطبيعية إلا أن الوظيفة الأستالية توجد في الأوزيدات المتجانسة holosides وفي عدد كبير من الأوزيدات غير المتجانسة heterosides.
تستعمل الأستالات في صناعة عطور صابون الزينة وفي تركيب بعض أنواع البرنيق varnish العازلة وصموغ المعادن وزجاج الأمان (التريبلكس triplex)، ويعد تفاعل تكون الأستالات المشتقة من الألدهيدات غير الثابتة حافظاً لهذه الأخيرة وذلك لصمود الأستالات لفعل الأكسدة.
للأسيتال أهمية كبيرة في الطبيعة، فعلى سبيل المثال يكون أكثر الأشكال استقراراً لمحلول الجلوكوز هو أسيتال جزئي حلقي، كما أن المالتوز أسيتال مكون من وحدتي كلوكوز.
Acetaldehyde diethyl acetal مادة منكهة مهمة في المشروبات المقطرة.[1]
يستخدم الأسيتال في بعض الأحيان كمجموعة واقية لمجاميع الكاربونيل في الصناعات العضوية، حيث تكون مستقرة نسبة إلى التحلل المائي بواسطة القواعد.
أمثلة
- Dimethoxymethane, a solvent
- Dioxolane
- Methylenedioxy group
- Metaldehyde
- Paraldehyde
- 1,3,5-Trioxane
المصادر
- ^ Volatile Compounds in Foods and Beverages, ISBN 0824783905, http://books.google.com/books?id=_OvXjhLUz-oC, p.554