غشاء اصطناعي
الغشاء الاصطناعي synthetic membrane، هو غشاء مخلق اصطناعياً عادة ما يستخدم عمليات الفصل في المعامل أو في الصناعة. الأغشية الاصطناعية تستخدم بنجاح في عمليات صناعية محدودة أو واسعة النطاق منذ منتصف القرن العشرين.[1] وهناك مجموعة واسعة من الأغشية الاصطناعية المعروفة.[2] يمكن انتاجها من مواد عضوية مثل الپوليمرات والسوائل، وكذلك من المواد اللاعضوية. معظم الأغشية المستخدمة تجارياً في صناعة الفصل مصنوعة من مركبات پوليمرية يمكن تصنيفها تبعاً لكيمياء السطح، تركيب الكتلة، المورفولوجيا، وطريقة الانتاج. الخصائص الكيميائية والفيزيائية للأغشية الصناعية والجزئيات المفصولة وكذلك اختيار القوة الدافعة لتحديد عمل الغشاء في الصناعة هي الضغط وتدريجات التركيز. ومن ثم يعرف هذا النوع بالمرشح. الأغشية الاصطناعية المستخدمة في عملية الفصل يمكن أن تكون ذات تكوين هندسي وتدفقي مهتلف. يمكن تصنيفها أيضاً اعتماداً على التطبيق المستخدمة فيه وعلى نظام الفصل.[2] من أشهر الأغشية الصناعية تنقية المياه، التناضح العكسي، نزع الهيدروجين من الغاز الطبيعي، إزالة جزئيات الخلية عن طريق الترشيح الدقيق والترشيح الفائق، إزالة العضيات الدقيقة من منتجات الألبان، وغسيل الكلى.
أنواع الأغشية وتركيبها
الأغشية السائلة
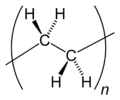
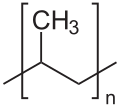
الأغشية الپوليمرية
الأغشية الخزفية
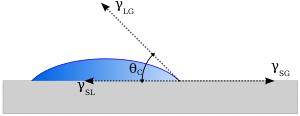
كيمياء السطح
مورفولوجيا الأغشية
انظر أيضاً
الهوامش
المصادر
- Pinnau, I., Freeman, B.D., Membrane Formation and Modification, ACS, 1999.
- Osada, Y., Nakagawa, T., Membrane Science and Technology, New York: Marcel Dekker, Inc,1992.
- Perry, R.H., Green D.H., Perry’s Chemical Engineers’ Handbook,7th edition, McGraw-Hill, 1997.
- Zeman, Leos J., Zydney, Andrew L., Microfiltration and Ultrafitration, Principles and Applications., New York: Marcel Dekker, Inc,1996.
- Mulder M., Basic Principles of Membrane Technology, Kluwer Academic Publishers, Netherlands, 1996.
- Jornitz, Maik W., Sterile Filtration, Springer, Germany, 2006
- Jacob J., Pradanos P., Calvo J.I, Hernandez A., Jonsson G. Fouling kinetics and associated dynamics of structural modifications. J. Coll and Surf. 138(1997): 173-183.
- Van Reis R., Zydney A. Bioprocess membrane technology. J Mem Sci. 297(2007): 16-50.
- Madaeni S.S. The effect of large particles on microfiltration of small particles J. Por Mat. 8(2001): 143-148.
- Martinez F., Martin A., Pradanos P., Calvo J.I., Palacio L.., Hernandez A. Protein adsorption and deposition onto microfiltration membranes: the role of solute-solid interactions. J. Coll Interf Sci. 221(2000): 254-261.
- Palacio L., Ho C., Pradanos P., Calvo J.I, Kherif G., Larbot A., Hernandez A. Fouling, structure and charges of composite inorganic microfiltration membrane. J. Coll and Surf. 138(1998): 291-299.
- Templin T., Johnston D., Singh V., Tumbleson M.E., Belyea R.L. Rausch K.D. Membrane separation of solids from corn processing streams. Biores Tech. 97(2006): 1536-1545.
- Zydney A. L., Ho C. Effect of Membrane Morphology on System Capacity During Normal Flow Microfiltration. Biotechnol, Bioeng. 83(2003): 537-543.
- Ripperger S., Schulz G. Microporous membranes in biotechnical applications. Bioprocess Eng. 1(1986): 43-49.
- Ho C., Zydney A. Protein fouling of asymmetric and composite microfiltration membranes. Ind Eng Chem Res. 40(2001): 1412-1421.