مصاوغ صنوي
المصاوغ الصنوي[1] أو المماكب الصنوي Epimer هو أحد فروع التزامر الفراغي, أو المتزامرات التى لها نفس نوع الترابط رابطة-رابطة, وليست نفس المركب. وتتضمن المتزامرات الفراغية المقابلات الضوئية ، مقابل غير ضوئي, وكلاهما يحتوى على مركز كربوني كايرال (بإستثناء المتزامرات الفراغية, والتى تنتمى إلى أضداد المقابلات الضوئية.
وفى الكيمياء, يكون الصنو تزامر فراغي له تركيب مختلف عند مركز أو أكثر من مراكز الكربون الكايرال. وعندما يساهم الصنو في تكون مركب حلقي فإنه يسمى أنومير. فمثلا السكر ألفا-جلوكوز, بيتا-جلوكوز صنوان. ففى ألفا-جلوكوز تكون مجموعة –OH على أول ذرة كربون أنوميرية في إتجاه معاكس لمجموعة الميثيل. بينما في البيتا-جلوكوز تكون مجموعة –OH موجهة في نفس إتجاه مجموعة الميثيل.
Epimerization is the interconversion of one epimer to the other epimer.
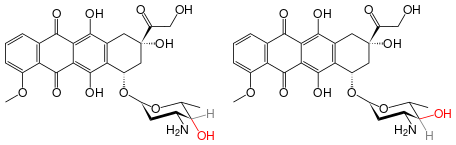
Doxorubicin and epirubicin are two epimers that are used as drugs.
|
Doxorubicin–epirubicin comparison
|
أمثلة
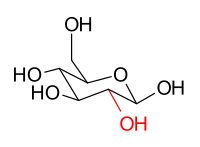
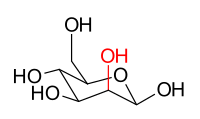
The stereoisomers β-D-glucopyranose and β-D-mannopyranose are epimers because they differ only in the stereochemistry at the C-2 position. The hydroxy group in β-D-glucopyranose is equatorial (in the "plane" of the ring), while in β-D-mannopyranose the C-2 hydroxy group is axial (up from the "plane" of the ring). These two molecules are epimers but, because they are not mirror images of each other, are not enantiomers. (Enantiomers have the same name, but differ in D and L classification.) They are also not sugar anomers, since it is not the anomeric carbon involved in the stereochemistry. Similarly, β-D-glucopyranose and β-D-galactopyranose are epimers that differ at the C-4 position, with the former being equatorial and the latter being axial.
 |
|
β-D-glucopyranose |
β-D-mannopyranose
|
In the case that the difference is the -OH groups on C-1, the anomeric carbon, such as in the case of α-D-glucopyranose and β-D-glucopyranose, the molecules are both epimers and anomers (as indicated by the α and β designation).[2]
 |

|
α-D-glucopyranose |
β-D-glucopyranose
|
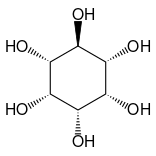
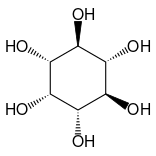
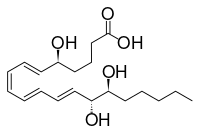
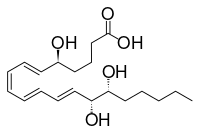
Other closely related compounds are epi-inositol and inositol and lipoxin and epilipoxin.
 |
 |
 |
|
epi-inositol
|
Inositol
|
Lipoxin
|
Epilipoxin
|
المصاوغة الصنوية
Epimerization is a chemical process where an epimer is converted to its diastereomeric counterpart.[3] It can happen in condensed tannins depolymerization reactions. Epimerization can be spontaneous (generally a slow process), or catalysed by enzymes, e.g. the epimerization between the sugars N-acetylglucosamine and N-acetylmannosamine, which is catalysed by renin-binding protein.
The penultimate step in Zhang & Trudell's classic epibatidine synthesis is an example of epimerization.[4] Pharmaceutical examples include epimerization of the erythro isomers of methylphenidate to the pharmacologically preferred and lower-energy threo isomers, and undesired in vivo epimerization of tesofensine to brasofensine.
المراجع
- ^ المعجم الطبي الموحد
- ^ Structure of the glucose molecule
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةClayden - ^ Zhang, Chunming; Trudell, Mark L. (1996). "A Short and Efficient Total Synthesis of (±)-Epibatidine". The Journal of Organic Chemistry. 61 (20): 7189–7191. doi:10.1021/jo9608681. ISSN 0022-3263. PMID 11667626.
المصادر
- ويكيبيديا الإنجليزية.